
2009年版 各論
1 Stage 0~Stage III大腸癌の治療方針
1) 内視鏡治療
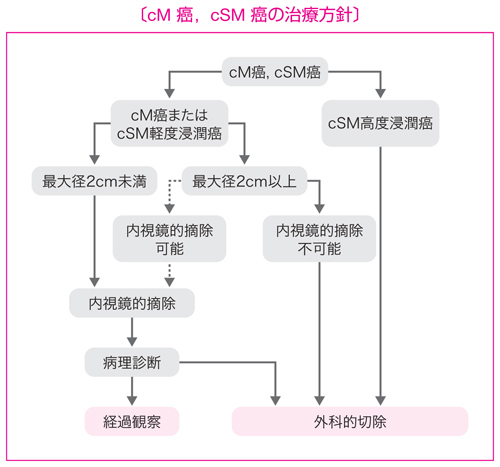
適応の原則
- リンパ節転移の可能性がほとんどなく,腫瘍が一括切除できる大きさと部位にある。
内視鏡的摘除の適応基準
(1)粘膜内癌,粘膜下層への軽度浸潤癌。
(2)最大径 2 cm 未満。
(3)肉眼型は問わない。
- 本法は内視鏡的に大腸の病巣部を切除し,切除組織を回収する方法である。
- 治療法にはポリペクトミー注1,内視鏡的粘膜切除術(EMR:endoscopic mucosal resection) 注2と内視鏡的粘膜下層剥離術(ESD:endoscopic submucosal dissection) 注3がある。
- 内視鏡治療の適応と治療法を決める際には,腫瘍の大きさ,予測深達度,形態に関する情報が不可欠であり,組織型も考慮する必要がある。
注 1 ポリペクトミー
病巣茎部にスネアをかけて高周波電流によって焼灼切除する方法。主として隆起型病変に用いられる。
注 2 EMR
粘膜下層に生理食塩水などを局注して病巣を挙上させ,ポリペクトミーの手技により焼灼切除する方法。スネア法,吸引キャップ法(EMRC:EMR using a cap),などがある。主として表面型腫瘍や大きな無茎性病変に用いられる。
注 3 ESD
病変周囲,粘膜下層にヒアルロン酸ナトリウム溶液などを局注して病巣を挙上させ,専用のナイフで病変周辺の切開,粘膜下層の剥離を進める手技である。主として,EMR で一括切除できない大きな腫瘍が適応である。
2)手術治療
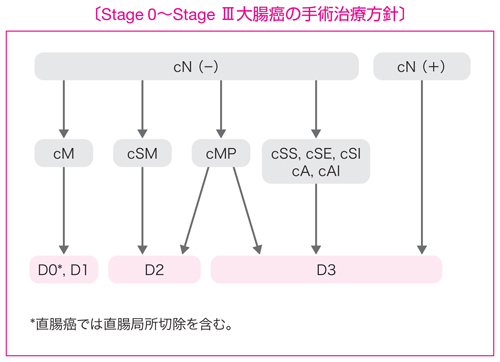
- 大腸癌手術におけるリンパ節郭清度は,術前の臨床所見(c)あるいは術中所見(s)によるリンパ節転移度と腫瘍の壁深達度から決定する。
- 術前・術中診断でリンパ節転移を疑う場合は,D3 郭清を行う。
- 術前・術中診断でリンパ節転移を認めない場合は,壁深達度に応じたリンパ節郭清を行う。
(1)M 癌にはリンパ節転移はないのでリンパ節郭清の必要はないが(D0),術前深達度診断の精度の問題もあり,D1 郭清を行ってもよい。
(2)SM 癌には約 10%のリンパ節転移があること,中間リンパ節転移も少なくないことから,D2 郭清が必要である。
(3)MP 癌の郭清範囲を規定するエビデンスは乏しいが,少なくとも D2 郭清が必要である。しかし,主リンパ節転移が少なからずあること,および術前深達度診断の精度の問題から,D3 郭清を行ってもよい。
【直腸癌の手術治療】
- 直腸切除の原則は,TME(total mesorectal excision)または TSME(tumor−specific mesorectal excision)である。
- 側方郭清の適応基準は,腫瘍下縁が腹膜反転部より肛門側にあり,かつ固有筋層を越えて浸潤する症例である。
- 第 2Houston 弁(腹膜反転部)より肛門側にある cM 癌,cSM 癌(軽度浸潤)が対象となる。
- 直腸局所切除のアプローチ法は経肛門的切除,経括約筋的切除,傍仙骨的切除に分類され,経肛門的切除には,直視化に腫瘍を切除する従来法と経肛門的内視鏡下切除術(TEM:transanal endoscopic microsurgery)がある。
- TEM では,従来法より口側の病変も切除することが可能である。
- 直腸癌手術に関連した自律神経系には,腰内臓神経,上下腹神経叢,下腹神経,骨盤内臓神経,骨盤神経叢がある。
- 癌の進行度,肉眼的な神経浸潤の有無等を考慮して,根治性を損なわない範囲で,排尿機能,性機能温存のため自律神経の温存に努める。
腹腔鏡下手術
- 経腹的手術治療には,開腹手術と腹腔鏡下手術がある。
- 腹腔鏡下手術は,癌の部位や進行度などの腫瘍側要因および肥満,開腹歴などの患者側要因だけでなく,術者の経験,技量を考慮して適応を決定する。
(CQ−3)
CQ1:内視鏡的摘除後の追加治療の適応基準
CQ2:最大径2cm 以上の cM 癌・cSM 癌の内視鏡的摘除
CQ3:大腸癌に対する腹腔鏡下手術
2 Stage IV大腸癌の治療方針
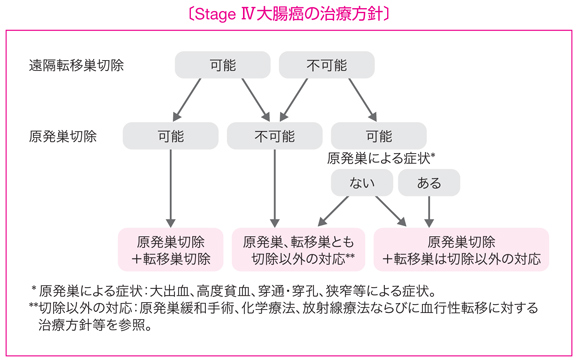
- Stage IV大腸癌では以下のいずれかの同時性遠隔転移を伴う。肝転移,肺転移,腹膜播種,脳転移,遠隔リンパ節転移,その他の転移(骨,副腎,脾など)。
- 遠隔転移巣ならびに原発巣がともに切除可能な場合には,原発巣の根治切除を行うとともに遠隔転移巣の切除を考慮する。
- 遠隔転移巣が切除可能であるが原発巣の切除が不可能な場合は,原則として原発巣および遠隔転移巣の切除は行わず,他の治療法を選択する。
- 遠隔転移巣の切除は不可能であるが原発巣切除が可能な場合は,原発巣の臨床症状や原発巣が有する予後への影響を考慮して,原発巣切除の適応を決める。
(CQ−4)
CQ4:切除不能な遠隔転移例における原発巣切除
CQ5:腹膜播種(癌性腹膜炎)の切除
3 再発大腸癌の治療方針
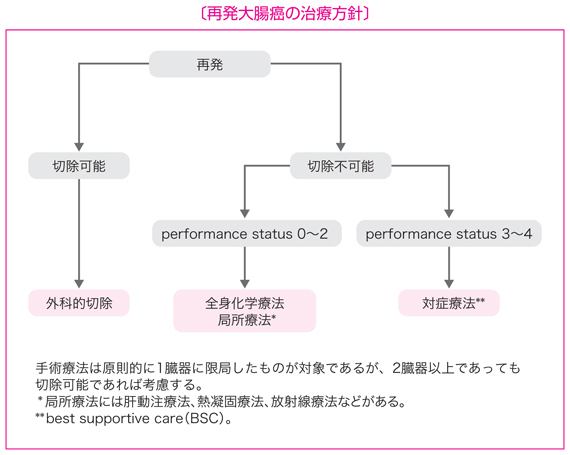
- 再発大腸癌の治療目的は,予後向上と QOL の改善である。
- 治療法には,手術療法,全身化学療法,動注化学療法,熱凝固療法,放射線療法などがある。
- 期待される予後,合併症,治療後の QOL などのさまざまな因子を考慮し,患者への十分なインフォームド・コンセントのもとに治療法を選択する。
- 再発臓器が 1 臓器の場合,手術にて再発巣の完全切除が可能であれば積極的に切除を考慮する。
- 再発臓器が 2 臓器以上の場合,それぞれが切除可能であれば切除を考慮してもよいが,治療効果については統一見解は得られていない。
- 肝あるいは肺転移に対して不顕性転移を除外するために一定の観察期間を置いてから切除を行うという見解がある。
- 血行性転移に対する治療法(血行性転移の治療方針)。
- 直腸癌局所再発には吻合部再発と骨盤内再発がある。
(1)切除可能であれば切除を考慮する。
(2)切除不能であれば放射線療法と全身化学療法の単独または併用を考慮する。
4 血行性転移の治療方針
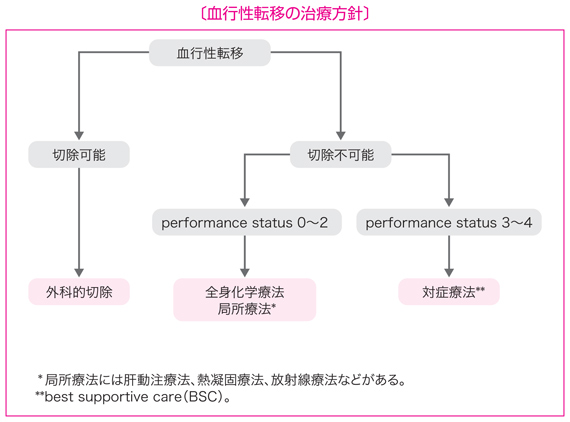
1)肝転移の治療方針
- 肝転移の治療は,肝切除,全身化学療法,肝動注療法および熱凝固療法に大別できる。
- 根治切除可能な肝転移には肝切除が推奨される。
- 肝切除術には系統的切除と部分(非系統的)切除がある。
肝切除の適応基準
(1)耐術可能。
(2)原発巣が制御されているか,制御可能。
(3)肝転移巣を遺残なく切除可能。
(4)肝外転移がないか,制御可能。
(5)十分な残肝機能。
- 切除不能な肝転移で全身状態が一定以上に保たれる場合(PS 0〜PS 2)は,全身化学療法と肝動注療法の単独または併用を考慮する。
- 熱凝固療法にはマイクロ波凝固療法(MCT:microwave coagulation therapy)とラジオ波焼灼療法(RFA:radiofrequency ablation)がある。
- 全身状態が不良な場合(PS≧3)は適切な対症療法(BSC:best supportive care)を行う。
2)肺転移の治療方針
- 肺転移の治療には,肺切除と化学療法がある。
- 肺転移巣の切除が可能であれば肺切除を考慮する。
- 肺切除には系統的切除と部分(非系統的)切除がある。
肺切除の適応基準
(1)耐術可能。
(2)原発巣が制御されているか,制御可能。
(3)肺転移巣を遺残なく切除可能。
(4)肺外転移がないか,制御可能。
(5)十分な残肺機能。
- 切除不能肺転移で全身状態が一定以上に保たれる場合は,全身化学療法を考慮する。
- 耐術不能な場合でも,原発巣と肺外転移が制御されているか,制御可能で,肺転移個数が 3~4 個以内であれば定位放射線治療も考慮する。
- 全身状態が不良な場合は適切な BSC を行う。
3)脳転移の治療方針
- 脳転移は全身疾患としての一分症として発見されることが少なくないが,治療効果が期待される病変に対しては,手術療法あるいは放射線療法を考慮する。
- 全身状態,他の転移巣の状況を考慮し,転移巣の大きさ,部位,病巣数を評価して最適な治療法を選択する。
- 切除不能例には放射線療法を考慮する。
脳切除の適応基準
(1)数カ月以上の生命予後。
(2)切除により重大な神経症状をきたさない。
(3)他臓器の転移がないか,制御可能。
- 脳神経症状や頭蓋内圧亢進症状などの症状緩和と局所制御による延命を目的とする。
- 多発性脳転移例や外科切除の対象とならない孤立性脳転移例では全脳照射を考慮する。
- 脳転移個数が 3〜4 個以内で 3 cm 以下であれば,定位放射線照射を考慮する。
4)その他の血行性転移の治療方針
- 副腎,皮膚,脾などの血行性転移に対しても,切除可能な場合は切除を考慮する。しかし,これらの転移は他の臓器の転移を伴うことが多く,化学療法あるいは放射線療法が適応されることが多い。
CQ7:肝・肺転移を有する症例に対する切除
CQ8:肝転移根治切除後の補助化学療法
CQ9:切除可能肝転移に対する術前化学療法
CQ10:切除不能肝転移に対する化学療法
5 化学療法
- 化学療法には,術後再発抑制を目的とした補助化学療法と切除不能な進行再発大腸癌を対象とした全身化学療法がある。
- 日本の保険診療として,大腸癌に対する適応が認められている主な抗がん剤には以下のものがある。
経口薬:5−FU,tegafur,tegafur/uracil(UFT),doxifluridine(5′−DFUR),carmofur(HCFU),S−1,UFT+LV 錠,capecitabine など
注射薬:5−FU,mitomycin C,irinotecan(CPT−11),5−FU+l −leucovorin(LV),oxaliplatin(L−OHP),bevacizumab,cetuximab など
1)補助化学療法
- 術後補助化学療法は,R0 切除が行われた症例に対して,再発を抑制し予後を改善する目的で,術後に実施される全身化学療法である。
適応の原則
(1)R0 切除が行われた Stage III大腸癌(結腸癌・直腸癌)。
(2)主要臓器機能が保たれている。
- 骨髄:白血球>4,000/mm3,血小板>100,000/mm3
- 肝機能:総ビリルビン<2.0 mg/dL,AST/ALT<100 IU/L
- 腎機能:血清クレアチニン:施設基準値上限以下
(3)performance status(PS)が 0~1 である。(CQ−11)
(4)術後合併症から回復している。
(5)適切なインフォームド・コンセントに基づき患者から文書による同意が得られている。
(6)重篤な合併症(特に,腸閉塞,下痢,発熱)がない。
- 再発リスクが高い Stage II大腸癌には,適切なインフォームド・コンセントのもとに,補助化学療法の適応を考慮する。(CQ−12)
推奨される療法注
- 5−FU/LV 療法
- UFT/LV 療法
- capecitabine 療法
- 投与期間 6 カ月を原則とする 注 日本における保険適応収載順。
2)切除不能進行再発大腸癌に対する化学療法
- 化学療法を実施しない場合,切除不能と判断された進行再発大腸癌の生存期間中央値(MST:median survival time)は約 8 カ月と報告されている。最近の化学療法の進歩によって MST は約 2 年まで延長してきたが,現状では治癒を望むことは難しい。
- 化学療法の目標は腫瘍増大を遅延させて延命と症状コントロールを行うことである。
- PS 0〜PS 2 の症例を対象とした第III相試験において,化学療法群は抗がん剤を用いない対症療法(BSC:best supportive care)群よりも有意に生存期間が延長することが示されている。
- 切除不能進行再発大腸癌に対する化学療法が奏効して切除可能となることがある。
適応の原則
(1)臨床診断または病理組織診断が確認されている。
(2)転移・再発巣が画像にて確認可能である。
(3)performance status(PS)が 0〜2 である。
(4)主要臓器機能が保たれている。
1.骨髄:白血球>3,500/mm3,血小板>100,000/mm3
2.肝機能:総ビリルビン<2.0 mg/dL,AST/ALT<100 IU/L
3.腎機能:血清クレアチニン:施設基準値上限以下
(5)適切なインフォームド・コンセントに基づき患者から文書による同意が得られている。
(6)重篤な合併症(特に,腸閉塞,下痢,発熱)を有さない。
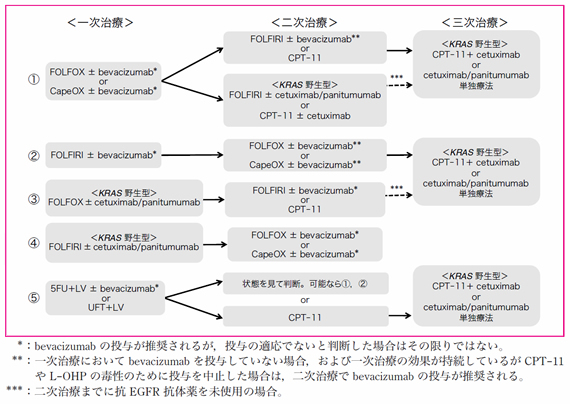
一次治療
- 国内外の第III相試験により生存期間の延長が検証されており,かつ保険診療として使用可能な一次治療としてのレジメンは以下の通りである。
(1)FOLFOX 療法注 1 ± bevacizumab
(2)FOLFIRI 療法注 2 ± bevacizumab
(3)5−FU/LV 療法 注 3 ±bevacizumab
(4)UFT/LV 療法
二次治療以降
- 二次治療以降の化学療法として以下のレジメンを考慮する。(CQ−15)
(1)L−OHP を含むレジメンに抵抗性となった場合
FOLFIRI 療法±bevacizumab
FOLFIRI 療法(または CPT−11 単独)±cetuximab
(2)CPT−11 を含むレジメンに抵抗性となった場合
FOLFOX 療法±bevacizumabまたは CPT−11+cetuximab
(3)5−FU,L−OHP,CPT−11 を含むレジメンに抵抗性となった場合
CPT−11+cetuximab,cetuximab 単独療法
注)cetuximab の保険適応が承認されているのは EGFR 陽性の大腸癌である。(CQ−16)
注 1 FOLFOX 療法
infusional 5−FU/LV+L−OHP。
注 2 FOLFIRI 療法
infusional 5−FU/LV+CPT−11。
注 3 5−FU/LV 療法
5−FU/LV 療法には,RPMI 法(l−LV 250 mg/m2,2 時間点滴;5−FU 600 mg/m2,l−LV 開始 1 時間後に 3 分以内に緩徐に静注:毎週 1 回投与,6 週連続 2 週休薬,8 週毎繰り返す),de Gramont 法(l−LV 100 mg/m2,2 時間点滴;5−FU 400 mg/m2,l−LV 終了直後に静注;5−FU 600 mg/m2を 22 時間かけて点滴静注:これを 2 日間連続して行い,2 週毎に繰り返す),sLV5FU2 法(l−LV 200 mg/m2,2 時間点滴;5−FU 400 mg/m2,l−LV 終了直後に静注;5−FU 2,400〜3,000 mg/m2を 46 時間かけて点滴静注:2 週毎に繰り返す),AIO 法(l−LV 250 mg/m2,2 時間点滴;5−FU 2,600 mg/m2を 24 時間かけて点滴静注:6 週連続 2 週休薬,8 週毎繰り返す)がある。なお,国内で承認されているl 型ロイコボリンの投与量は欧米で使用されている dl 型ロイコボリンの半量で等量となる。
CQ11:術後補助化学療法と年齢
CQ12:Stage II大腸癌に対する術後補助化学療法
CQ13:術後補助化学療法の治療期間
CQ14:術後補助化学療法における oxaliplatin(L−OHP)
CQ15:二次治療における分子標的治療薬
CQ16:KRAS 遺伝子変異と cetuximab
6 放射線療法
- 放射線療法には,直腸癌の術後の再発抑制や術前の腫瘍量減量,肛門温存を目的とした補助放射線療法と切除不能進行再発大腸癌の症状緩和や延命を目的とした緩和的放射線療法がある。
1)補助放射線療法
- 補助放射線療法には,術前照射,術中照射,術後照射がある。
- 補助放射線療法の目的は直腸癌の局所制御率の向上,生存率の改善であり,術前照射ではさらに肛門括約筋温存率と切除率の向上も目的とする。
- 術前照射は「深達度 cSS/cA 以深または cN 陽性」,術後照射は「深達度 pSS/pA 以深または pN 陽性」,術中照射は外科剥離面陽性(RM+)または剥離面近傍への癌浸潤(RM±)を対象とする。
- 照射方法により外部照射と術中照射に分けられる。
2)緩和的放射線療法
a.骨盤内病変(CQ−18)- 骨盤内腫瘍による疼痛,出血,便通障害などの症状緩和を目的とする。
- 標的体積には症状の原因となっている腫瘍を含める。
- 1 回 1.8~2.0 Gy,総線量 45~50 Gy 照射する。
- 全身状態,症状の程度によっては 1 回線量を多くして短期間で照射を終了することもある。
(1)骨転移
- 疼痛の軽減,病的骨折の予防,脊髄麻痺の予防と治療を目的とする。
- 標的体積には症状の原因となっている腫瘍を含める。
- 局所照射では 30 Gy/10 回,20 Gy/5 回などの分割照射が広く行われている。
- 血行性転移の項を参照。
- 全脳照射では 30 Gy/10 回が標準的であり,長期予後が期待される場合には 37.5 Gy/15 回ないしは 40 Gy/20 回などを検討する。
- 定位手術的照射では辺縁線量 16〜25 Gy を 1 回で照射する。
CQ17:直腸癌に対する術前化学放射線療法の意義
CQ18:切除不能な局所進行・局所再発直腸癌に対する化学放射線療法
7 緩和医療
- 緩和医療とは,がんにかかわる精神的,身体的なさまざまな症状に対する緩和治療の総称である。
- 緩和医療は,がんの診断がついた時点から終末期までを包括する医療であり,病期や症状により,実施すべき内容が異なる。
- がん治療は症状緩和が図られた状態で行うことが原則であり,外科治療や化学療法の当初から緩和医療を導入すべきである。
- 大腸癌終末期における QOL 向上のための緩和医療には以下のものが含まれる。
(1)疼痛緩和
(2)外科治療
(3)化学療法
(4)放射線療法
(5)精神症状に対するカウンセリング
8 大腸癌手術後のサーベイランス
1)大腸癌根治度 A 切除後の再発に関するサーベイランス
- Stage 0(pM 癌)は,切除断端に癌が陰性であれば,サーベイランスは不要である。ただし,切除断端の評価が困難な場合は,半年~1 年後に大腸内視鏡検査を行い,局所再発の有無を調べる。
- サーベイランス期間は術後 5 年間を目安とし,術後 3 年以内はサーベイランス間隔を短めに設定する。
- 直腸癌では肺転移再発と局所再発の頻度が高いことに留意する。
- 吻合部再発のサーベイランスは術後 3 年までを目安とする。
- 再発の好発部位,発生頻度,治療効果等をレトロスペクティブに検討して導き出された Stage I~Stage III大腸癌の治癒切除後のサーベイランススケジュールの一例を示す。
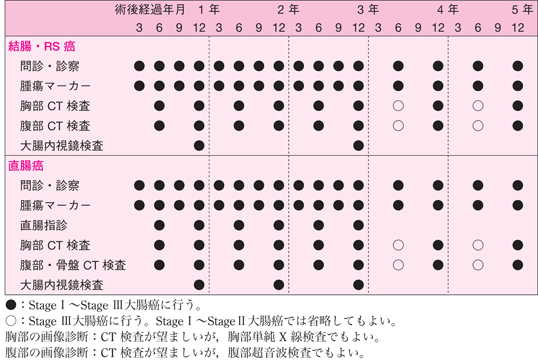
2)大腸癌根治度 B 切除後および再発巣切除後のサーベイランス
- Stage IIIのサーベイランスに準ずるが,転移・再発の切除臓器に再発・再々発が多いことに留意する。
3)異時性多重がんのサーベイランス
- 異時性多発癌のサーベイランスを目的として大腸内視鏡検査を行う。









