
各論Ⅱ
Ⅱ.CD関連消化管腫瘍
1 疫 学
● ポイント
- CDにおける大腸癌および小腸癌の発生リスクは一般集団と比べて有意に高い。
- CD関連大腸癌の発症リスクは大腸病変を伴うCDで有意に上昇し,UCとほぼ同等である。
- CDでは小腸,結腸,直腸,肛門部で悪性腫瘍の発生リスクが有意に上昇し,本邦では特に直腸肛門部が多い。
- CD関連消化管腫瘍のリスク因子としては,罹病期間,若年発症,大腸癌の家族歴,広範囲の大腸病変,狭窄などが挙げられる。
● 解説
- 発生頻度
UCと同様,CDにおいても一般集団と比較して消化管腫瘍の発生リスクの増加が報告されている。CD関連消化管腫瘍に関する初めてのメタアナリシスであるJessらの報告では,CDにおける大腸癌(colorectal cancer:CRC)および小腸癌(small bowel cancer)の発生リスクは一般集団と比べて有意に高い(大腸癌:標準化罹患比(standard incidence ratio:SIR)1.9,95%信頼区間1.4-2.5,小腸癌:SIR 27.1,95%信頼区間14.9-49.2)1)。2004年までに報告された12件の集団ベースのコホート研究をまとめたCanavanらのメタアナリシスでも同様であり(大腸癌:SIR 2.5,95%信頼区間1.3-4.7,小腸癌:SIR 31.2,95%信頼区間15.9-60.9),CD患者における大腸癌累積発生率は10年で2.9%,20年で5.6%,30年で8.3%と報告されている2)。CDにおける大腸癌の発症リスクは大腸病変を伴うCD患者で有意に上昇するが,小腸病変のみのCD(小腸型CD)では一般集団と同等である2,3)。また大腸病変を伴うCDにおける大腸癌の発生リスクはUCとほぼ同じである2,3)。さらに2005年から2021年までに報告された24本のメタアナリシスを包括的に再解析したumbrella reviewでもCD患者における消化管腫瘍全体の発生リスクは一般集団と比較して有意に高く(相対的リスク比RR 1.56,95%信頼区間1.10-2.23),部位別の検討では小腸(RR 11.9,95%信頼区間8.07-17.7)結腸(RR 2.30,95%信頼区間1.73-3.06),直腸(RR 1.85,95%信頼区間1.58-2.17),肛門(RR 4.52,95%信頼区間1.19-17.1)で特に高い(図22)4)。しかし,その他の部位(上部消化管,咽頭,食道,胃)については有意な上昇は認められない4)。いずれの報告でもCDにおける小腸癌の相対危険度はきわめて高いが全消化管癌に占める小腸癌の割合は約2%と低く5),その絶対的リスクは小さいと考えられる2,6,7)。またIBD患者における大腸癌の発生リスクの経時的傾向については,ここ数十年でUCにおける大腸癌の発生リスクは低下傾向にあるが,CDでは変化していないことが報告されている3)。 - 臨床的特徴
CD関連大腸癌の診断時年齢は一般人口における大腸癌の診断時年齢と比べて低く(平均;51.5歳vs 71.0歳),癌診断までのCD平均罹病期間は18.3年と報告されている6)。CD関連消化管腫瘍の好発部位については地域差あるいは人種差があり,欧米では右側大腸に多く,本邦では痔瘻癌を含む直腸肛門管癌が多い8,9)。しかしUchinoらのメタアナリシスでは,本邦を含むアジアからの報告ではCD関連大腸癌は左側大腸に多いが(84.1%),欧米からの報告でもCD関連大腸癌の63.1%は左側大腸に発生している(右側大腸36.9%)10)。このように,散発性大腸癌やUC関連大腸癌と比べるとCD関連大腸癌の合併頻度は右側大腸にやや高いが,欧米からの報告でもCD関連大腸癌は主に左側大腸に発生しており,その解釈には注意が必要である。実際,欧米のガイドラインでも直腸肛門部を含めた発癌リスクへの注意喚起がなされている7)。またCD関連小腸癌のほとんどは炎症を有する小腸罹患部(主に回腸)から発生し,十二指腸を含め小腸全域から発生する散発性小腸癌とは異なる特徴を有する5,7)。 - リスク因子
CD関連消化管腫瘍のリスク因子としては,罹病期間,発症時年齢(若年発症),大腸癌の家族歴,広範囲の大腸病変,狭窄などが挙げられる。UCと同様,CDでも罹患年数とともに大腸癌の累積発生率が上昇する2)。診断時年齢もIBD関連大腸癌の発生リスクに大きく影響する。小児発症CDではUC同様,大腸癌の発症リスクが上昇する(SIR 6.3,95%信頼区間3.93-10.2)11)。また集団ベースのコホート研究のみを対象としたメタアナリシスでは若年発症(30歳未満)のCD患者は非若年発症CD(30歳以上)と比較してCD関連大腸癌の発生リスクが有意に上昇することが報告されている(30歳未満:SIR 8.2,95%信頼区間1.8-14.6,30歳以上:SIR 1.8,95%信頼区間0.9-2.7)3)。CD関連大腸癌と広範な大腸病変の関連性については個別の報告のみに限定されるが複数の報告がある12,13)。大腸癌の家族歴を有するCDでは家族歴がない場合と比べて,大腸癌の発生リスクが3.7倍(95%信頼区間1.4-9.4)上昇する14)。大腸狭窄を有するCD患者における大腸癌の発癌リスクは上昇することが報告されているが(オッズ比8.03,95%信頼区間3.50-18.45),小腸狭窄病変の発癌リスクについては今後の検討が待たれる15)。
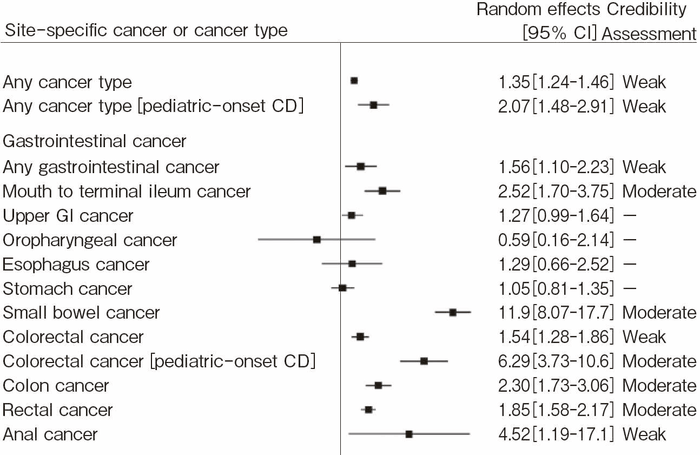
図22 CD関連消化管腫瘍の全体および部位別発癌リスク
(文献4)より引用し,一部を抜粋)
文献
- Jess T, Gamborg M, Matzen P, et al.:Increased risk of intestinal cancer in Crohn’s disease:a meta-analysis of population-based cohort studies. Am J Gastroenterol 2005;100:2724-2729
- Canavan C, Abrams KR, Mayberry J:Meta-analysis:colorectal and small bowel cancer risk in patients with Crohn’s disease. Aliment Pharmacol Ther 2006;23:1097-1104
- Lutgens MW, van Oijen MG, van der Heijden GJ, et al.:Declining risk of colorectal cancer in inflammatory bowel disease:an updated meta-analysis of population-based cohort studies. Inflamm Bowel Dis 2013;19:789-799
- Piovani D, Hassan C, Repici A, et al.:Risk of Cancer in Inflammatory Bowel Diseases:Umbrella Review and Reanalysis of Meta-analyses. Gastroenterology 2022;163:671-684
- Aparicio T, Zaanan A, Svrcek M, et al.:Small bowel adenocarcinoma:epidemiology, risk factors, diagnosis and treatment. Dig Liver Dis 2014;46:97-104
- Laukoetter MG, Mennigen R, Hannig CM, et al.:Intestinal cancer risk in Crohn’s disease:a meta-analysis. J Gastrointest Surg 2011;15:576-583
- Annese V, Beaugerie L, Egan L, et al.:European Evidence-based Consensus:Inflammatory Bowel Disease and Malignancies. J Crohns Colitis 2015;9:945-965
- Choi PM, Zelig MP:Similarity of colorectal cancer in Crohn’s disease and ulcerative colitis:implications for carcinogenesis and prevention. Gut 1994;35:950-954
- Delaunoit T, Limburg PJ, Goldberg RM, et al.:Colorectal cancer prognosis among patients with inflammatory bowel disease. Clin Gastroenterol Hepatol 2006;4:335-342
- Uchino M, Ikeuchi H, Hata K, et al.:Intestinal cancer in patients with Crohn’s disease:A systematic review and meta-analysis. J Gastroenterol Hepatol 2021;36:329-336
- Aardoom MA, Joosse ME, de Vries ACH, et al.:Malignancy and Mortality in Pediatric-onset Inflammatory Bowel Disease:A Systematic Review. Inflamm Bowel Dis 2018;24:732-741
- Ekbom A, Helmick C, Zack M, et al.:Increased risk of large-bowel cancer in Crohn’s disease with colonic involvement. Lancet 1990;336:357-359
- Gillen CD, Walmsley RS, Prior P, et al.:Ulcerative colitis and Crohn’s disease:a comparison of the colorectal cancer risk in extensive colitis. Gut 1994;35:1590-1592
- Askling J, Dickman PW, Karlén P, et al.:Family history as a risk factor for colorectal cancer in inflammatory bowel disease. Gastroenterology 2001;120:1356-1362
- Wijnands AM, de Jong ME, Lutgens MWMD, et al.:Prognostic Factors for Advanced Colorectal Neoplasia in Inflammatory Bowel Disease:Systematic Review and Meta-analysis. Gastroenterology 2021;160:1584-1598
2 サーベイランス
1)直腸肛門管癌サーベイランス
● ポイント
- CD罹患年数10年以上で,おもに肛門病変を有する症例を対象に,直腸肛門管癌のサーベイランスを1年に1回程度行う。
- 肛門痛がある症例では,麻酔下に内視鏡を用いて直腸の観察,生検を行う。さらにMRI検査で肛門周囲の状況を確認する必要がある。
- 全身麻酔下に定期的,継続的にシートンドレナージ,肛門拡張術を行っている場合は,処置時に生検も行う。
● 解説
麻酔下肛門部観察(examination under anesthesia:EUA)はCDの肛門部診察において有用性は報告されており1),関連した直腸肛門管癌の診断や鑑別にも,同様に有用性が考えられる。肛門痛を伴う症例では,全身麻酔下による内視鏡検査を併用し,直腸までの観察を行う。
(1)体位,生検部位(図23)
全身麻酔下に,砕石位もしくはJack-knife位で行う。生検を行う部位は,歯状線付近を全周性に3カ所程度行う。
(2)手 順(図24)
視診,触診,直腸診で診察を行う(図24a)。診察でターゲットとなる部を認めた場合は,その部位から生検し,ない場合は肛門鏡で視野を確保し,歯状線近傍から全周性に3カ所ほど行う(図24b)。痔瘻を伴う場合は,非活動性,瘢痕化している場合でも,瘻管内から生検を行う(図24c)。
(3)狭窄病変がある場合(図25)
小指,示指で愛護的に拡張した後(図25a),ブジーを使って,内視鏡検査が可能な程度まで拡張を行う(図25b)。内視鏡により直腸の観察,生検を併せて行う(図25c,d)。
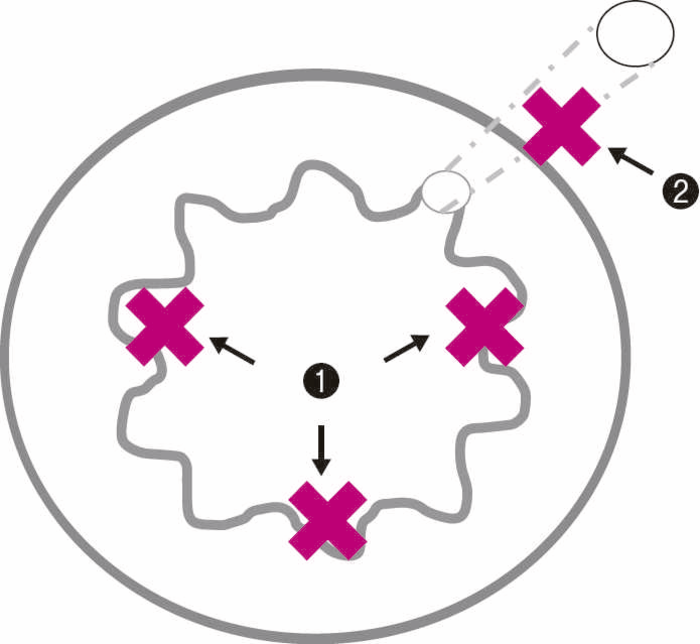
図23 肛門管粘膜,瘻管内からの生検
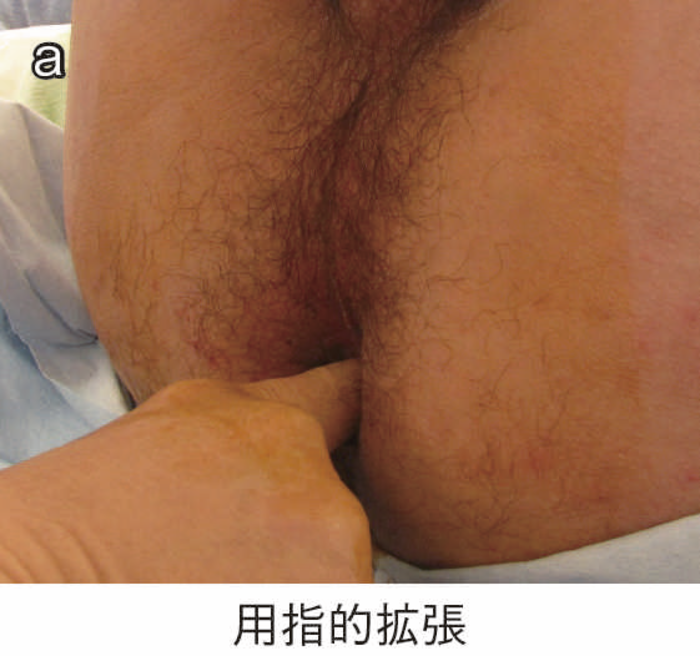
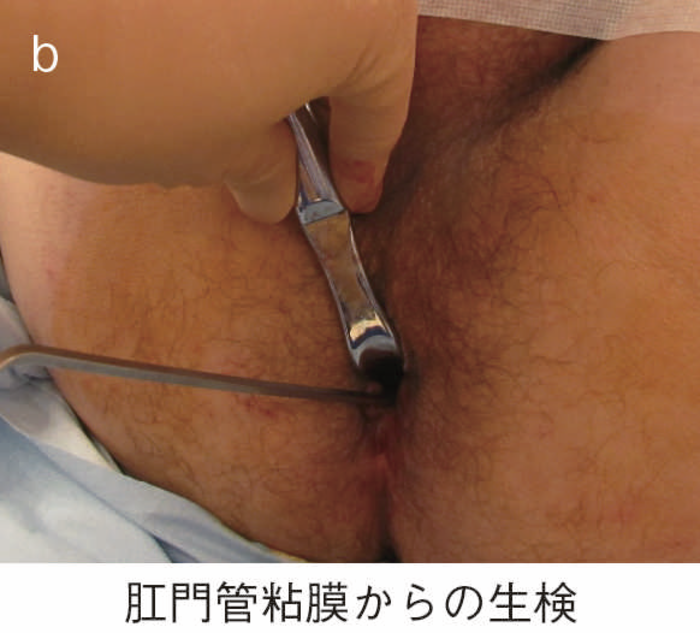
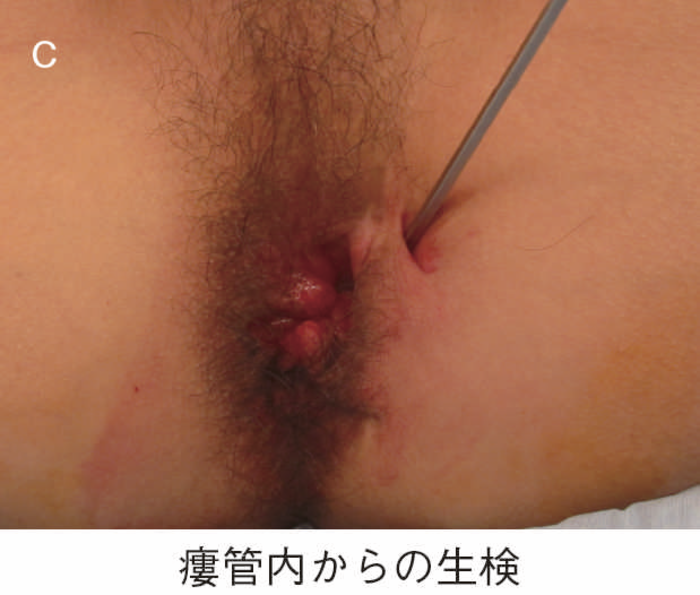
図24 EUAの手順
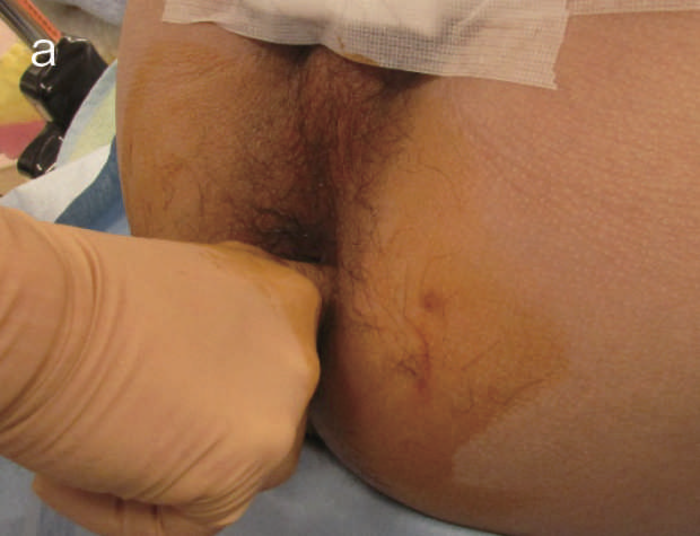
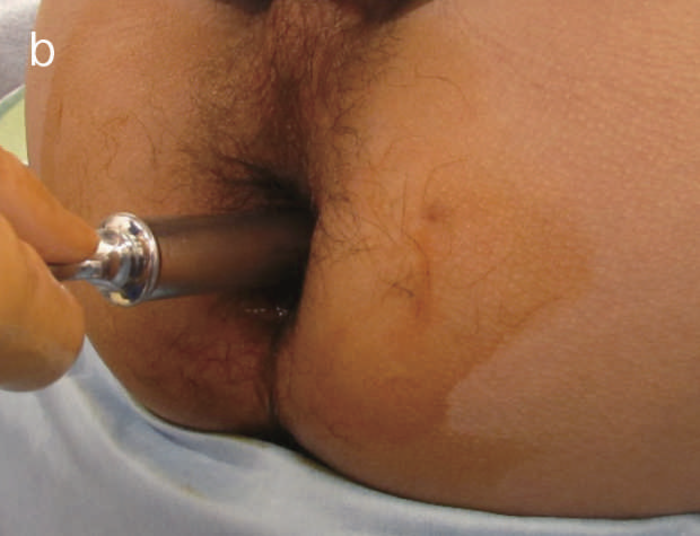
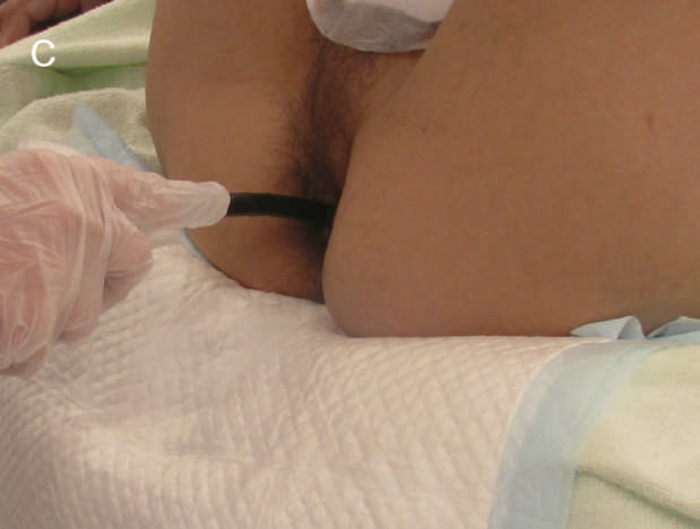
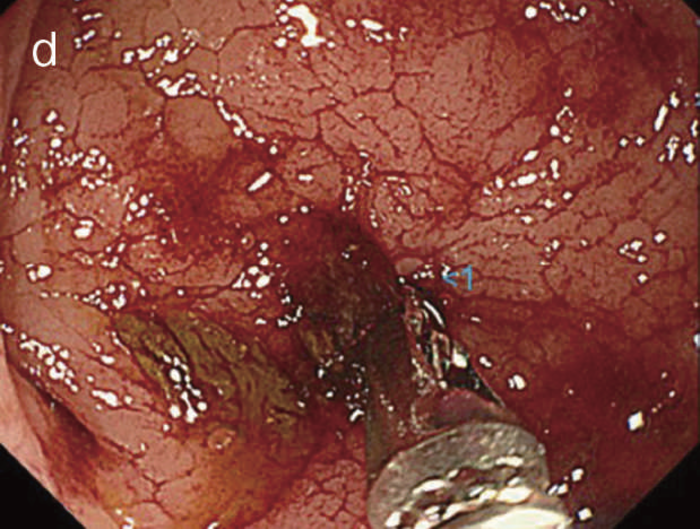
図25 狭窄症例のEUA
サイドメモ
Hiranoらの報告で,10年以上のCD歴を有する患者を対象とした103例のEUAの結果,癌検出率は4.9%であった2)。痔瘻病変,肛門狭窄などのリスクを有している症例は10年未満であっても生検を行う。さらに難治性痔瘻,高度の肛門狭窄を伴うような症例では1年に複数回行うことを考慮する必要がある。
文献
- Marzo M, Felice C, Pugliese D, et al.:Management of perianal fistulas in Crohn’s disease:an up-to-date review. World J Gastroenterol 2015;21:1394-1403
- Hirano Y, Futami K, Higashi D, et al.:Anorectal cancer surveillance in Crohn’s disease. J Anus Rectum Colon 2018;2:145-154
2)内視鏡,その他
● ポイント
- CD長期経過例で,主に直腸肛門管領域を対象としてサーベイランスを行う。
- 外科的切除で生命予後が期待できる病期で発見することがサーベイランスの目標となる。
- 肛門部の疼痛悪化や強い肛門部痛,肛門部排出粘液の増加を認めた場合は,サーベイランスの追加を検討する。また空置直腸はハイリスクであり,サーベイランスの対象に加える。
- サーベイランスは一つの方法に固執せず,検査や症例の特徴を考慮して,複合的かつ定期的に行うことが必要である。
● 解説
長期の罹病期間を有するCD症例で,サーベイランスの対象となる臓器は頻度を考えると直腸肛門管領域となる1,2)。他の消化管,特に小腸はバルーン小腸内視鏡を用いないと内視鏡によるサーベイランスが困難なこともあり,CD関連消化管腫瘍術後例などを除き,臨床でのサーベイランスは根拠も乏しく,実施も困難である3)。UC同様,8年以上の罹病期間が目安となるが,直腸肛門部の炎症が慢性持続となっている例や発症時期が不明確な例では,より短い罹病期間でも注意を要する。また高度の直腸肛門部病変により手術で空置された直腸はハイリスクであり,サーベイランスの必要性が高い4)。
注意すべき症状として肛門部の疼痛悪化や強い肛門部痛,肛門部排出粘液の増加などがあり,認めた場合にはサーベイランスの追加を検討する5)。
CD関連腫瘍,特に直腸肛門管領域の腫瘍では内視鏡切除の適応を検討するような病変はほとんど存在せず,外科切除(直腸肛門部の腫瘍では腹会陰式直腸切断術)で生命予後が期待できる病期で発見することがサーベイランスの目標となる4)。
サーベイランスの方法には直腸診などの触診,外科的な局所麻酔ないし腰椎麻酔を用いた生検や細胞診の他,腫瘍マーカー測定,超音波検査,CT検査,MRI検査,positron emission tomography(PET)検査,内視鏡検査などがある6)。各検査法の特徴を表6に示す。直腸肛門管領域以外の消化管のサーベイランスは,生検が可能な内視鏡検査が主体となるが,直腸肛門管領域においては一つの方法に固執せず,症例の特徴や検査手技の実行可能性を考慮して,複合的かつ定期的に行うことが必要である4)。
特に内視鏡検査によるサーベイランスでは,狭窄が悪化すると内視鏡の挿入が困難となる。内視鏡が挿入困難とならないよう肛門狭窄等をコントロールしておくことと,Rbの反転観察の励行,使用するスコープの工夫などが大切である。Treat-to-target診療で治療目標の評価を内視鏡的に行う際に,サーベイランスを兼ねて内視鏡検査を施行することが理想である7)。
サイドメモ
肛門部領域では扁平上皮癌を合併する可能性があり,注意を要する8)。
文献
- 日本消化器病学会編:炎症性腸疾患(IBD)診療ガイドライン2020(改訂第2版),南江堂,東京,2020.
- Higashi D, Katsuno H, Kimura H, et al.:Current State of and Problems Related to Cancer of the Intestinal Tract Associated with Crohn’s Disease in Japan. Anticancer Res 2016;36:3761-3766
- Sogawa M, Watanabe K, Egashira Y, et al.:Precise endoscopic and pathologic features in a Crohn’s disease case with two fistula-associated small bowel adenocarcinomas complicated by an anal canal adenocarcinoma. Intern Med 2013;52:445-449
- 渡辺憲治,樋田信幸,中村志郎:炎症性腸疾患関連腫瘍サーベイランスの精度向上に向けて.日消誌2019;116:878-890
- クローン病肛門部病変に対する治療指針(2022年1月改訂).厚生労働科学研究費 難治性疾患政策研究事業「難治性炎症性腸管障害に関する調査研究」(久松班)令和3年度分担研究報告書 潰瘍性大腸炎・クローン病 診断基準・治療指針 令和3年度改訂版(令和4年3月31日)
- Hirano Y, Futami K, Higashi D, et al.:Anorectal cancer surveillance in Crohn’s disease. J Anus Rectum Colon 2018;2:145-154
- Watanabe K:Clinical management for small bowel of Crohn’s disease in the treat-to-target era:now is the time to optimize treatment based on the dominant lesion. Intest Res 2020;18:347-354
- Palmieri C, Müller G, Kroesen AJ, et al.:Perianal Fistula-Associated Carcinoma in Crohn’s Disease:A Multicentre Retrospective Case Control Study. J Crohns Colitis 2021;15:1686-1693
3 診 断
1)内視鏡診断,その他画像診断
● ポイント
- CD関連消化管腫瘍の確定診断には病理診断が必要なため,生検可能な内視鏡検査以外の画像診断では原則として確定診断には至らない。
- 各種画像診断には長所短所があり,症例の病状や特徴,病変の存在部位などに応じて使い分けることと,一つの方法に固執しないことが大切である。
- 内視鏡が挿入,到達可能となるよう,CD病変の活動性や狭窄をコントロールする。腫瘍性病変を疑う所見を見出し,狙撃生検を施行することになるが,CD関連消化管腫瘍に関する内視鏡診断は未確立である。
- CD関連消化管腫瘍の好発部位である直腸肛門管領域の内視鏡観察は慎重に行う。直腸下部,痔瘻一次口付近の内視鏡反転観察も重要で,施行可能となるよう,鎮静や内視鏡機器の選択に配慮を要する。
- CD関連消化管腫瘍を疑って内視鏡検査を施行し,生検標本の病理診断で確定診断が得られない場合には,再検査を検討する。
● 解説
-
内視鏡診断
CD関連消化管腫瘍に対する内視鏡診断には,存在診断,質的診断,深達度診断などがあるが,いずれも未確立であり,CD関連消化管腫瘍を疑う病変の生検で確定診断に導く存在診断が目標となる1)。CDの慢性炎症に関連した腫瘍性病変であるので,高い活動性の炎症に長期に罹患した部位が好発部位となるが,本邦においては痔瘻や肛門周囲膿瘍が発生する直腸肛門管領域が圧倒的に多く,肛門狭窄によって内視鏡が挿入困難とならないよう,ブジーや内科的治療によりコントロールすることが前提となる1,2)。
内視鏡検査による存在診断における課題は,CD関連消化管腫瘍を疑う所見の拾い上げになる。直腸肛門管領域に絨毛様の表面構造を有する病変を認めることが多い(図26)が,分化度の低い病変の拾い上げに有用な内視鏡所見はわかっていない1,3)。特に内科的治療で炎症の消退が困難な慢性に炎症が持続する領域の場合,炎症により腫瘍性病変を疑う所見の拾い上げがさらに困難となる。
質的診断には,範囲診断,CD非関連腫瘍との内視鏡的鑑別,病変の悪性度の診断などがある。UCの場合と異なり,内視鏡的に視認困難な平坦dysplasiaはCDでは報告されておらず,CD関連消化管腫瘍が内視鏡切除の適応となる場合も乏しいため,範囲診断が問題となることは少ないが,例えば痔瘻の瘻管内に存在する腫瘍の範囲診断は不可能である。
深達度診断も,炎症発癌病変の特徴として粘膜の表層よりも深部で異型度が高くなっている場合があることに加え,CDでは痔瘻など瘻孔が関与する病変が存在するため,困難と思われる。CD関連腫瘍を疑っても生検標本の病理診断で確定診断に至らない場合は,病変の表層は異型度が低くなっている可能性も考慮し,再検査を検討する。 -
その他画像診断
内視鏡以外の画像診断には,超音波検査,CT検査,MRI検査などがあるが,CD関連腫瘍に関する診断は,やはり未確立である4)。こうしたcross sectional imagingにおいては,CDの炎症による腫瘤や膿瘍との鑑別が課題となる5)。CD関連消化管癌では病変が房状を呈することがあるが(図27),早期の病変を診断することは困難である。臨床では,痔瘻や肛門周囲膿瘍の評価のためのcross sectional imagingによる検査でCD関連消化管癌の可能性がある所見を拾い上げられるかがポイントとなるが,確定診断後に画像診断所見を見直した際に,所見に気付くことも少なくない。また確定診断のためには,内視鏡検査による生検や外科的な生検か細胞診を行う必要がある。
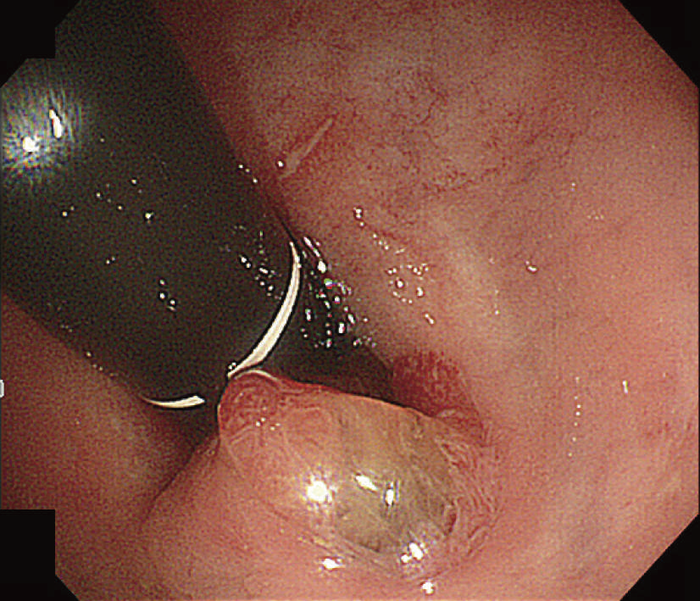
図26 痔瘻一次口から表出したクローン病関連腫瘍の直腸反転内視鏡観察像
粘液をともない,腫瘍性病変を強く疑う表面構造を有している。当初の生検病理診断は過形成性病変で,再検の後,直腸切断術を施行した。(文献1)から転載)
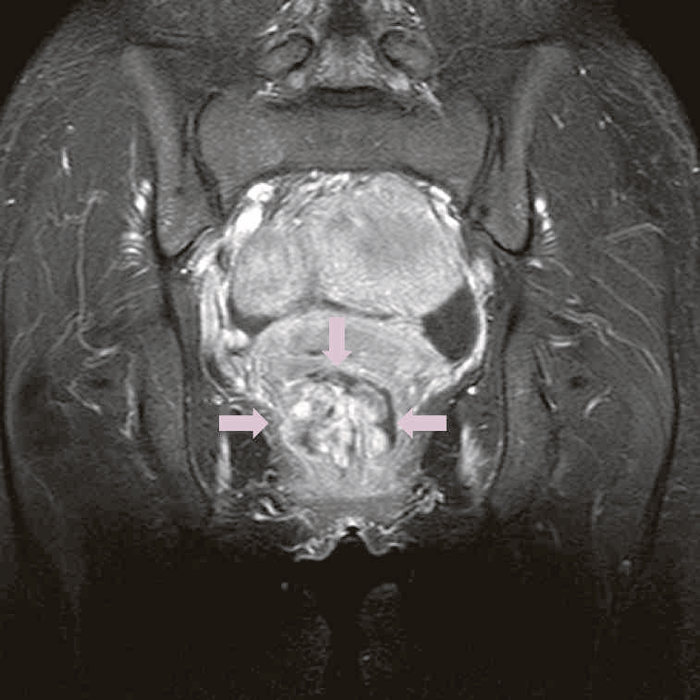
図27 CD直腸肛門部癌の骨盤造影MRI検査像
直腸内に増強効果を受ける分葉状の腫瘤を認める。
サイドメモ
CD関連腫瘍の早期診断が発展困難な一因は,経験豊富な病理医により十分に検討された早期の病変が乏しいことで,多くの病変は病期が進行した状態で診断されることが多いため,病変の初発部位や痔瘻(瘻孔)との関係の病理診断が困難な場合が多い1)。正確な病理診断に基づき,痔瘻に関連する腫瘍と非関連の腫瘍の比率を検討したり,dysplasiaの存在する比率を検討した報告もほとんどなく,早期診断の確立の大きな妨げとなっている。多施設共同研究による初期病変の検討が可能な症例の集積と,詳細な病理診断の検討が必要である。
文献
- 渡辺憲治,樋田信幸,中村志郎:炎症性腸疾患関連腫瘍サーベイランスの精度向上に向けて.日消誌2019;116:878-890
- Ballester MP, Mesonero F, Flórez-Diez P, et al.:Adherence to endoscopic surveillance for advanced lesions and colorectal cancer in inflammatory bowel disease:an AEG and GETECCU collaborative cohort study. Aliment Pharmacol Ther 2022;55:1402-1413
- Matsuno H, Mizushima T, Nezu R, et al.:Detection of Anorectal Cancer among Patients with Crohn’s Disease Undergoing Surveillance with Various Biopsy Methods. Digestion 2016;94:24-29
- 日本消化器病学会編:炎症性腸疾患(IBD)診療ガイドライン2020(改訂第2版),南江堂,東京,2020
- Furfaro F, Dal Buono A, Sicuso C, et al.:Carcinomas in inflammatory bowel disease:a narrative review on diagnostic imaging techniques. Chin Clin Oncol 2022;11:2
2)病理診断
● ポイント
- CD関連消化管癌には,大腸・肛門管癌(痔瘻癌を含む),小腸癌が含まれ,組織学的にはいずれも低分化腺癌,印環細胞癌,粘液癌の発生頻度が高い。
- 直腸・肛門管部に発生するCD関連進行癌の肉眼型では5型(分類不能型)が多い。わが国では小腸癌の発症頻度は高くはないが,その肉眼型は3型,4型が多くを占める。
- DysplasiaはUCだけではなく,CDにおいても認められるが,CD関連消化管癌におけるdysplasiaの併存率は報告によりばらつきがある。
- 痔瘻癌の生検検体では,大半が粘液成分で癌細胞が少数のことがしばしばあり,病理診断に苦慮することが少なくない。粘液癌を見逃さないためにも,痔瘻部の生検組織内に多量の粘液が認められた際にはより慎重な精査が望まれる。
● 解説
- 肉眼的特徴
CD関連消化管癌には,大腸癌・肛門管癌(痔瘻癌を含む),小腸癌が含まれる。CDによる非腫瘍性の狭窄,痔瘻や炎症性変化が加わり,非典型的な肉眼像を呈することが多い。CD関連大腸癌は左半結腸,特に直腸に好発する。直腸・肛門管部に発生するCD関連進行癌では,直腸・肛門管部の狭窄が目立ち,肉眼的に5型を呈することが多い(図28)。痔瘻から発生したと推測される腺癌(痔瘻癌)が多いのもCD関連消化管癌の特徴である(図29)。その他の部位に発生した大腸癌は3型を示すこともある。一方,CD関連小腸癌は本邦では多くはないが,3型もしくは4型を呈する進行癌が多くを占める1)。発生部位は回腸が75.3~95%と多く,通常の小腸癌とは異なる分布を示す2,3)。また,早期の小腸癌はCDによる炎症や潰瘍に修飾され術前に発見することは非常に困難である。隆起性病変を呈する症例に関しても炎症性ポリープとの鑑別は容易ではない(図30,図31)。 - 組織学的特徴
IBD関連消化管癌では,組織学的に単一の組織型のみならず,きわめて分化の良い高分化腺癌(いわゆる超高分化腺癌)から低分化腺癌や粘液癌などの混在した腺癌まで,多彩な組織像を呈することが多い。CD関連消化管癌においても同様の特徴を有するが,特に低分化腺癌,印環細胞癌,粘液癌の発症頻度が高い傾向がみられる。また,dysplasiaはUCだけではなくCDでも認められる(図32)。CD関連消化管癌におけるdysplasiaの併存率は27~100%と論文によりばらつきがあるものの,UCで見られるような広範囲かつ多発するdysplasiaの併存は少ないように思われる4)。2019年に出版されたWHO分類では,CDを背景に発生するdysplasiaもInflammatory bowel disease(IBD)-associated dysplasia of the colorectumに含まれ,UCと同様に,LGDとHGDに二分される5)。IBD関連dysplasiaでは,腫瘍発生早期の段階よりTP53遺伝子異常が起こることが知られており,免疫染色におけるp53蛋白異常発現の有無が反応性異型や散発性腺腫との鑑別において重要となる(図32b)(CQ 12,CQ 13)。
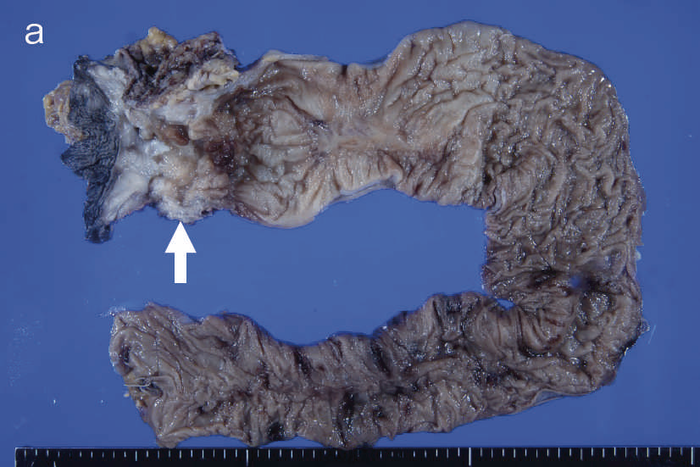
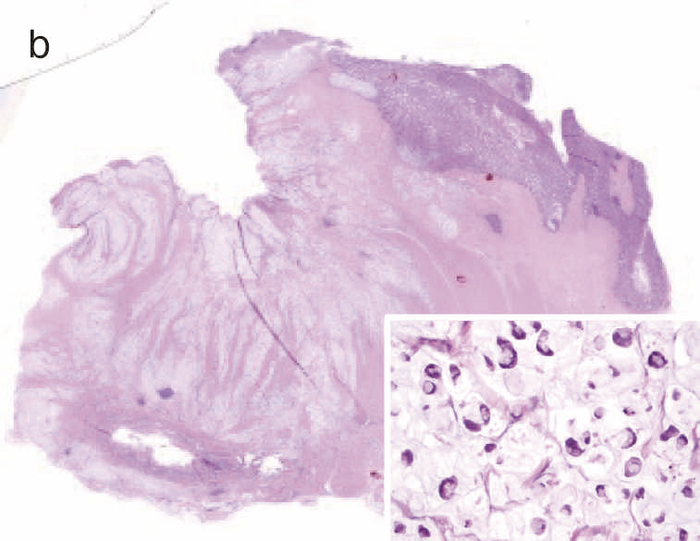
図28 CD関連進行直腸・肛門管癌(5型)の代表的な肉眼像・組織像
- 肉眼像:直腸・肛門管部に内腔狭窄を伴った5型腫瘍(矢印)を認める。
- 組織像(HE染色):組織学的には,壁内に浸潤している粘液癌を認める(inset:粘液癌の拡大像)。
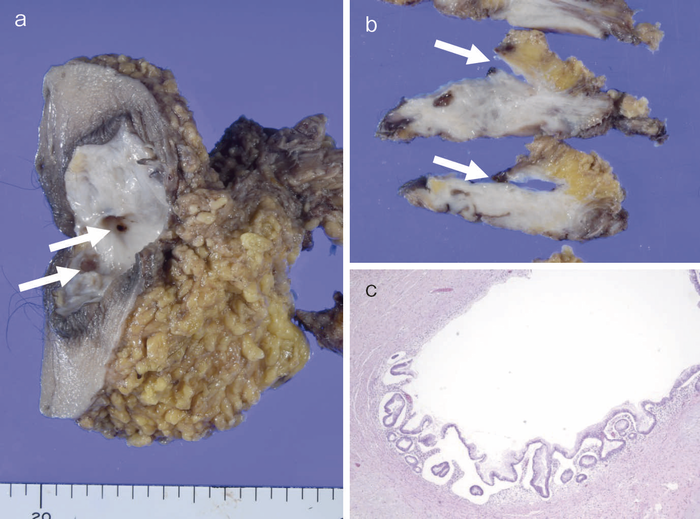
図29 CD関連痔瘻癌の代表的な肉眼像・組織像
- 肉眼像:肛門管部に痔瘻の開口部(矢印)が認められる。
- 割面像:aで認められた開口部と連続して空隙状の瘻孔形成(矢印)が認められる。
- 組織像(HE染色):瘻孔壁は胞体に豊富な粘液を含む高分化腺癌に裏装されている。
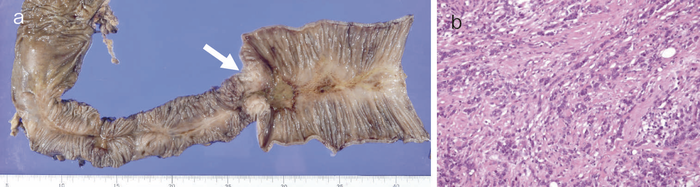
図30 CD関連小腸癌(5型)の代表的な肉眼像・組織像
- 肉眼像:縦走潰瘍を背景に,内腔狭窄を伴った5型腫瘍を認める(矢印)。狭窄により口側には著明な拡張が見られる。
- 組織像(HE染色):線維化を伴いながら小塊状・索状に増殖・浸潤する低分化腺癌を認める。
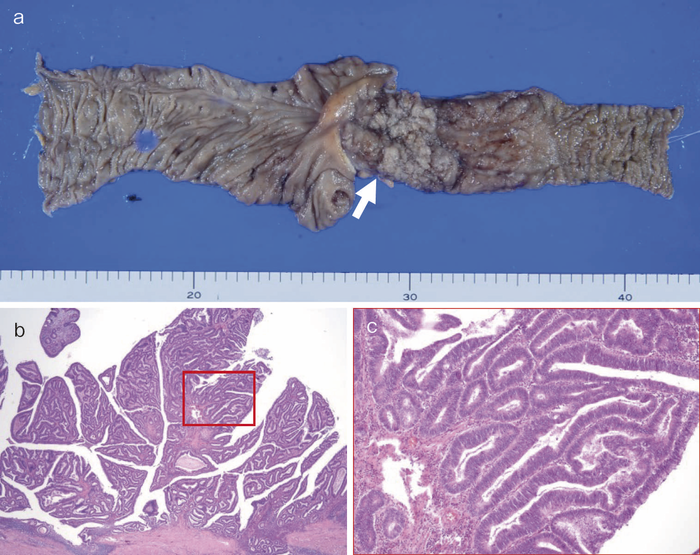
図31 CD関連小腸癌(1型)の代表的な肉眼像・組織像
- 肉眼像:回腸末端部に隆起を示す1型腫瘍を認める(矢印)。
- 組織像(HE染色)(低拡大像):管状・絨毛状に増殖する高分化管状腺癌を認める。
- bの赤枠部の拡大像。
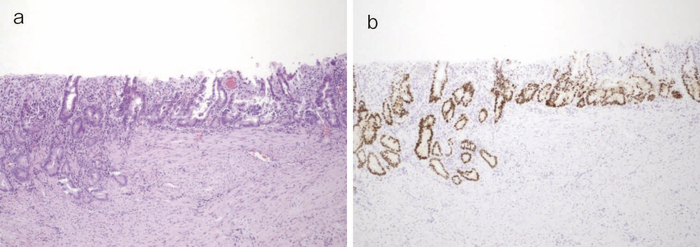
図32 CD関連消化管癌と併存するdysplasia
- 組織像(HE染色):粘膜下層へ浸潤するCD関連大腸癌(左側)に連続してdysplasiaの併存(右側)を認める。
- 同部位のp53免疫染色像:CD関連大腸癌(左側)と併存するdysplasia(右側)はいずれもp53蛋白過剰発現を示す。
- 生検診断
痔瘻癌では,粘膜表面への露出に乏しい痔瘻内部に発生した癌組織を適切かつ十分に採取することが難しい場合がある。また,痔瘻癌の多くは粘液癌であるが,生検組織の大半が粘液からなり,癌細胞がごく少数しか確認できない場合(図33)や,異型上皮を確認出来た際にも細胞異型が弱く,病理診断に苦慮することが多い6)。診断の際には免疫染色にてp53蛋白異常発現を確認することも有用である。生検組織中に異型上皮が見られない際にも多量の粘液が含まれている場合や反応性異型との鑑別を要する軽度異型上皮が採取されている場合には,粘液癌や低異型度癌を見逃さないよう,再生検を行うことが重要である。
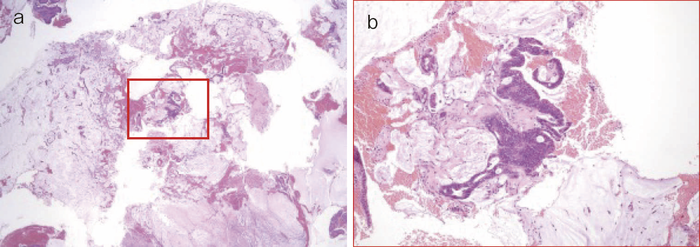
図33 痔瘻癌(粘液癌)からの生検組織像
- 組織像(HE染色)(低拡大像):生検組織の大部分は粘液からなり,その中にごく少量の異型上皮の介在を認める。
- aの赤枠部の拡大像:粘液中に浮遊する異型上皮は,細胞異型・構造異型が目立ち腺癌に相当する。本生検は粘液癌と診断された。
謝辞
本項執筆にあたり,横浜市立市民病院病理診断科 林宏行先生には多数の貴重な症例を供与頂きましたこと深く感謝申し上げます。
文献
- 岩下明徳,田邊 寛:炎症性腸疾患関連癌の臨床病理学的特徴と病理診断.松井敏幸,岩下明徳 監,松井敏幸,岩下明徳,松本主之,他 編:炎症性腸疾患関連腸癌アトラス.シービーアール出版,東京,2021:17-19
- Palascak-Juif V, Bouvier AM, Cosnes J, et al.:Small bowel adenocarcinoma in patients with Crohn’s disease compared with small bowel adenocarcinoma de novo. Inflamm Bowel Dis 2005;11:828-832
- Feldstein RC, Sood S, Katz S:Small bowel adenocarcinoma in Crohn’s disease. Inflamm Bowel Dis 2008;14:1154-1157
- 八尾隆史:クローン病発癌の病理.大腸癌Frontier 2013;6:31-35
- WHO Classification of Tumours Editorial Board:Digestive System Tumours, WHO Classification of Tumours, 5th Edition, Volume 1. Lyon:International Agency For Research on Cancer, 2019
- 林 宏行:IBD dysplasia/cancer.八尾隆史・菅井 有 編,腫瘍病理鑑別診断アトラス刊行委員会 監:腫瘍病理鑑別診断アトラス 大腸癌 第2版.文光堂,東京,2021:187-196
4 治 療
1)手術治療
● ポイント
- 本邦におけるCD関連消化管癌の多くは腺癌であり,その治療の中心は手術による切除である。
- CD関連消化管癌のうち小腸,結腸に生じたものに対しては,通常の大腸癌,小腸癌に準じ,必要十分な断端を確保した腫瘍切除,リンパ節郭清を行う。
- 本邦で最も頻度が高い直腸肛門管癌に対しても,通常の直腸癌に準じた切除,リンパ節郭清を基本とする。
- 直腸肛門管癌に対して最も行われることが多い手術は腹会陰式直腸切断術である。その際,断端陰性を確保することが重要である。
- CD関連消化管腫瘍では術前診断がつかず,術中あるいは術後に癌と診断される場合も多く,術中に癌を疑った場合には術中迅速病理診断などを行う。
● 解説
現状で,CD関連消化腫瘍に関する知見は限られており(CQ 15),本症に至適な手術治療についてエビデンスをもって示すことは困難である。このため,本稿は過去に施行された術式を参考とした。CDではその特徴から,特に小腸の可及的な温存が必要とされ1),消化管合併症の有無を含め,残存腸管長や他の消化管病変への対応も考慮し,最終的な術式を選択する必要がある。本症に合併した腫瘍はしばしば本症の消化管病変としての壁肥厚,狭窄,瘻孔また炎症の波及に伴った線維組織との鑑別が困難で,これらの組織内への癌細胞の進展の可能性があるため,癌の切除の際にはこれらの炎症性病変を含めて行わざるを得ない。また,術後のCDに対する治療に使用する薬剤(CQ 23)や合併した癌に対する補助化学療法,および進行,再発癌に対する化学療法(CQ 24,25)には配慮が必要である。
- CD関連小腸腫瘍
CD関連小腸癌は主に回腸に生じ,回腸部分切除術,あるいは回盲部切除術が行われることが多い。一方で,リンパ節への転移度,壁内進展の範囲などが示された報告もなく,適切なリンパ節郭清の範囲や切除範囲については不明である。
CDの小腸切除時には可及的な腸管温存が基本であり1),小腸癌合併例では断端陰性の確保に加え考慮に入れる必要がある。また,過去の報告からは,リンパ節転移が予後規定因子になる可能性があり(CQ 19),リンパ節郭清は行うべきと考えられる。
CDの活動性病変付近に腫瘍が存在し,活動性病変と癌あるいはdysplasiaの範囲が不明瞭な場合にはこれら全体の切除を行う(症例1)。リンパ節はしばしば腸管の炎症に伴って病変周囲に腫大を認めるため,転移との鑑別は困難な場合もあり,至適郭清範囲が不明な現時点ではリンパ節郭清範囲は術中に判断せざるを得ない。
症例1 回腸癌(40歳代女性)
2年前にUCと診断されたが,1年前に,痔瘻の悪化と内視鏡検査で回腸末端に縦走潰瘍を認め,CDと診断された。adalimumabで治療が開始され,治療効果判定目的に施行した内視鏡検査で回腸に潰瘍を認め,生検でadenocarcinomaと診断された(内視鏡画像なし)。
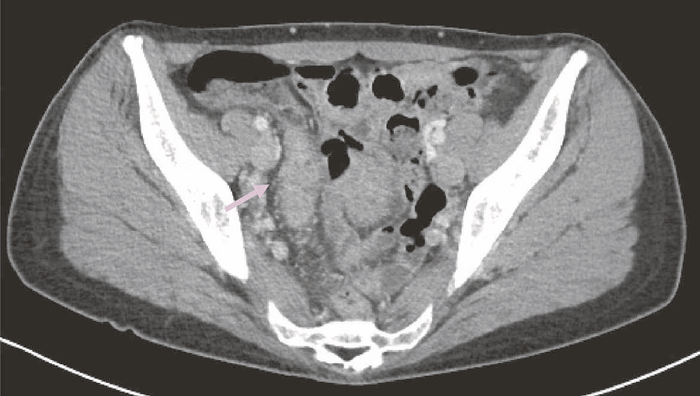
図34 術前CT
術前CTでは回腸末端の壁肥厚を認め,周囲リンパ節の腫大は明らかではなかった。
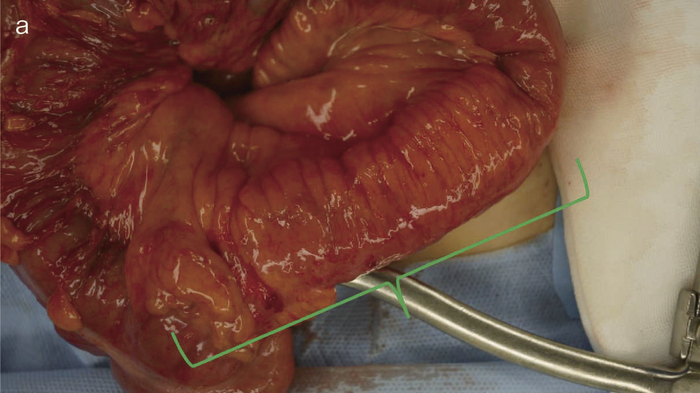
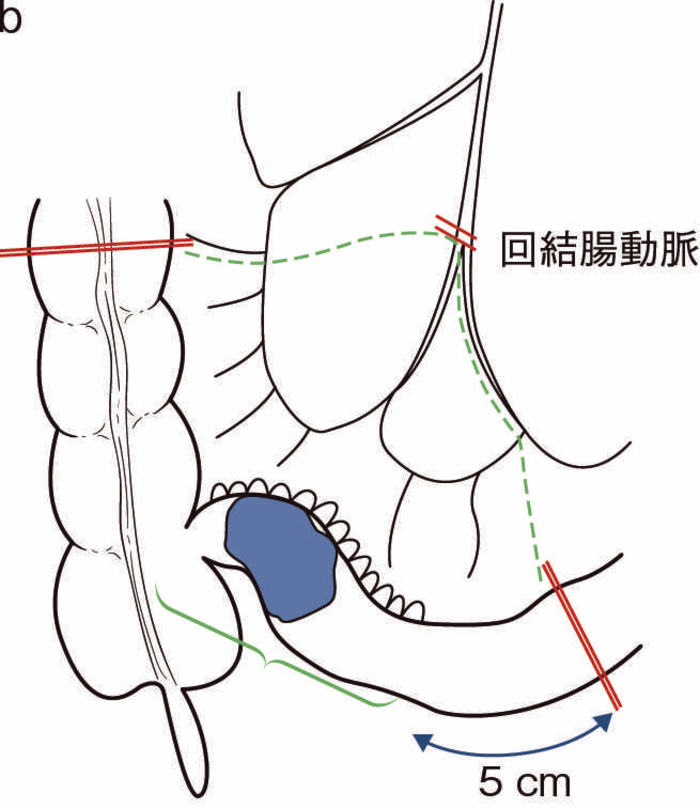
図35 術中所見と術式
術中所見では,肝転移,腹膜播種はなく,回盲部周囲のリンパ節には軽度の腫大を認めたものの,明らかな転移を疑う所見はなかった。回腸末端部に回盲弁から連続した壁硬化とfat creepingを伴う病変を認めた(図35a緑の範囲)。回結腸動脈が主な支配血管であり,触診上壁の硬化を認めた部から口側に5 cmまでの回腸と上行結腸を切除した。術中,迅速病理診断で202リンパ節に転移がないことを確認し,回結腸動脈根部まで郭清した。
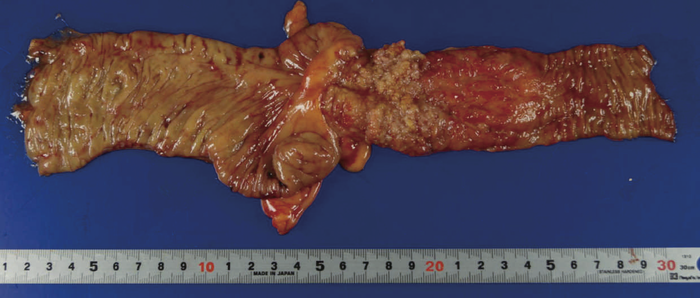
図36 切除標本
切除標本の肉眼像では4 cm長の全周性腫瘍でvillous様の構造を呈しており,この肛門側に縦走潰瘍を伴う5 cm長の病変(炎症)を認めた。
病理組織検査所見では,well differentiated adenocarcinoma,m,ly0,v0,pN0,p53弱陽性,全層性炎症で非乾酪性類上皮性肉芽腫を認め,診断後の経過は短いものの,CDの慢性炎症から生じた炎症性発癌と考えられた。
CD腸管癌では周囲病変と癌あるいはdysplasiaの範囲を区別することは困難で,本症例のように切除範囲が長くなる場合もあり得る。
- CD関連結腸腫瘍
本邦ではCD関連大腸腫瘍の多くが直腸肛門管に生じる。このため,結腸腫瘍に対する術式について検討した報告はない。過去の報告でみると,結腸右半切除術,結腸左半切除術,S状結腸切除術が挙げられており2),現時点ではCD関連結腸腫瘍については通常の大腸腫瘍と同様な術式を行うべきと考えられる(CQ 15)。
一方,欧米からはCD関連大腸腫瘍では癌または異型上皮が同時性,異時性多発することや,大腸部分切除術施行例が大腸全摘術施行例より再手術率が高い報告が認められるものの,どのような症例に大腸全摘術の適応があるかは明確ではない(CQ 15)。 - CD関連直腸肛門管腫瘍
本邦のCD関連消化管腫瘍では直腸肛門管癌(痔瘻癌を含む)が最も多い。過去の報告では直腸肛門管癌に対しては,低位前方切除術,腹会陰式直腸切断術が行われているが,最も多いのは腹会陰式直腸切断術である2)(CQ 18)。本邦と同様に腺癌が多い韓国からの報告でも腹会陰式直腸切断術が多い3)。欧米の痔瘻に関連した癌の報告では放射線化学療法が施行されている症例もあるものの,扁平上皮癌の症例があることが影響している4)。
通常の大腸癌に準じ,腫瘍の局在や深達度,リンパ節転移などを加味し,さらにCDの病変範囲と状態を診て術式を決定する必要がある。直腸肛門管癌では,組織型では粘液癌が多く,多くの症例で痔瘻,膿瘍,狭窄,直腸瘻などの直腸肛門部病変を合併しており,腹会陰式直腸切断術が最も選択されやすい。一方,上部の直腸癌(RSあるいはRa)で周囲臓器への浸潤がなく,直腸肛門部病変を含むCDの活動性病変が肛門側にない場合には,前方切除術やハルトマン手術などが可能な場合もある。
一般的な痔瘻癌でも断端陽性例が多いことが報告されているが5,6),本症でも同様で7),直腸肛門部病変合併例では,瘻管内や線維化した組織内にも腫瘍細胞が存在し,腫瘍の進展範囲の判断が難しい症例があり,術中には断端の確保に留意する。多発する瘻管のある複雑痔瘻合併例では肛門側皮膚を切除する際から関連する痔瘻の瘻管を残さない範囲まで可及的に切除し,骨盤内でも,瘻管や膿瘍,瘢痕組織など腫瘍が存在する可能性のある組織は可及的に切除する(症例2,3)。骨盤内臓器への浸潤に対し,断端陰性が可能と判断される場合には男性の前立腺,精囊腺の部分切除,女性の腟壁切除なども考慮する(症例3)。骨盤内臓全摘術や会陰部の皮膚欠損部への筋皮弁充填などが行われた報告が散見されるものの8,9),遠隔成績は不明で,本症での適応の決定には今後の検討が必要である。
症例2 痔瘻癌(50歳代男性)
23年前 CDと診断され,回盲部切除術を施行。
18年前 直腸周囲膿瘍,痔瘻を発症。以降,seton法を計2回施行。5-ASA製剤で加療。
11年前 infliximab投与開始し,腹部症状は安定。以降,毎年痔瘻の細胞診を施行。
X年 痔瘻の細胞診でclass Ⅲb。痔瘻癌が疑われ,全身麻酔下に瘻孔から生検施行。
病理組織所見でadenocarcinoma。痔瘻癌(TXN1M0)の診断で手術施行。
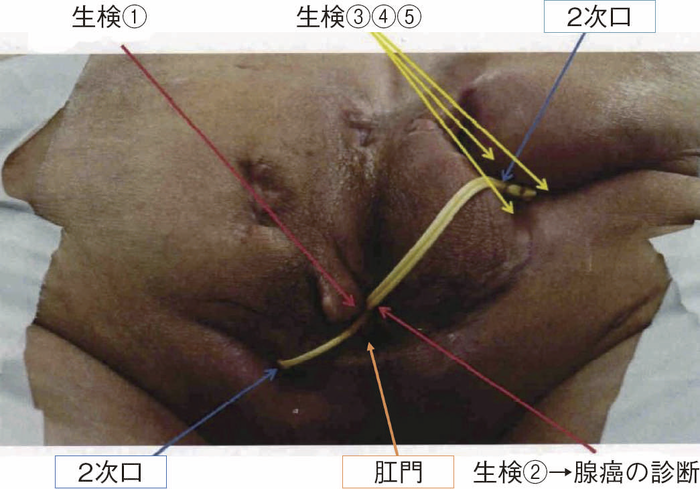
図37 肛門部所見と生検組織採取部位(Jack-knife position)
図上が背側(6時方向),下が腹側(0時方向)。肛門の右後方(7時方向)にある2次口からの分泌物の細胞診はclass Ⅲbであった。全身麻酔下の生検ではその2次口の原発口からadenocarcinomaが検出された。
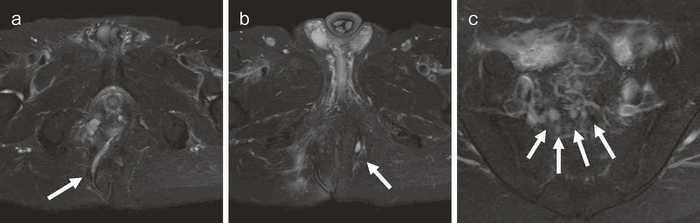
図38 骨盤部MRI
術前の骨盤部MRIでは右側の痔瘻瘻管と,左側の瘻管,周囲のリンパ節腫大を認めた。
明らかな癌を示す所見は不明であった。
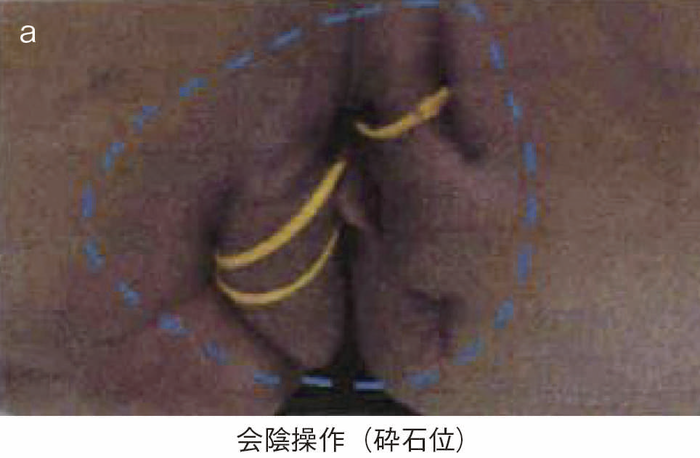
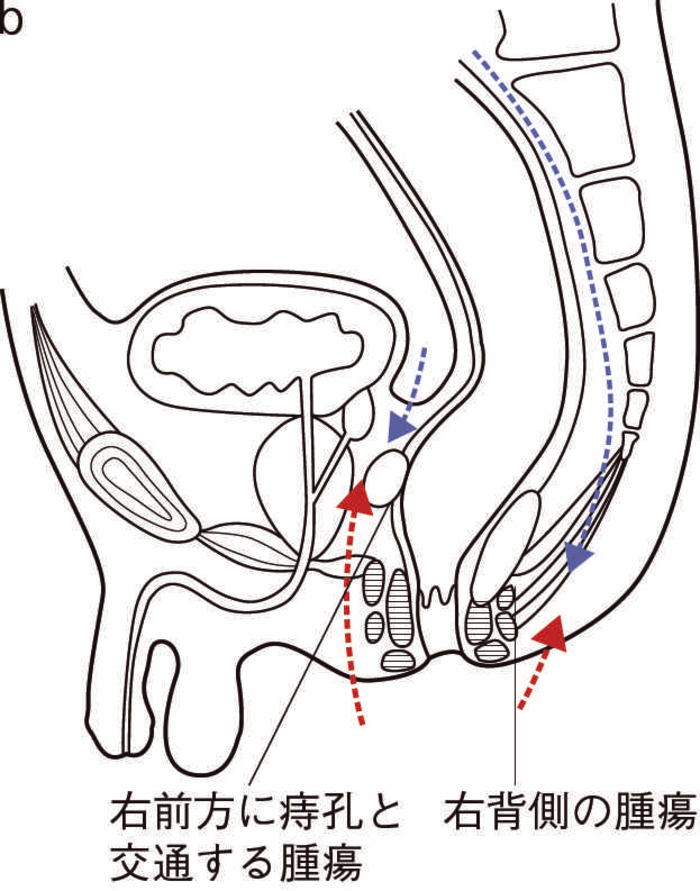
図39 術式と術中所見(直腸切断術,リンパ節郭清(D3))
D3郭清を伴う直腸切断術を施行した。
術中所見では直腸の右側には前立腺の高さの前方と後方に膿瘍を認め,それぞれ癌と診断された瘻管と交通の可能性があり,これらを取り残すことがないよう外側で切離を行った。特に,前壁側では精囊腺,前立腺との境界が不明瞭であり,腹腔側からのアプローチのみでは困難で,肛門側からの操作を合わせて施行して切離した。肛門側ではすべての痔瘻瘻管を切離するように皮膚切開を置き,瘻管とその周囲の炎症が波及した組織を含めて切除を行った(生検施行時とは異なり体位が砕石位で,本図では腹側で0時方向)。
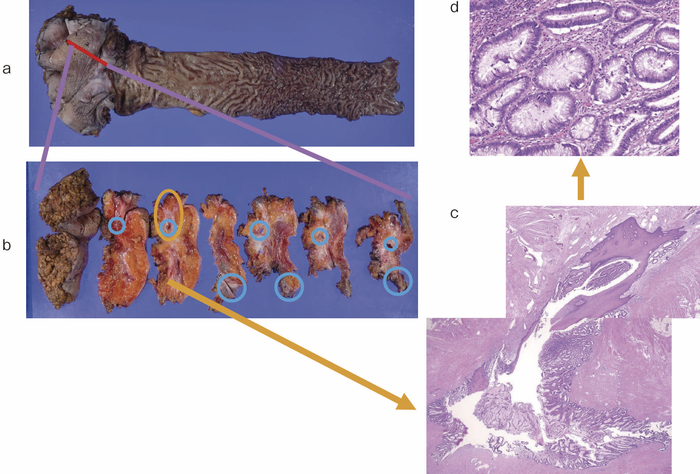
図40 切除標本と病理組織所見
痔瘻の瘻管を伝うように広がる粘液癌で,浸潤傾向がなく,瘻管に限局していた。
マッピングの赤線部で示す瘻管に癌があった。
Mucinous adenocarcinoma,Type 5 50×15×10 mm(T2)Budding 1,低分化成分なし,p53陽性,PN0,Ly0,V0,pN0,H-,P-,EX-,断端陰性
症例3 直腸肛門管癌(60歳代男性)
40年前 肛門周囲膿瘍で手術。
19年前 CDと診断。
4年前 回腸周囲に膿瘍形成があり,回腸回盲部切除術施行。
2年前 吻合部にCDの腸管病変が再発。
X年 発熱,肛門部痛,残便感が出現し,肛門周囲膿瘍を認め,切開排膿術施行。
精査で施行したCT,MRIで痔瘻癌が疑われた。
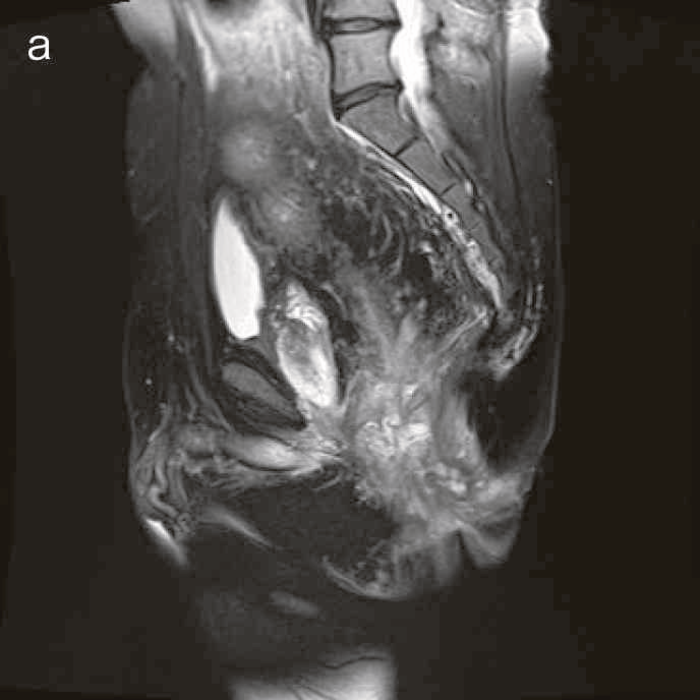
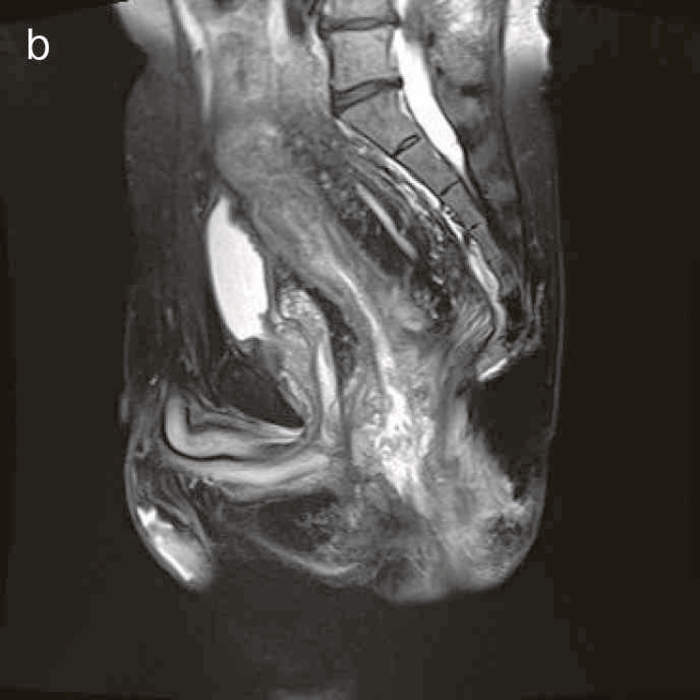
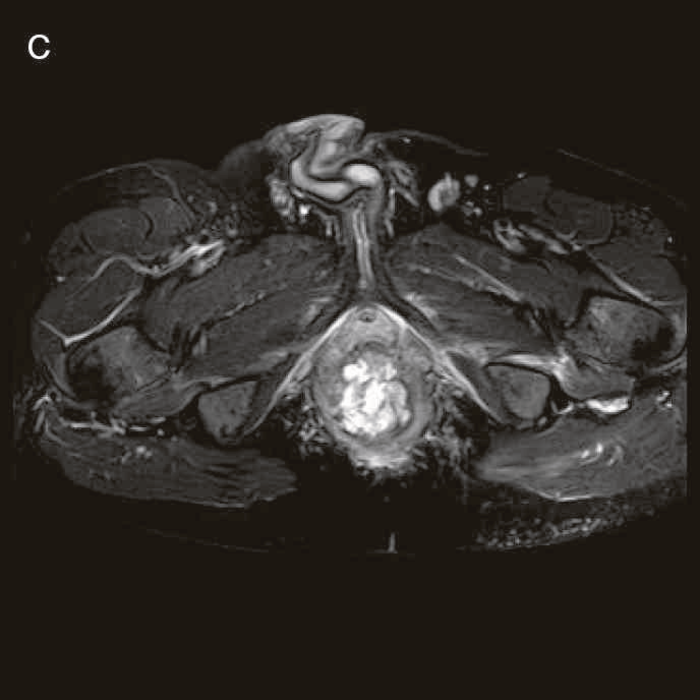
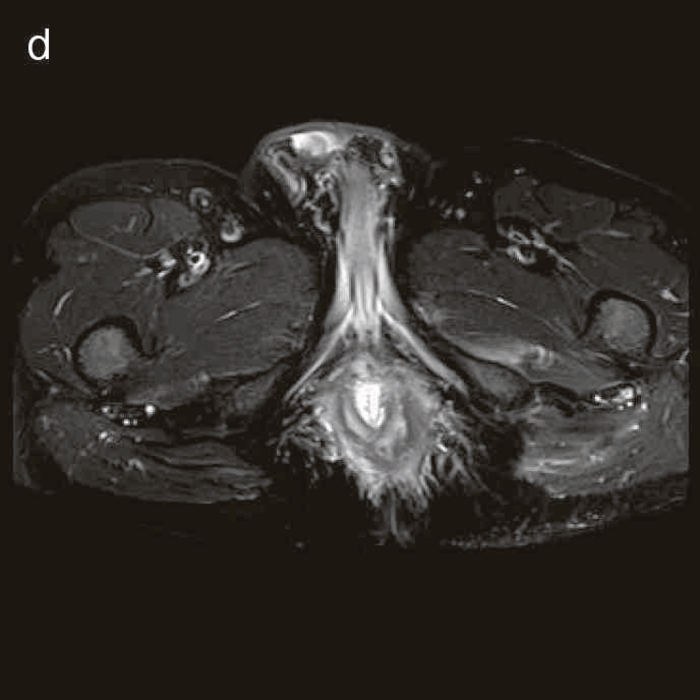
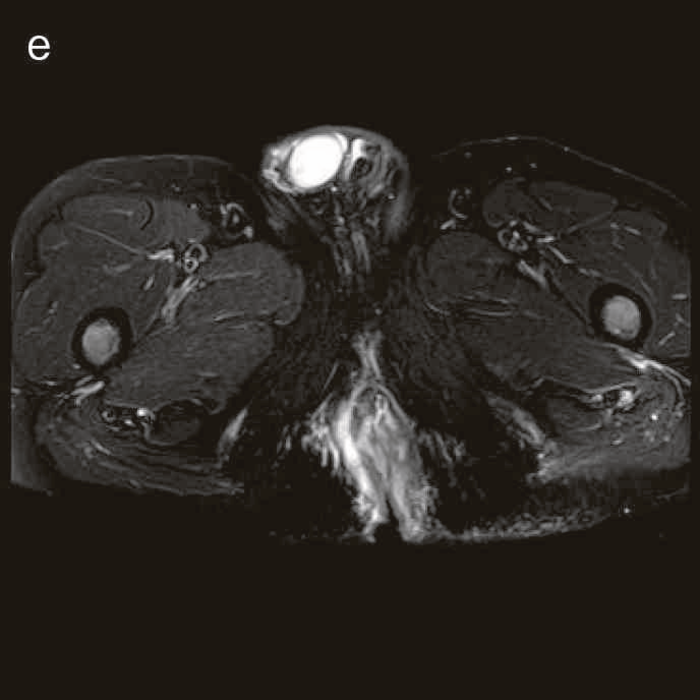
図41 腹部骨盤MRI
診断時のMRIでは直腸下部壁内から周囲にhigh intensity areaが拡がり,右側には痔瘻の瘻管を認めた。high intensity areaは前方で前立腺や陰茎海綿体付近まで広がっていた。
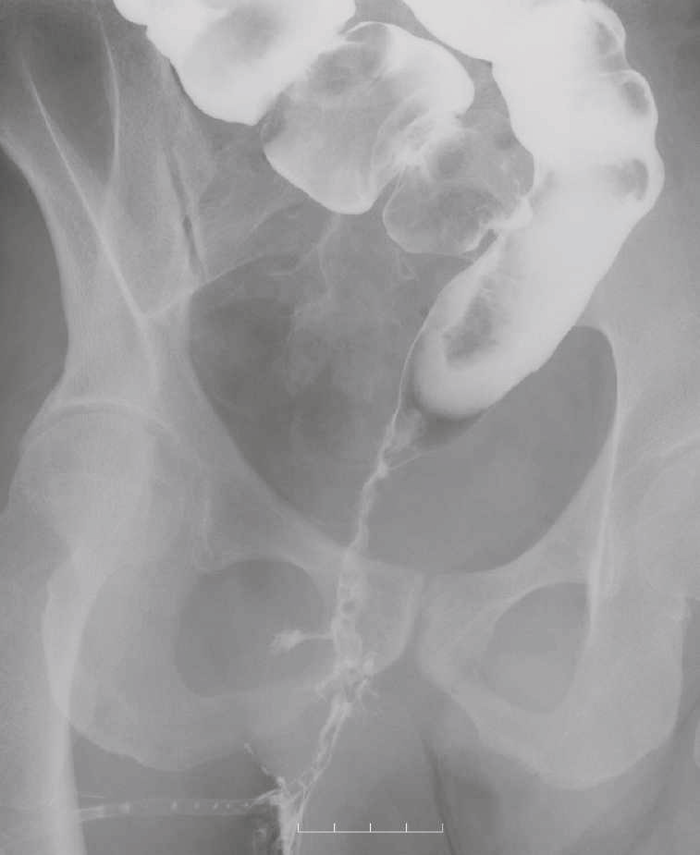
図42 注腸造影検査
注腸造影検査では,直腸は狭小化しており,痔瘻に続く,瘻管が描出された。
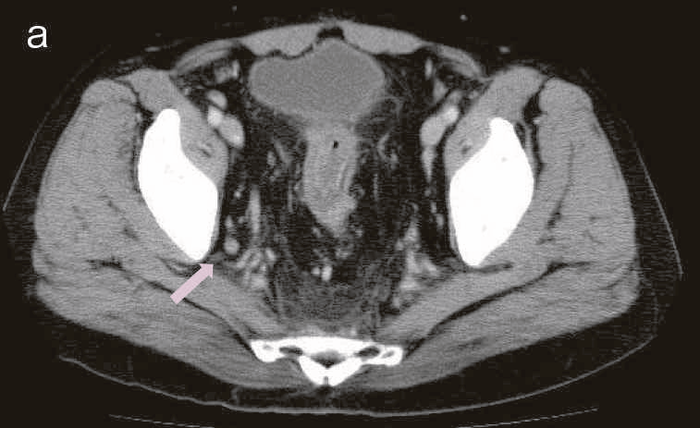
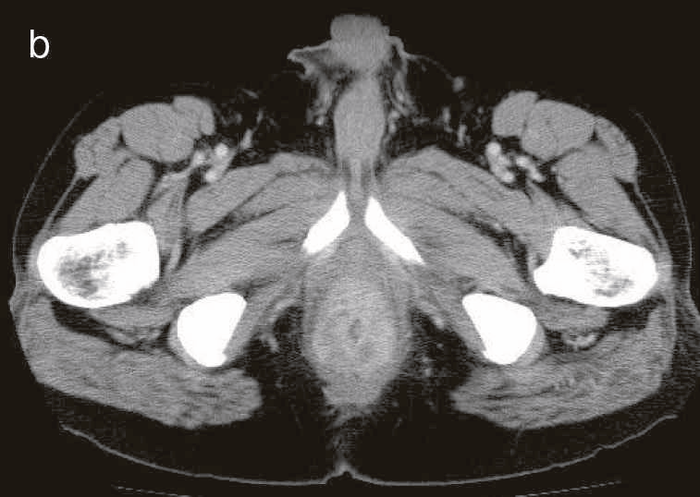
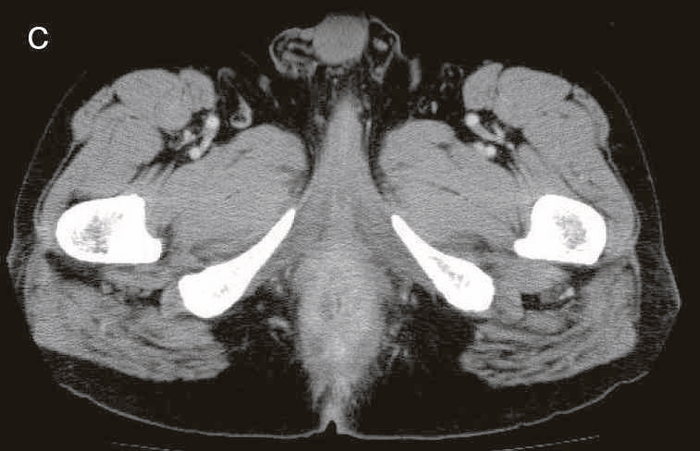
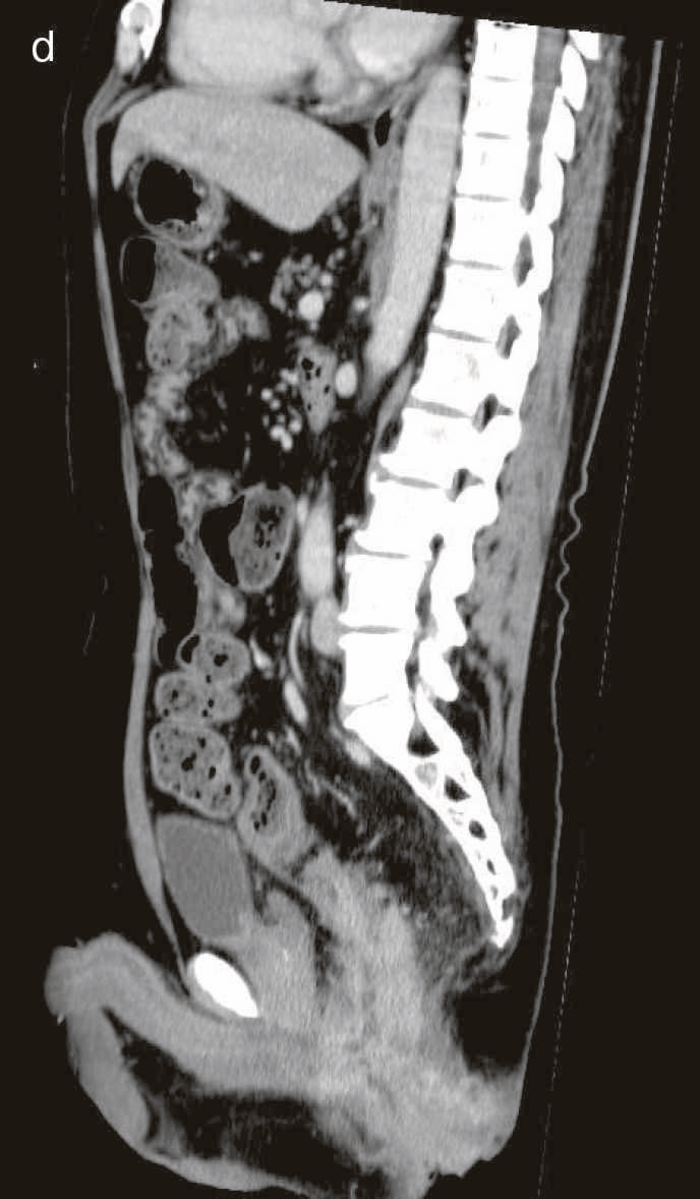
図43 腹部骨盤CT
CTではMRIと同様に広範囲のhigh density areaがあり,癌と炎症が波及した領域の区別がつかず右側方領域にリンパ節腫大を認めた。
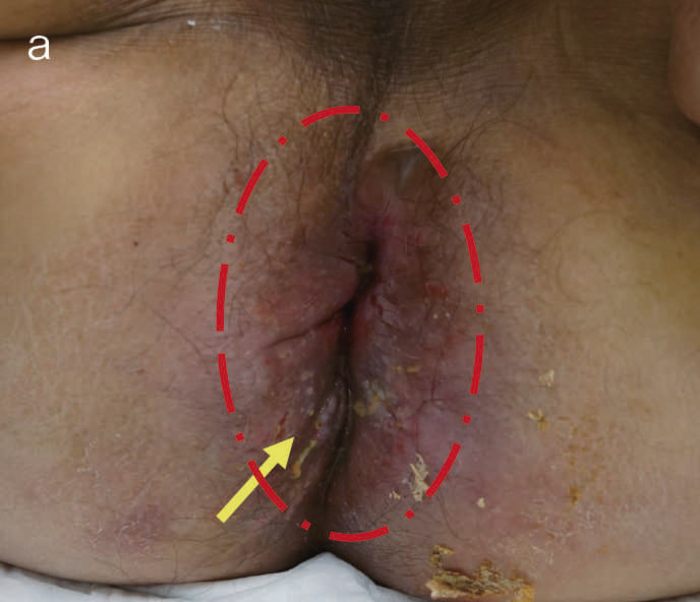
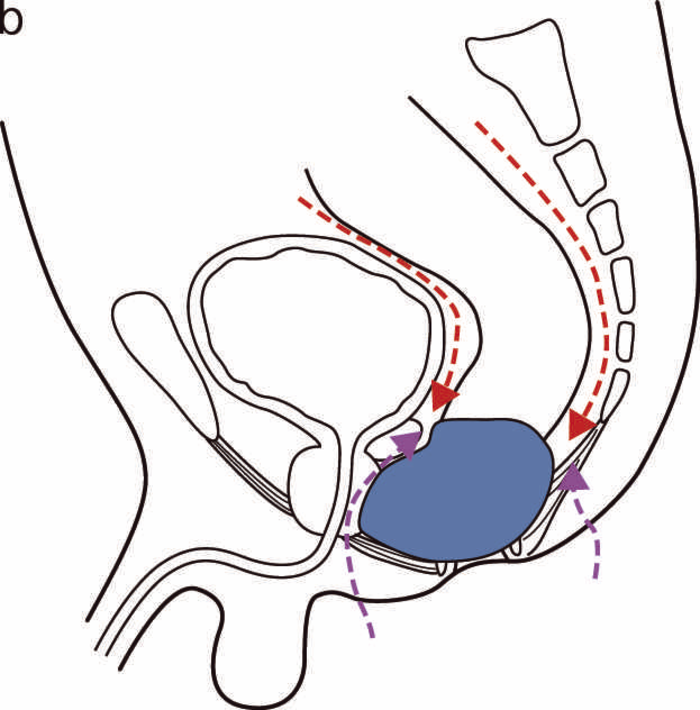
図44 術式と術中所見(直腸切断術,リンパ節郭清(D3))
術中所見では,肝転移,腹膜播種はなく,腹腔内には転移を疑うリンパ節は認めなかった。
下腸間膜動脈を根部で処理するD3郭清と右側方リンパ節郭清を施行。術前画像にもあるように直腸間膜の肥厚が著しく,骨盤内からは後壁側は腫瘍の背側から肛門挙筋付近までの剝離が可能であったが,前側は精囊腺,前立腺と炎症,あるいは癌の境界が不明で,精囊腺の頭側までしか剝離ができなかった(赤矢印)。また,肛門側は痔瘻の2次口を含む瘻管,硬結をすべて切除するように皮膚切開を施行した。前後壁とも骨盤側と会陰側からの操作を繰り返しながら,腫瘤からのmarginを確保しながら切除することとなった。このため,精囊腺の一部と前立腺の一部を合併切除した。
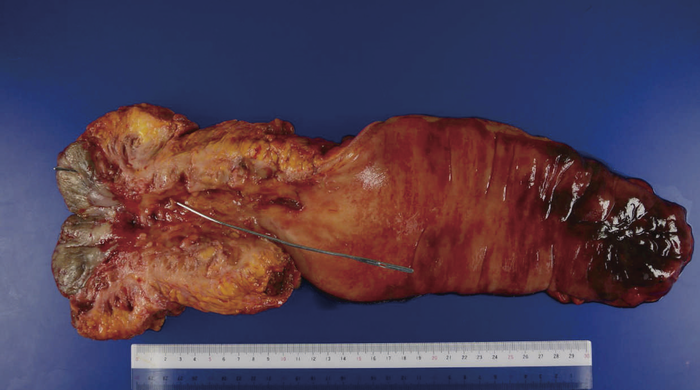
図45 切除標本
切除標本では痔瘻につながる瘻管(消息子が留置されている)と肥厚した直腸壁があり,裏面には合併切除した前立腺と精囊腺の一部があった。
病理組織検査所見ではwell differentiated tubular adenocarcinomaで,痔瘻は癌の辺縁にあり,直腸肛門管癌の診断,Type 4 80×45×11 mm,RbP,低分化成分なし,PN0,ly0,v0,pN0(0/32),H-,P-,EX-,pPM0,pDM0,pRM0,pStage 2であり,前立腺,精囊腺への浸潤はなく,根治手術であった。
文献
- 厚生労働科学研究費補助金難治性疾患政策研究事業「難治性炎症性腸管障害に関する調査研究」(久松班):クローン病外科治療指針.「潰瘍性大腸炎・クローン病 診断基準・治療指針」令和3年度分担研究報告書,2022
- Higashi D, Katsuno H, Kimura H, et al.:Current State of and Problems Related to Cancer of the Intestinal Tract Associated with Crohn’s Disease in Japan. Anticancer Res 2016;36:3761-3766
- Lee YN, Lee JL, Yu CS, et al.:Clinicopathological Characteristics and Surgical Outcomes of Crohn Disease-Associated Colorectal Malignancy. Ann Coloproctol 2021;37:101-108
- Palmieri C, Müller G, Kroesen AJ, et al.:Perianal Fistula-Associated Carcinoma in Crohn’s Disease:A Multicentre Retrospective Case Control Study. J Crohns Colitis 2021;15:1686-1693
- 鮫島伸一,澤田俊夫,長廻 紘:本邦における肛門扁平上皮癌,痔瘻癌の現況,第59回大腸癌研究会アンケート調査報告.日本大腸肛門病会誌2005;58:415-421
- 佐藤太一,山田一隆,緒方俊二,他.痔瘻癌25例の臨床病理学的検討.日消外誌2016;49:579-587
- Sasaki H, Ikeuchi H, Bando T, et al.:Clinicopathological characteristics of cancer associated with Crohn’s disease. Surg Today 2017;47:35-41
- 杉田 昭,小金井一隆,辰巳健志,他:クローン病に合併する直腸肛門管癌.日消誌2013;110:396-402
- 北山 卓,佐藤 俊,阿部道夫,他:有茎筋皮弁自家移植術により肛門管癌を治療した小腸大腸型Crohn病の1例.日臨外会誌2007;68:406-409
2)薬物療法(CQ 23,24,25)
● ポイント
- CD関連消化管癌に対する薬物療法には,術後再発予防を目的とした補助化学療法と,切除不能進行・再発癌の延命や症状緩和を目的とした薬物療法がある。CD関連大腸癌に対し,本邦のガイドライン1)に準じ薬物療法の適応判断やレジメン選択を行う。
- CD関連小腸癌に対し,大腸癌に準じた薬物療法が選択されている2)。
- 薬物療法に伴う胃腸障害(特に下痢)とCDの再燃との鑑別が時に困難であることに注意を要する(CQ 25)。
- ECCOガイドライン3)では,5-ASA製剤,栄養療法,ステロイド製剤は担癌状態であっても安全に使用できるとされている一方,少なくとも抗癌薬物療法施行中はチオプリン製剤,カルシニューリン阻害薬,抗TNFα抗体製剤の投与を避けるよう推奨されている。ただしCDの再燃時はその限りでなく,消化器内科医,腫瘍内科医,外科医がそれぞれの専門性をもって治療方針を協議し,症例ごとに判断されることが望ましい4)(CQ 23,25)。
● 解説
- 術後補助化学療法
CD関連大腸癌に対する術後補助化学療法の有用性を手術単独群と比較したランダム化比較試験は存在せず,病理学的Stageや再発リスクだけでなく,全身状態,CDの残存病変の程度や広がり,CDの治療内容などを考慮して適応の判断やレジメンの選択を行う(CQ 24)。
CD関連小腸癌に対する術後補助化学療法の有用性を示した報告はなく,再発抑制効果および生存期間延長効果は明らかでない(CQ 24)。 - 切除不能進行・再発癌に対する薬物療法
CD関連の進行・再発消化管癌症例に対する薬物療法の有効性を散発性消化管癌と比較したメタアナリシスやランダム化比較試験,前向きコホート研究は存在しない。IBD関連進行・再発消化管癌に対し,一次治療としてFOLFOXまたはFOLFOX+BEV療法,FOLFIRIまたはFOLFIRI+BEV療法,5FU+l-LV療法等のレジメンを用いた後ろ向き症例対照研究5,6),後ろ向き症例集積研究7)の結果が報告されているが(CQ 25),CD関連大腸癌の薬物治療選択に際し特定のレジメンを推奨できるエビデンスに乏しい。
小腸癌は希少疾患であり,CD症例に限った薬物療法の有用性を検討した報告はないものの,小腸癌347例を対象とした前向きコホート研究(ARCAD-NADEGE)8)では8.7%がCD症例であった。進行・再発小腸腺癌に対する一次治療としてFOLFOX療法(奏効率48.5%,無増悪生存期間中央値7.8カ月)9)や,CAPOX療法(奏効率50%,無増悪生存期間中央値11.3カ月)10)の成績が報告されている。進行・再発小腸癌に対する治療戦略を検討したレビュー2)では,一次治療にFOLFOX療法あるいはCAPOX療法,二次治療としてFOLFIRI療法が推奨されている。 - 薬物療法とCDの病勢コントロール
(1)CD再燃時の治療選択
薬物療法中のCD再燃時に,短期間の全身ステロイド製剤の投与は許容される3,11,12)。ステロイドに反応しない場合,抗TNFα抗体製剤の投与が検討される4,13,14)が,作用機序よりベドリズマブの使用も考慮される(CQ 23)。また,病状に応じて外科治療の選択肢も検討しておく14)。(2)薬物療法終了後のCD治療薬選択
免疫抑制的治療(免疫調節薬,生物学的製剤)は癌治療が終了した後に実施することが推奨される(CQ 23)。
ECCOガイドライン3)やレビュー4,14)によると,免疫抑制的治療は癌治療終了後少なくとも2年間,再発リスクが中等度,あるいは高度では5年間行わないよう提言されている(CQ 23)。
文献
- 大腸癌研究会編:大腸癌治療ガイドライン 医師用2022年版,金原出版,東京,2022
- Moati E, Overman MJ, Zaanan A:Therapeutic Strategies for Patients with Advanced Small Bowel Adenocarcinoma:Current Knowledge and Perspectives. Cancers(Basel)2022;14:1137
- Annese V, Beaugerie L, Egan L, et al.:European evidence-based consensus:inflammatory bowel disease and malignancies. J Crohns Colitis 2015;9:945-965
- Fiorillo C, Schena CA, Quero G, et al.:Challenges in Crohn’s Disease Management after Gastrointestinal Cancer Diagnosis. Cancers(Basel)2021;13:574
- Yaeger R, Paroder V, Bates DB, et al.:Systemic chemotherapy for metastatic colitis-associated cancer has a worse outcome than sporadic colorectal cancer:matched case cohort analysis. Clin Colorectal Cancer 2020;19:e151-e156
- Axelrad J, Kriplani A, Ozbek U, et al.:Chemotherapy tolerance and oncologic outcome in patients with colorectal cancer with and without inflammatory bowel disease. Clin Colorectal Cancer 2017;16:e205-e210
- Nio K, Higashi D, Kumagai H, et al.:Efficacy and safety analysis of chemotherapy for advanced colitis-associated colorectal cancer in Japan. Anticancer Drugs 2016;27:457-463
- Aparicio T, Henriques J, Manfredi S, et al.:Small bowel adenocarcinoma:Results from a nationwide prospective ARCAD-NADEGE cohort study of 347 patients. Int J Cancer 2020;147:967-977
- Xiang XJ, Liu YW, Zhang L, et al.:A phase Ⅱ study of modified FOLFOX as first-line chemotherapy in advanced small bowel adenocarcinoma. Anticancer Drugs 2012;23:561-566
- Overman MJ, Varadhachary GR, Kopetz S, et al.:Phase Ⅱ study of capecitabine and oxaliplatin for advanced adenocarcinoma of the small bowel and ampulla of Vater. J Clin Oncol 2009;27:2598-603
- Bernheim O, Colombel J-F, Ullman A, et al.:The management of immunosuppression in patients with inflammatory bowel disease and cancer. Gut 2013;62:1523-1528
- Beaugerie L, Rahier J-F, Kirchgesner J:Predicting, Preventing, and Managing Treatment-Related Complications in Patients With Inflammatory Bowel Diseases. Clin Gastroenterol Hepatol 2020;18:1324-1335. e2
- Brown ER, Charles KA, Hoare SA, et al.:A clinical study assessing the tolerability and biological effects of infliximab, a TNF-alpha inhibitor, in patients with advanced cancer. Ann Oncol 2008;19:1340-1346
- Sebastian S, Neilaj S:Practical guidance for the management of inflammatory bowel disease in patients with cancer. Which treatment? Ther Adv Gastroenterol 2019;12:1-15
5 予 後
● ポイント
- CD関連大腸癌の全生存は散発性大腸癌よりも不良である。
- CD関連大腸癌の全生存はUC関連大腸癌よりも不良である。
- 肛門部癌の頻度が高く,切除術後の再発は局所再発が多い。
● 解説
- CD関連大腸癌(結腸癌+直腸癌)の全生存
大腸癌研究会で行われたプロジェクト研究「炎症性腸疾患合併消化管癌のデータベース作成と臨床病理学的研究」(以下「プロジェクト研究」)で集積された,CD関連消化管癌症例(1983~2020年)の中で45%が大腸癌(結腸癌+直腸癌,肛門管癌を除く)であった1)。全生存率を図46に示す。進行度がStage 0,1である症例の5年全生存率はそれぞれ100%,90%と比較的良好であるが,Stage 2症例の5年全生存率は76%と大きく低下し,Stage 3症例では18%,Stage 4症例では0%と進行癌症例の予後は極めて不良である。CD関連大腸癌と散発性大腸癌を直接比較した国内外の報告に関するシステマティックレビューにおける5論文のメタアナリシスでは,散発性大腸癌に比べてCD関連大腸癌の全生存率は優位に不良であることが示されている(HR 1.32)2)(CQ 27)。 - UC関連大腸癌との比較
プロジェクト研究で行われたUC関連大腸癌との全生存率の比較においては,Stage 0,1症例の全生存は同等であったが,Stage 2,3,4症例においてはCD関連大腸癌(結腸癌+直腸癌)の全生存はUC関連大腸癌に比べて有意に不良であった1)(各論Ⅰ,UC関連消化管腫瘍,5.予後を参照)。CD関連大腸癌とUC関連大腸癌の予後を直接比較した論文は少ないが,3論文のメタアナリシスの結果でも同様にCD関連大腸癌の全生存はUC関連大腸癌よりも有意に不良である結果が示されている(UC関連大腸癌のCD関連大腸癌に対するHR 0.79)2)。 - CD関連小腸癌
CD患者は一般人口と比べて小腸癌のリスクが相対的に高いが,絶対的な頻度は少なく,システマティックレビューにおける33論文のメタアナリシスの結果ではCD関連小腸癌の頻度は1,000 CD患者あたり1.15とされる3)。同論文においてCD関連小腸癌879例の5年全生存率は29%と報告されており,散発性小腸癌4,197例の33%よりも有意に不良であったと報告されている。本邦プロジェクト研究においては29例のCD関連小腸癌が集積され,5年全生存率は71%であり(図47),比較的良好な結果であった1)。しかしながらStage 4で診断された症例の予後は5年全生存率が17%と不良であった(図48)。 - CD関連肛門管癌
本邦におけるCD関連消化管腫瘍は肛門管癌の占める頻度が高いのが特徴であり,プロジェクト研究の集積症例においても44%が肛門管癌であった1)。進行度別の全生存率を図49に示す。78%の症例がStage 2,3,4の進行した状態で診断されており,5年全生存率はそれぞれ50%,28%,0%と不良であった。 - 術後再発形式
プロジェクト研究で集積されたCD関連消化管癌の手術後における部位別再発症例数(観察期間中央値36カ月)を図50に示す。局所再発が最も多い再発形式であることが特徴であるが,これは局所進行の直腸肛門管癌症例が多いことが一因であると考えられる1)。
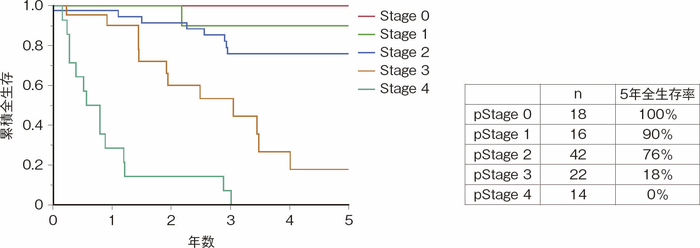
図46 CD関連大腸癌(結腸癌+直腸癌,全生存率)
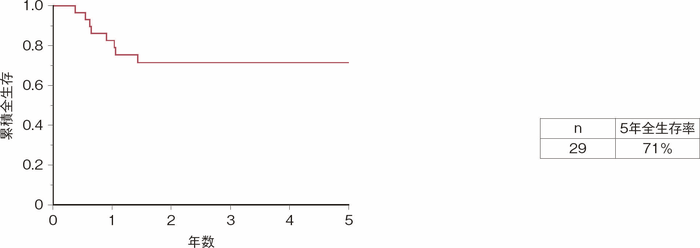
図47 CD関連小腸癌(全生存率)
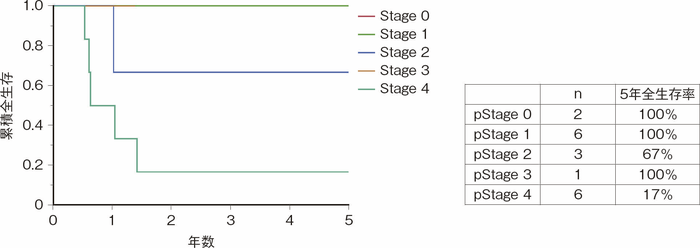
図48 CD関連小腸癌(全生存率)
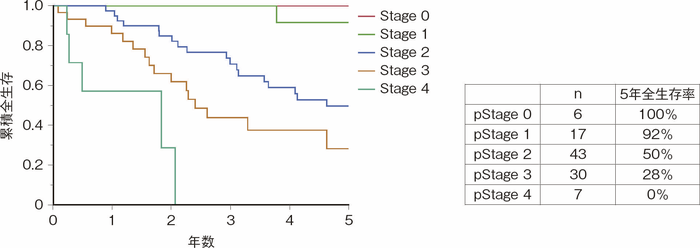
図49 CD関連肛門管癌(全生存率)
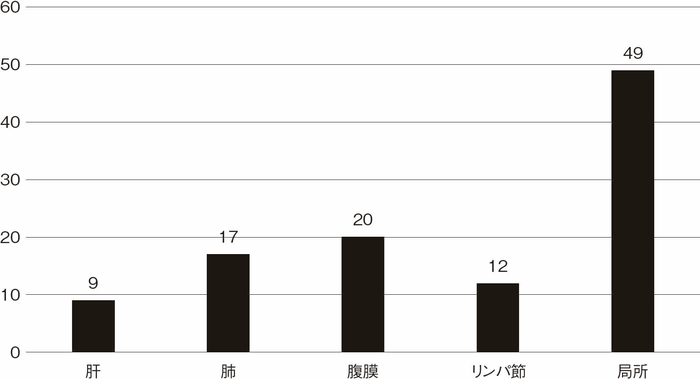
図50 CD関連消化管癌再発部位
文献
- Noguchi T, Ishihara S, Uchino M, et al.:Clinical features and oncological outcomes of intestinal cancers associated with ulcerative colitis and Crohn’s disease. J Gastroenterol 2023;58:14-24
- Lu C, Schardey J, Zhang T, et al.:Survival Outcomes and Clinicopathological Features in Inflammatory Bowel Disease-associated Colorectal Cancer:A Systematic Review and Meta-analysis. Ann Surg 2021;276:e319-e330
- Chin YH, Jain SR, Lee MH, et al.:Small bowel adenocarcinoma in Crohn’s disease:a systematic review and meta-analysis of the prevalence, manifestation, histopathology, and outcomes. Int J Colorectal Dis 2022;37:239-250









