
各論Ⅰ
Ⅰ. UC関連消化管腫瘍
1 疫 学
● ポイント
- UCの長期罹患や炎症範囲が左側以上でUC関連大腸腫瘍の発生リスクが増大する。
- 原発性硬化性胆管炎(primary sclerosing cholangitis:PSC)合併,中等度以上の活動性炎症,dysplasia既往,大腸癌家族歴,狭窄病変など大腸癌発生のリスク因子に注意する。
- 前癌病変であるdysplasiaの早期診断が重要である。
● 解説
-
発生頻度
UCは長期罹患に伴う粘膜の慢性炎症を背景に発癌リスクが上がることが知られており,1925年にCrohnとRosenbergが最初のUC関連大腸癌の報告を行って以降,これまで多くの報告がなされてきた1)。UC関連大腸癌は罹患年数が長くなるにつれ発生リスクが上がるとされ,2001年Eadenらの報告では,浸潤癌の累積発生率は10年で1.8%,20年で8.3%,30年で18.4%であることが示された2)。一方近年では,英国Choiらの報告にて10年で0.1%,20年で2.9%,30年で6.7%とされ,罹患年数に伴う累積発生率は低い値を示している3)(図1)。本邦ではKishikawaらの報告によると,浸潤癌の累積発生率は10年で0.7%,20年で3.2%,30年で5.2%でありChoiらの結果同様であったが,一方でdysplasiaも含めた腫瘍性病変の累積発生率は10年で3.3%,20年で12.1%,30年で21.8%であり,依然長期経過での発生率は高く注意すべき問題である4)(図2)。また炎症の範囲が広いほど発癌リスクが上がることも知られており,Ekbomらの報告によると一般集団と比較した大腸癌発生の相対危険度は,直腸炎型では1.7倍,左側大腸炎型では2.8倍,全大腸炎型では14.8倍であり,広範囲の炎症を伴う場合にも注意を要する5)。
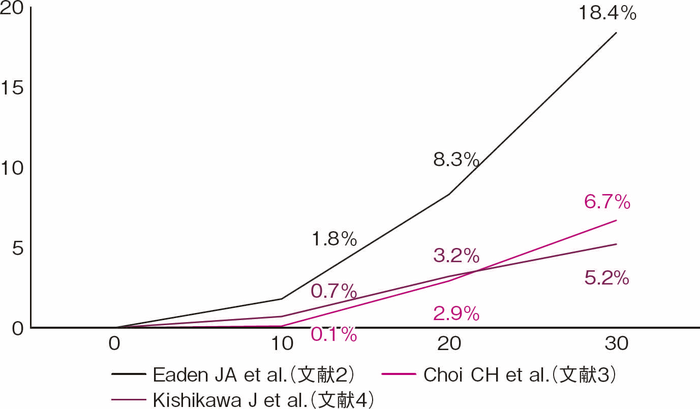
図1 大腸浸潤癌累積発生率
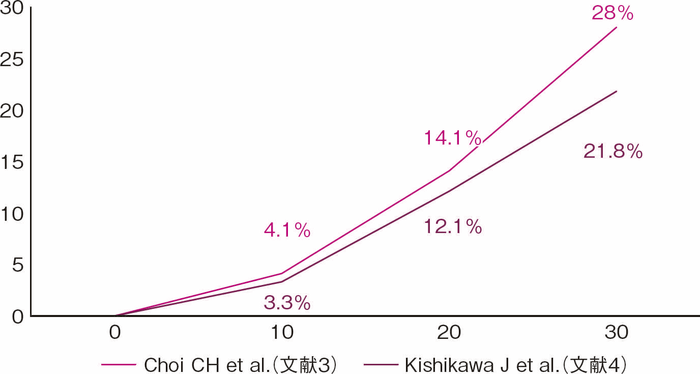
図2 大腸腫瘍累積発生率
-
リスク因子
UC関連大腸腫瘍発生のリスク因子としては前述のように罹患年数や罹患範囲に加え,炎症の程度(中等度から重症),PSC合併,5年以内のdysplasia既往,若年(50歳未満)発症の大腸癌家族歴,狭窄病変などが知られており,リスク因子を有する症例に対しては毎年のサーベイランス大腸内視鏡検査を含めた慎重な経過観察が必要と考えられている6)。特にPSC合併例では発症早期でも大腸癌合併の可能性が高いことが知られており診断時にサーベイランスを開始することが推奨される。 -
特徴
UC関連大腸腫瘍の特徴としては,散発性大腸癌と比較して境界不明瞭な肉眼形態や腫瘍の多発傾向があることが知られている。肉眼的に境界不明瞭で背景粘膜の炎症も相まって発見や範囲診断に難渋することも少なくない。またUC関連大腸腫瘍は平坦な病変であっても上皮性変化に乏しく,深部にびまん性に腫瘍が浸潤することもあるという特徴がある。その発癌様式も散発性大腸癌と異なり,慢性炎症に伴う酸化ストレスなどにより粘膜のDNA損傷が生じ,TP53変異をはじめとするさまざまなゲノム異常やエピゲノム異常が蓄積されることで,前癌病変であるdysplasiaを経て発癌に至る“dysplasia-carcinoma sequence”が知られている7)。また生検組織にdysplasiaが認められた場合にはすでに他の部位に癌が発生しているか,短期間に癌化するリスクも高いことが古くから知られており8),癌診断のマーカーとして前癌病変であるdysplasiaをいかに早期に発見できるかが大腸癌の早期診断のために重要である。
文献
- Crohn BB, Rosenberg H:The sigmoidoscopic picture of chronic ulcerative colitis(non-specific). Am J Med Sci 1925;170:220-228
- Eaden JA, Abrams KR, Mayberry JF:The risk of colorectal cancer in ulcerative colitis:a meta-analysis. Gut 2001;48:526-535
- Choi CH, Rutter MD, Askari A, et al.:Forty-Year Analysis of Colonoscopic Surveillance Program for Neoplasia in Ulcerative Colitis:An Updated Overview. Am J Gastroenterol 2015;110:1022-1034
- Kishikawa J, Hata K, Kazama S, et al.:Results of a 36-year surveillance program for ulcerative colitis-associated neoplasia in the Japanese population. Dig Endosc 2018;30:236-244
- Ekbom A, Helmick C, Zack M, et al.:Ulcerative colitis and colorectal cancer. A population-based study. N Engl J Med 1990;323:1228-1233
- Maaser C, Sturm A, Vavricka SR, et al.:ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 1:Initial diagnosis, monitoring of known IBD, detection of complications. J Crohns Colitis 2019;13:144-164
- Ullman TA, Itzkowitz SH:Intestinal inflammation and cancer. Gastroenterology 2011;140:1807-1816
- Morson BC, Pang LS:Rectal biopsy as an aid to cancer control in ulcerative colitis. Gut 1967;8:423-434
2 サーベイランス
● ポイント
- サーベイランスで発見された腫瘍病変は有症状により発見された腫瘍病変より予後がよいことをふまえ,定期的に内視鏡検査によるサーベイランスを行うことが重要である。
- サーベイランスは診断後8年経過した全大腸炎型,左側大腸炎型の症例を対象とし,リスクによりサーベイランス施行の間隔を計画する。
- サーベイランスの方法としては狙撃生検とランダム生検があり,検出能が同等であることより狙撃生検が推奨されるが,ランダム生検にて検出される腫瘍病変もあり,患者の背景などによりその適応を検討する。
- 色素内視鏡検査は病変の局在診断,境界,肉眼形態などが明確になる点は有用な検査法であるが,高画素内視鏡に対する病変検出能の優越性は示されていない。
- 画像強調内視鏡によるサーベイランスの有用性に関する報告がなされているが,比較した対照群が均一した検査法でないことより,今後の研究の集積が待たれる。
● 解説
-
サーベイランスの重要性
近年UCの疾患活動性を評価する方法としてカルプロテクチンや便潜血定量検査,腸管エコー検査などの非侵襲的な検査法の有用性が報告されているが,UC関連大腸腫瘍の標準的なサーベイランス方法は大腸内視鏡検査である。これまでの報告で切除可能な段階で発見された病変の予後は比較的よいこと1,2),またサーベイランス大腸内視鏡検査で発見された腫瘍病変は有症状により発見された腫瘍病変より早期癌の割合が高く,死亡率が低いことがメタアナリシスにより確認されており3),UC関連大腸腫瘍を早期に発見,診断していくうえで内視鏡検査によるサーベイランスは重要である。その対象,方法についてはガイドラインにより推奨されており,次項以降で概説する。 -
サーベイランスの対象と施行時期
サーベイランスの開始時期については,多くのガイドラインでは診断後,もしくはUCの症状が出現してから8年経過した全大腸炎型,左側大腸炎型(直腸炎型以外)の症例を対象とするとされている4-7)。しかし罹病期間が短い症例においても大腸癌が検出されることもあり,注意が必要である。また炎症がある場合には病変の存在診断が困難であり,原則として寛解期にサーベイランスを行うべきである。
サーベイランスの対象を考慮するうえで,リスク因子を把握することは重要である。通常の大腸癌のリスク因子は加齢,男性,家族歴,肥満,喫煙,赤身の肉(read meat)摂取などであるが,UC関連大腸腫瘍のリスク因子としては,PSC,全大腸炎型,長期経過例,内視鏡的・組織学的炎症の持続などが挙げられている8)。本邦では難病申請の更新時の書類作成のために大腸内視鏡検査を行う傾向があったため,リスクにかかわらず毎年検査を施行する場合も少なからずあるが,海外のガイドラインでは,リスク因子別にサーベイランスの施行間隔が記載されている(表5)。
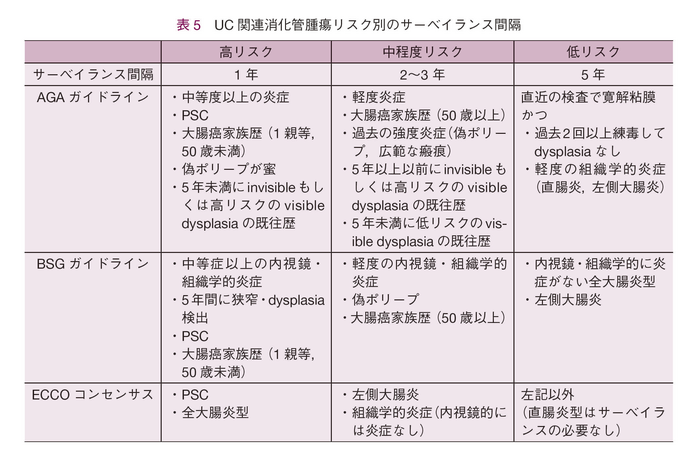
高リスク群としては活動性の強い全大腸炎型,50歳以下の大腸癌の家族歴がある場合,PSC,5年以内にdysplasia(HGD or LGD)の検出の既往が挙げられており,これらのリスクがある場合にはサーベイランスを毎年行うことが推奨されている。中程度リスク(Intermediate)群としては,50歳以下の大腸癌の家族歴がある場合,軽度の内視鏡的・組織学的炎症の持続などが挙げられており,2~3年ごとのサーベイランスが推奨されている。低リスク群は5年おきのサーベイランスが推奨されており,内視鏡的・組織学的炎症のない全大腸炎型や左側大腸炎型5),2回以上dysplasiaがないもしくは組織学的活動性がなく,かつ直近の検査で内視鏡的寛解が確認されている場合をあげている4)。また内視鏡所見からみた大腸癌発症のリスク因子についても研究がなされており,内視鏡的寛解例は発症のリスクを低下させること,一方で炎症性ポリープ,管腔の狭小化はリスクを増加することが報告されており9),慢性に炎症が持続すること,過去に強度の炎症を有することにより炎症を母地とした発癌のリスクが高まると考えられている。
上記の通りガイドラインにおいてリスク別に施行間隔が推奨されているにもかかわらず,中程度リスク群の34%,高リスク群の39%が推奨通りの間隔でサーベイランスが行われていないことが報告されており10),リスクの高い症例に対するサーベイランスの必要性を啓蒙するプログラムなどが必要であると考えられる。
-
ランダム生検と狙撃生検によるサーベイランス
UC関連大腸腫瘍の肉眼的特徴として,偶発的に発生する散発性腫瘍病変に比して平坦型の割合が多く,病変の境界が不明瞭であることが多いことが報告されている2,11)。したがって内視鏡検査による通常観察では腫瘍病変を検出することが容易ではないと考えられており,ランダム生検すなわち10 cmおきに4個ずつ(最低33個以上)生検を行うことが推奨されてきた。一方で本邦においてランダム生検と狙撃生検を比較する腫瘍病変検出率を検討した多施設共同ランダム化比較試験が行われ,ランダム生検群で腫瘍病変が検出された患者の割合は9.3%,狙撃生検群では11.4%であり,両群の検出率が同等であり,かつ生検数は狙撃生検群で有意に少ないことが示された12)。したがって炎症が安定している症例では狙撃生検が推奨される。一方でランダム生検により腫瘍検出率が15%上昇すること13)やランダム生検でなければ検出困難と思われる病変が存在することも報告されている14)。以上より患者の病歴や内視鏡所見,内視鏡医の技量などを参考に,ランダム生検の施行を検討することも本ガイドラインのステートメントに記載されている(CQ 8)。
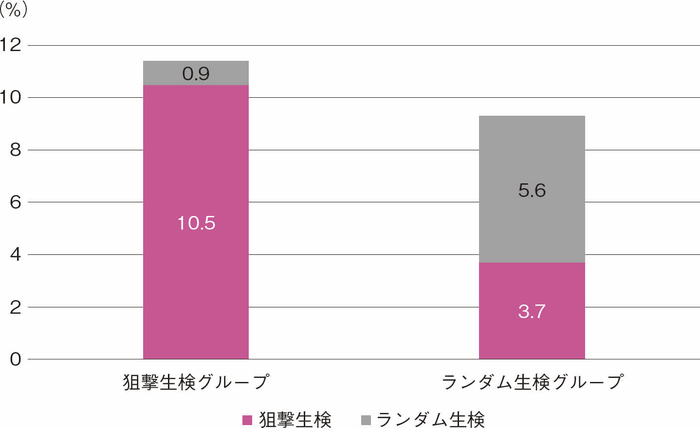
図3 RCTによる狙撃生検とランダム生検によるdysplasia検出能(各グループの検出率)
-
色素内視鏡検査の有用性
サーベイランスにおいて,色素散布を行うことにより病変の局在診断,境界,肉眼形態などがより明確になり腫瘍病変の検出に有用であると考えられている。色素内視鏡検査はインジゴカルミンやメチレンブルーを用いる方法が行われている。 SCENIC(Surveillance for Colorectal Endoscopic Neoplasia Detection and Management in Inflammatory Bowel Disease Patients:International Consensus Recommendations)ガイドラインでは特に標準画質(standard definition)内視鏡において色素併用内視鏡の併用が強く推奨されている15)。高画素内視鏡(high definition)では,色素併用は非使用例に比して腫瘍病変の検出率が高い報告例がある一方で16,17),メタアナリシス18,19)において高画素内視鏡では,色素散布併用は病変検出率の向上につながらないという結果が報告されている。また色素内視鏡併用高画素内視鏡とランダム生検併用高画素内視鏡検査では,色素散布併用した狙撃生検群では生検数が少なくて済むものの,腫瘍検出率には有意差がないことが示されている20)。色素散布による観察は検査時間に時間を要する欠点はあるものの,病変の境界や形態をより明確にし,症例によっては病変の検出に寄与する可能性があることや,さらには内視鏡切除の適応を検討する上でも有用な検査方法であると考えられる。 -
画像強調内視鏡によるサーベイランス
内視鏡診断に関しては別項で解説があるため,本項ではサーベイランスに関する内容を概説する。画像強調内視鏡は色素散布を行わないで腫瘍病変を検出することが可能であるが,近年NBI,FICE,iSCAN(以下画像強調内視鏡)と高画素内視鏡もしくは色素併用通常画質内視鏡との病変検出を比較したメタアナリシス(11研究)が行われ,画像強調内視鏡の有用性は確認されなかった21)。また通常光観察,色素併用観察,NBI観察の3つを直接比較したランダム化比較試験はないが,Gondalらはネットワークメタアナリシスを行い,高画素内視鏡においては,3つの病変検出能には明らかな差がないことを示している22)。しかし画像強調内視鏡を用いたサーベイランスに関する研究は多くない点や比較した対照群が均一した検査法でないことより,今後の研究の集積が待たれる。
文献
- Choi CH, Rutter MD, Askari A, et al.:Forty-Year Analysis of Colonoscopic Surveillance Program for Neoplasia in Ulcerative Colitis:An Updated Overview. Am J Gastroenterol 2015;110:1022-1034
- Mutaguchi M, Naganuma M, Sugimoto S, et al.:Difference in the clinical characteristic and prognosis of colitis-associated cancer and sporadic neoplasia in ulcerative colitis patients. Dig Liver Dis 2019;51:1257-1264
- Bye W, Ma C, Nguyen T, et al.:Strategies for Detecting Colorectal Cancer in Patients with Inflammatory Bowel Disease:A Cochrane Systematic Review and Meta-Analysis. Am J Gastroenterol 2018;113:1801-1809
- Beaugerie, Itzkowitz SH:Cancers complicating inflammatory bowel disease. N Engl J Med 2015;372:1441-1452
- Rubin DT, Ananthakrishnan AN, Siegel CA, et al.:ACG Clinical Guideline:Ulcerative Colitis in Adults. Am J Gastroenterol 2019;114:384-413
- Lamb CA, Kennedy NA, Raine T, et al.:British Society of Gastroenterology Consensus Guidelines on the Management of Inflammatory Bowel Disease in Adults. Gut 2019;68(Suppl 3):s1-s106
- Magro F, Gionchetti P, Eliakim R, et al.:Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1:Difinition, Diagnosis, extra-intestinal manifestations, pregnancy, cancer surveillance, surgery, and ileo-anal pouch disorders. J Crohns Colitis 2017;11:648-670
- Matsuoka K, Kobayashi T, Ueno F, et al.:Evidence-based clinical practice guidelines for inflammatory bowel disease. J Gastroenterol 2018;53:305-353
- Rutter MD:Cancer surveillance in longstanding ulcerative colitis:endoscopic appearances help predict cancer risk. Gut 2004;53:1813-1816
- Ballester MP, Mesonero F, Florez-Diez P, et al.:Adherence to endoscopic surveillance for advanced lesions and colorectal cancer in inflammatory bowel disease:An AEG and GETECCU collaborative cohort study. Aliment Pharm 2022;55:1402-1413
- Sugimoto S, Naganuma M, Iwao Y et al.:Endoscopic morphological features of ulcerative colitis-associated dysplasia classified according to the SCENIC consensus statement. Gastrointest Endosc 2017;85:639-646
- Watanabe T, Ajioka Y, Mitsuyama K, et al.:Comparison of Targeted vs Random Biopsies for Surveillance of Ulcerative Colitis-Associated Colorectal Cancer. Gastroenterology 2016;151:1122-1130
- Moussata D, Allez M, Cazals-Hatem D, et al.:Are random biopsies still useful for the detection of neoplasia in patients with IBD undergoing surveillance colonoscopy with chromoendoscopy? Gut 2018;67:616-624
- Hata K, Anzai H, Ikeuchi H, et al. Surveillance colonoscopy for ulcerative colitis-associated colorectal cancer offers better overall survival in real-world surgically resected cases. Am J Gastroenterol 2019;114:483-489
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastrointest Endosc 2015;81:489-501.e26
- Har-Noy O, Katz L, Avni T, et al.:Chromoendoscopy, Narrow-Band Imaging or White Light Endoscopy for Neoplasia Detection in Inflammatory Bowel Diseases. Dig Dis Sci 2017;62:2982-2990
- Alexandersson B, Hamad Y, Andreasson A, et al.:High-Definition Chromoendoscopy Superior to High-Definition White-Light Endoscopy in Surveillance of Inflammatory Bowel Diseases in a Randomized Trial. Clin Gastroenterol Hepatol 2020;18:2101-2107
- Feuerstein JD, Rakowsky S, Sattler L, et al.:Meta-analysis of dye-based chromoendoscopy compared with standard- and high-definition white-light endoscopy in patients with inflammatory bowel disease at increased risk of colon cancer. Gastrointest Endosc 2019;90:186-195
- Resende RH, Ribeiro IB, de Moura DTH, et al.:Surveillance in inflammatory bowel disease:is chromoendoscopy the only way to go? A systematic review and meta-analysis of randomized clinical trials. Endosc Int Open 2020;8:E578-E590
- Yang, DH, Park SJ, Kim HS, et al.:High-Definition Chromoendoscopy Versus High-Definition White Light Colonoscopy for Neoplasia Surveillance in Ulcerative Colitis:A Randomized Controlled Trial. Am J Gastroenterol 2019;114:1642-1648
- El Dallal M, Chen Y, Lin Q, et al.:Meta-analysis of Virtual-based Chromoendoscopy Compared with Dye-spraying Chromoendoscopy Standard and High-definition White Light Endoscopy in Patients with Inflammatory Bowel Disease at Increased Risk of Colon Cancer. Inflamm Bowel Dis 2020;26:1319-1329
- Gondal B, Haider H, Komaki Y, et al.:Efficacy of various endoscopic modalities in detecting dysplasia in ulcerative colitis:A systematic review and network meta-analysis. World J Gastrointest Endosc 2020;12:159-171
3 診 断
1)内視鏡診断
● ポイント
- UC関連大腸腫瘍においては,その存在診断だけでなく,病変を認めた際の範囲,質的(腫瘍・非腫瘍,異型度)および深達度診断は,通常の上皮性腫瘍と比べ困難である。
- 内視鏡診断は,炎症の寛解期にインジゴカルミンを用いた色素内視鏡検査や画像強調内視鏡観察が推奨される。
- UC関連大腸腫瘍の内視鏡診断基準は未確立であり,内視鏡検査所見のみならず臨床情報や病理所見も加えて総合的に診断する。
● 解説
- UC関連大腸腫瘍発生からみた内視鏡診断の困難性
UC関連大腸癌の発癌経路は,通常の大腸癌におけるadenoma-carcinoma sequenceとは異なり,dysplasiaが癌の前駆病変とされるdysplasia-carcinoma sequence1)を辿ることから,長期経過中にdysplasiaの早期発見,正確な診断および適切な治療選択が,腸管温存を含めた予後において重要である。大腸内視鏡検査は,通常の上皮性腫瘍と同様にUC関連大腸腫瘍に対して最も正確な画像診断である。一方で,慢性炎症を背景に発生するUC関連大腸腫瘍は通常の上皮性腫瘍性病変と異なり,細胞増殖帯が粘膜中層~深層に存在することが多く,表層に向かって細胞分化する傾向にある。すなわち,腫瘍の発育形式は腺管底部から表層に向けたbottom-upを呈するために2),UC関連大腸腫瘍初期病変を病変表面から診断することは容易ではない。辺縁が不明瞭な平坦型を呈することが多いなど通常の上皮性腫瘍とは異なることから内視鏡診断の困難性が伺える。浸潤癌においては,低分化癌や粘液癌の頻度が通常よりも高いことも特徴的であり3),通常の浸潤癌と異なる肉眼型を呈することが多い。以上の特徴を十分に認識して内視鏡診断を行うことが肝要である。 - 内視鏡診断の手順
UCの活動期には,生検による病理診断において腫瘍性変化と炎症や再生異型との鑑別診断は困難であり,内視鏡診断においても炎症による修飾のため活動期に正確な内視鏡診断を行うことは困難である。UC診療における治療目標は内視鏡的寛解であるが,適切なサーベイランス内視鏡検査および発見病変への内視鏡診断のためにも炎症の寛解導入・維持を目指すべきである。UC関連大腸腫瘍の内視鏡診断は,その難易度が高く,複数の内視鏡modalityを用いて段階的に進めることが求められる。白色光,非拡大画像強調(NBIやBLI),拡大画像強調観察にて診断を進める。インジゴカルミンによる病変の性状を非拡大で病変範囲や凹凸を観察し,画像強調およびクリスタルバイオレット注)を用いた色素併用拡大観察で診断を絞り込む。 - 白色光および色素内視鏡検査による診断(形態的特徴)
UC関連大腸腫瘍の形態的特徴として,隆起型,表面型,複合型(分類不能)とさまざまな形態を呈する。SCENIC(Surveillance for Colorectal Endoscopic Neoplasia Detection and Management in Inflammatory Bowel Disease Patients:International Consensus Recommendations)4)では,ⅰ)polypoid dysplasia(pedunculated,sessile),ⅱ)nonpolypoid dysplasia(superficial elevated,flat,depressed)のいずれかに潰瘍の有無や病変の境界の明瞭さを付記する肉眼型分類を提唱しているが,このような肉眼型分類に当てはまらない病変が多く存在する。
通常の上皮性腫瘍に多く認められる有茎性や亜有茎性のような隆起型病変は稀であり,頻度的には辺縁や立ち上がりが不明瞭な顆粒状隆起で,絨毛状の表面構造を呈することが多い5)。表面平坦および陥凹型のHGDは,領域のある発赤調を呈する6,7)。インジゴカルミン散布後に表面構造(粘膜模様)や色調変化を慎重に観察することで肉眼型,領域が明瞭化となるため,色素内視鏡検査を併用することが推奨される5)。一方で,色素内視鏡検査を併用しても,腫瘍と非腫瘍の境界を判定することが困難な症例もあり,範囲診断には生検による病理診断を併用することが望まれる。 - 拡大内視鏡検査による診断
画像強調内視検査にて微小血管や表面構造を観察することで,白色光観察よりも病変辺縁が明瞭化されることがあり,さらには拡大観察を併用することが推奨される。これまでUC関連大腸腫瘍の腫瘍・非腫瘍の鑑別や異型度の診断における拡大併用画像強調内視鏡検査の有用性が検討されており,表面微細構造が有用であるという報告8,9)や通常の上皮性腫瘍の質的診断に用いられるJNET(The Japan NBI Expert Team)10)の応用11)について報告されてきた。しかし,その診断精度の検討は十分でなく,微小血管や表面構造の不整とUC関連大腸腫瘍の異型度が相関するという研究結果は十分とはいえない。
拡大内視鏡検査を用いたpit pattern診断に関する検討が国内外から報告されており7,12,13),厚生労働省研究班の合同班会議でUC関連大腸腫瘍におけるpit pattern分類としてのNPUC分類14)が提唱されたが,広い普及までには至らなかった。病変周囲の非腫瘍性再生上皮と腺腫性pit patternが酷似していることも多く,従来の上皮性腫瘍に用いられている工藤・鶴田分類をUC関連大腸腫瘍に対する腫瘍・非腫瘍の鑑別にそのまま当てはめることには限界があると考えられる7,15)。また,異型度の診断においても同様で,癌であった場合の深達度診断は,特異度は極めて高いものの,感度は低いとされている。しかし,pit patternのみならず,その領域性を加味することでUC関連大腸腫瘍の診断の絞り込みが可能であると考えられている(図4)。さらには,内視鏡検査所見に加えて,臨床情報や生検による病理組織学的(Ki-67やp53の免疫染色を含む)所見も加えて総合的に診断することが現時点では推奨される。
近年,超拡大内視鏡検査によるUC関連大腸腫瘍の診断の有用性が報告されている16)。UC関連大腸腫瘍における構造異型および細胞異型の診断の困難性は,超拡大内視鏡検査においても同様であり,今後のさらなる研究成果の報告が待たれる。 - UC関連大腸腫瘍における内視鏡診断の展望
UC関連大腸腫瘍に特化した内視鏡分類を開発する研究グループ(NAVIGATOR Study 2 Group)が国内専門家によって発足しており,診断アルゴリズムの確立を含めた検討がなされている14)。UC関連大腸腫瘍・非腫瘍の鑑別,非UC関連大腸腫瘍との鑑別,UC関連大腸腫瘍の異型度や癌の深達度診断,内視鏡的粘膜下層剝離術(ESD)をはじめとする診断的治療を目的とした内視鏡切除の適応にも関連する内視鏡診断基準の確立が望まれる。
注:日本消化器内視鏡学会からの声明17)
『ピオクタニン(クリスタルバイオレット)の臨床使用に際しては,従来から注意喚起されているように,その安全性については現在のところ確立されていない。したがって,その使用による患者(被験者)の利益が不利益をうわまわると判断される場合にのみ,施行医および施設の責任のもと,必要最小量の使用にとどめることが望ましい。』
サイドメモ
■SCENIC(Surveillance for Colorectal Endoscopic Neoplasia Detection and Management in Inflammatory Bowel Disease Patients:International Consensus Recommendations)
2015年に米国消化器病学会と同消化器内視鏡学会から合同で発刊されたSCENIC4)は,炎症性腸疾患関連腫瘍の診断・治療について現時点で最も重要視されている国際的コンセンサスである。サーベイランス内視鏡検査の方法,発見されたdysplasiaの取り扱いについて言及されている。これまでのdysplasia-associated lesion or mass(DALM)やadenoma-likeは用いず,Pari分類を基本として潰瘍の有無や病変境界の形態用語を統一したこと,内視鏡切除の適応病変と考えられる“endoscopically resectable”の使用が推奨されている。
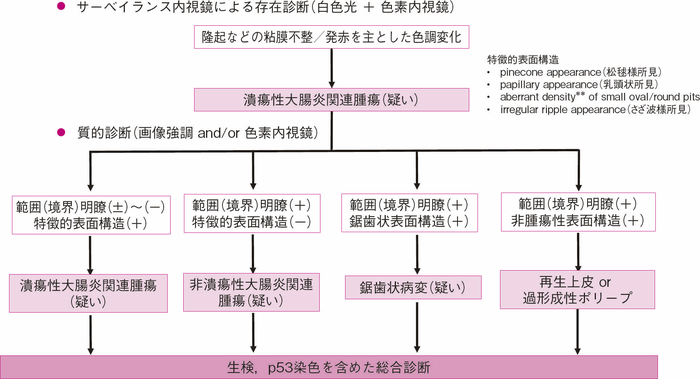
図4 UC関連大腸腫瘍 診断アルゴリズム
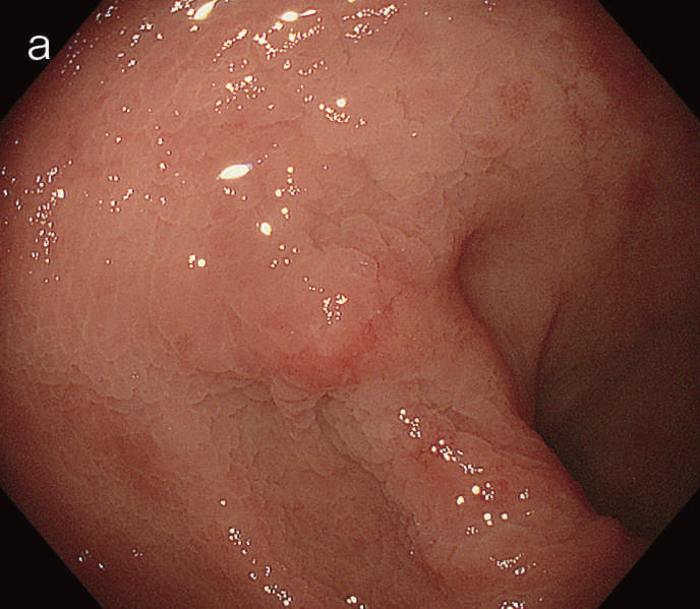
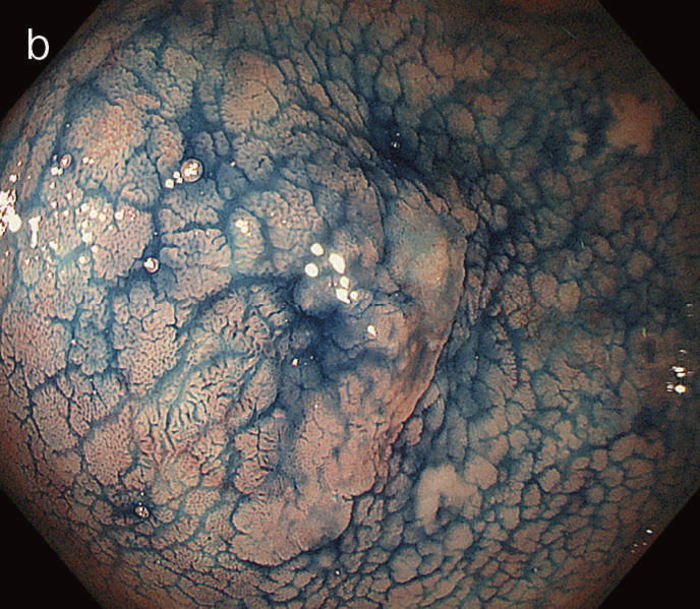
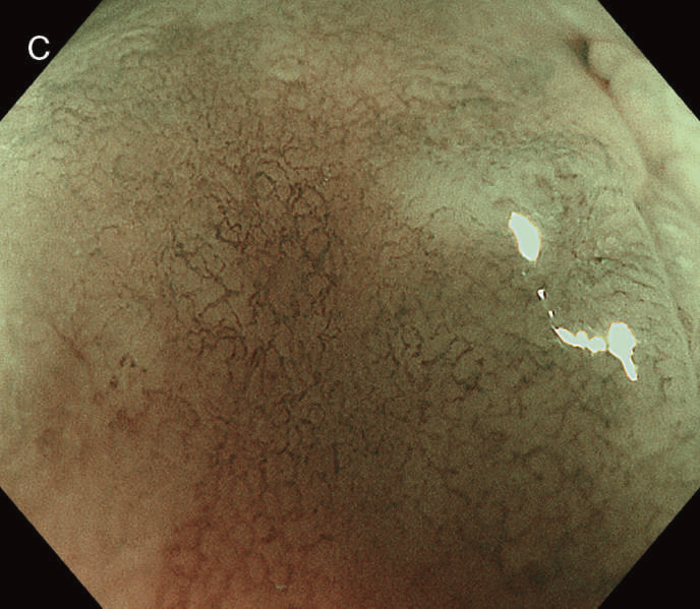
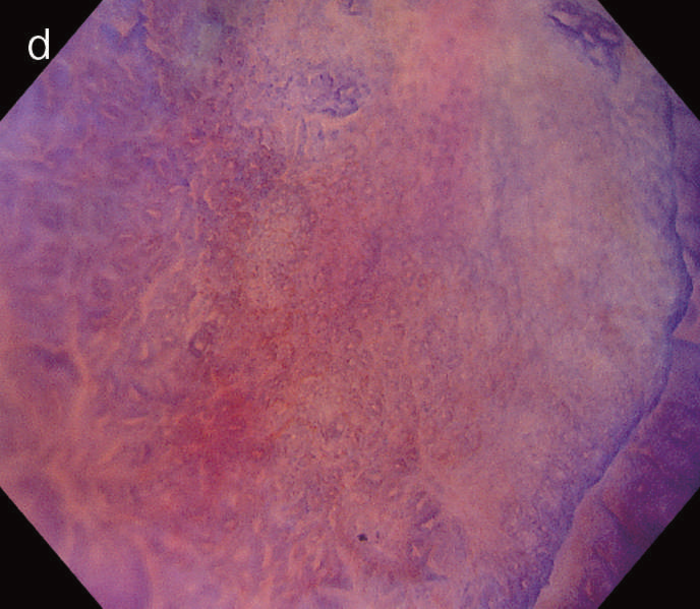
図5 UC関連粘膜下層浸潤癌の内視鏡所見
- 白色光像:直腸(直腸S状部)の発赤調変化。背景粘膜は寛解期にあった。
- 色素内視鏡像:病変辺縁が明瞭となるが,病変肛門側で不明瞭であった。
- NBI拡大像:口径不同,不均一な微小血管と不整な表面構造所見を認めた。
- pit pattern像:小型の類円形,管状pitを認めた。
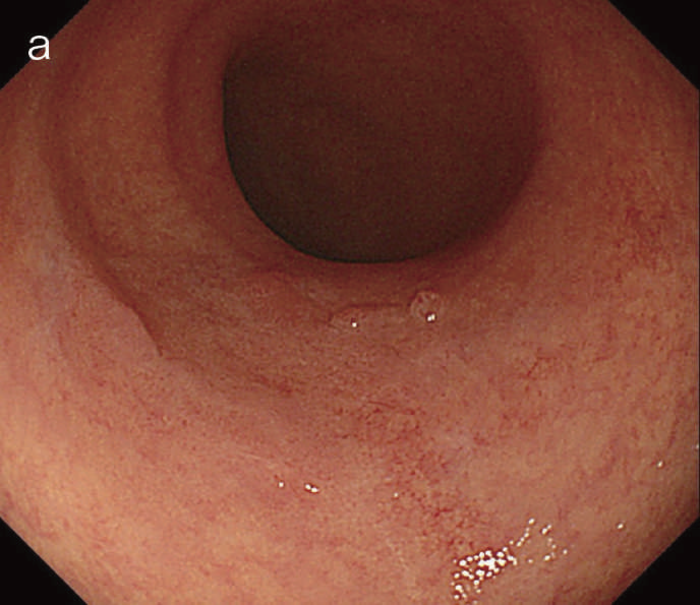
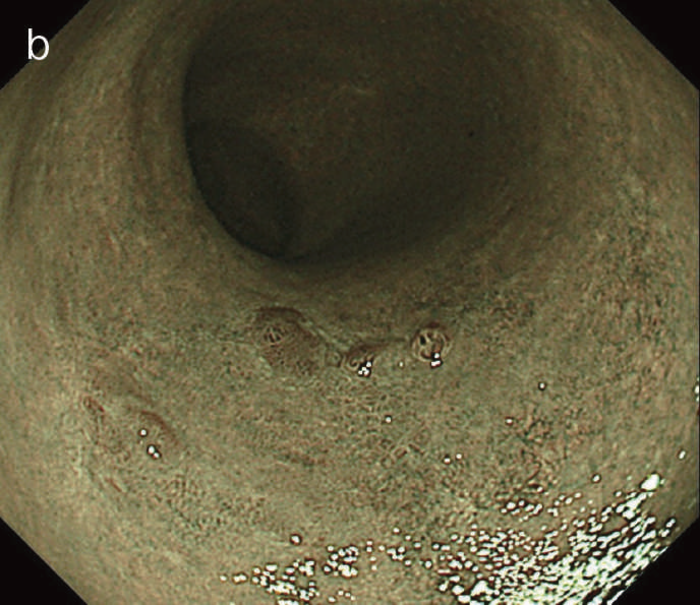
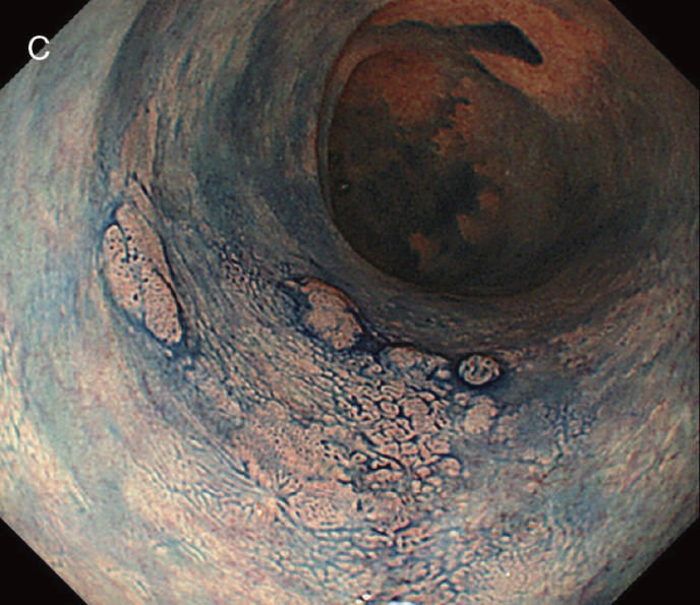
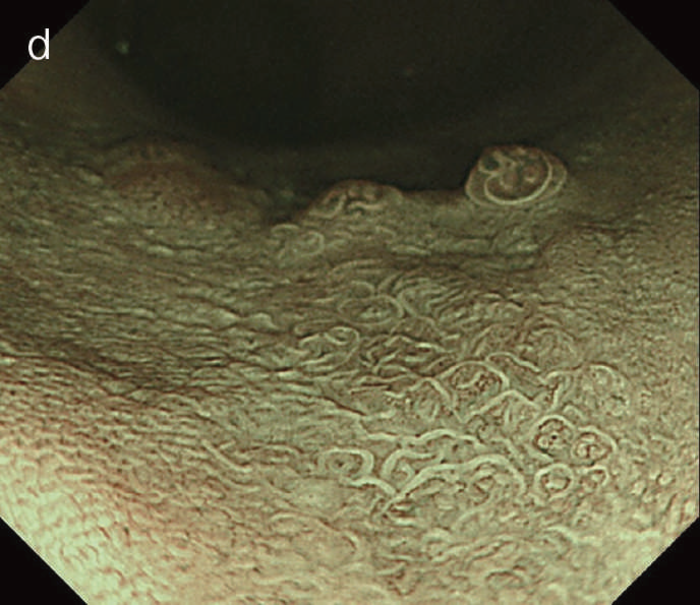
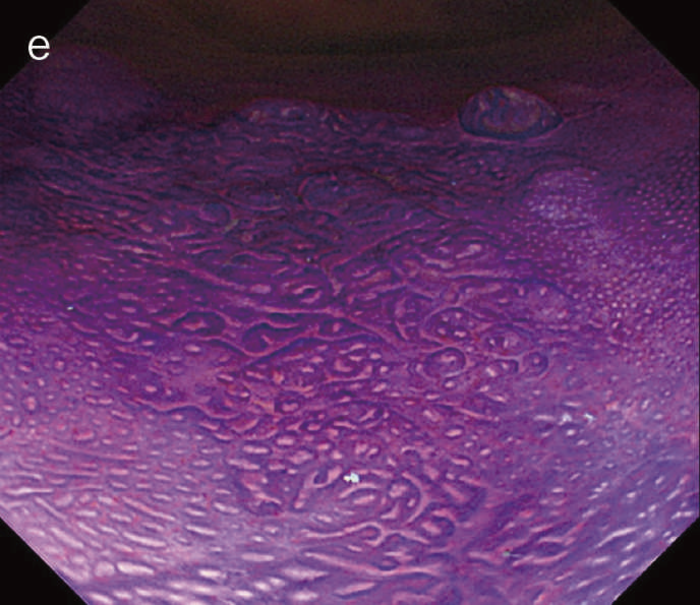
図6 UC関連LGDの内視鏡所見
- 白色光像:直腸(下部直腸)に色調変化は乏しく,微小な隆起を複数認めた。背景粘膜は寛解期にあった。
- NBI非拡大像:Brownishな領域が明らかとなった。
- 色素内視鏡像:病変辺縁が明瞭な微小な隆起を複数伴う表面平坦型病変。
- NBI拡大像:口径整でらせん状の微小血管と絨毛状の表面構造を認めた。
- pit pattern像:小型の類円形,管状pitを認めた。
文献
- Ullman TA, Itzkowiz SH:Intestinal inflammation and cancer. Gastroenterology 2011;140:1807-1816
- 味岡洋一:潰瘍性大腸炎におけるcolitis-associated cancer(炎症性発癌)早期病変の病理診断―現状と問題点―.日消誌2020;117:957-964
- 味岡洋一,佐野知江:潰瘍性大腸炎における大腸癌の病理組織学的特徴と生検診断.日消誌2013;110:379-384
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology 2015;148:639-651.e28
- Sugimoto S, Naganuma M, Iwao Y, et al.:Endoscopic morphological features of ulcerative colitis-associated dysplasia classified according to the SCENIC consensus statement. Gastrointest Endosc 2017;85:639-646
- Matsumoto T, Iwao Y, Igarashi M, et al.:Endoscopic and chromoendoscopic atlas featuring dysplastic lesions in surveillance colonoscopy for patients with long-standing ulcerative colitis. Inflamm Bowel Dis 2008;14:259-264
- 岩男 泰,長沼 誠,下田将之,他:拡大内視鏡による潰瘍性大腸炎関連腫瘍診断の現状と課題―初期病変を中心に.胃と腸2020;55:142-149
- Matsumoto T, Kudo T, Jo Y, et al.:Magnifying colonoscopy with narrow band imaging system for the diagnosis of dysplasia in ulcerative colitis:a pilot study. Gastrointest Endosc 2007;66:957-965
- Nishiyama S, Oka S, Tanaka S, et al. Clinical usefulness of narrow band imaging magnifying colonoscopy for assessing ulcerative colitis-associated cancer/dysplasia. Endosc Int Open 2016;4:E1183-E1187
- Sano Y, Tanaka S, Kudo SE, et al.:Narrow-band imaging(NBI)magnifying endoscopic classification of colorectal tumors proposed by the Japan NBI Expert Team. Dig Endosc 2016;28:526-533
- Kawasaki K, Nakamura S, Esaki M, et al.:Clinical usefulness of magnifying colonoscopy for the diagnosis of ulcerative colitis-associated neoplasia. Dig Endosc 2019;31 Suppl 1:36-42
- Hata K, Watanabe T, Motoi T, et al.:Pitfalls of pit pattern diagnosis in ulcerative colitis-associated dysplasia. Gastroenterology 2004;126:374-376
- Bisschops R, Bessissow T, Dekker E, et al.:Pit pattern analysis with high-definition chromoendoscopy and narrow-band imaging for optical diagnosis of dysplasia in patients with ulcerative colitis. Gastrointest Endosc 2017;86:1100-1106.e1
- 渡辺憲治,樋田信幸,岡 志郎,他:UC関連大腸腫瘍の内視鏡所見分類に関する多施設共同研究(NAVIGATOR Study 2)の紹介.胃と腸2020;55:208-211
- 工藤進英,日比紀文,松本譽之,他:炎症性腸疾患の拡大内視鏡診断―dysplasia,癌のNPUC所見.早期大腸癌2006;10:255-258
- Kudo SE, Maeda Y, Ogata N, et al.:Combined endocytoscopy with pit pattern diagnosis in ulcerative colitis-associated neoplasia:Pilot study. Dig Endosc 2022;34:133-143
- 日本消化器内視鏡学会:「消化器内視鏡検査におけるクリスタルバイオレットの使用に関する学会声明」https://www.jges.net/news/news-official/2019/12/12/25311
2)病理診断
● ポイント
- UC関連進行大腸癌の肉眼像は潰瘍浸潤型(3型),びまん浸潤型(4型)や分類不能型(5型)が多い。同初期病変の多くは隆起型,平坦型,あるいはその混合型であり,平坦型成分はdysplasiaの特徴といえる。
- Dysplasiaはその異型度によりLGDとHGDに二分される。また,粘膜内脱分化,表層への細胞分化,細胞の分化異常,疎な腺管密度,粘膜全層置換,分岐の少ないストレートな腺管,周囲粘膜とのなだらかな移行,平坦な肉眼形態,bottom-up patternの細胞増殖動態,p53蛋白発現異常を特徴とし,粘膜下層以深浸潤癌では散発性腫瘍に比べ,粘液癌,低分化腺癌,印環細胞癌などの頻度が高い。
- UC関連大腸腫瘍の生検診断には,Riddell systemや厚生省(現厚生労働省)難治性炎症性腸管障害調査研究班によるUCにおける異型上皮に関する診断基準が用いられている。本ガイドラインでは,Riddell systemで定義されたdysplasiaの概念を採用している。
- 本邦で広く受け入れられている非浸潤癌(上皮内癌)の概念も日常的に用いられているので,dysplasiaのうち,組織学的異型度を指標とする日本の病理診断基準で癌と診断されるものは,非浸潤性であってもUC関連粘膜内癌と呼ぶ。
● 解説
- 肉眼的特徴
通常の散発性進行大腸癌の多くは潰瘍限局型(2型)であるが,UC関連進行大腸癌は潰瘍浸潤型(3型),びまん浸潤型(4型)や分類不能型(5型)が多いとされる(図7)。初期病変であるdysplasiaの肉眼形態に関しては,混合型を含む約70%の症例が何らかの隆起成分を有することが報告されている1,2)。ただ同じ隆起といっても,UC関連大腸腫瘍の多くは境界不明瞭な丈の低い顆粒状・結節状・不整扁平隆起を呈する一方で,散発性腫瘍は有茎性もしくは亜有茎性病変,境界や立ち上がりが明瞭な病変であることが多く,詳細な肉眼形態の観察は両者の鑑別に重要である。二番目に多い肉眼形態は平坦型であり,全体の約30%を占める1,2)。散発性大腸腫瘍の平坦型は極めて頻度が低いことから,平坦型成分の存在もdysplasiaの特徴といえる(図8)。
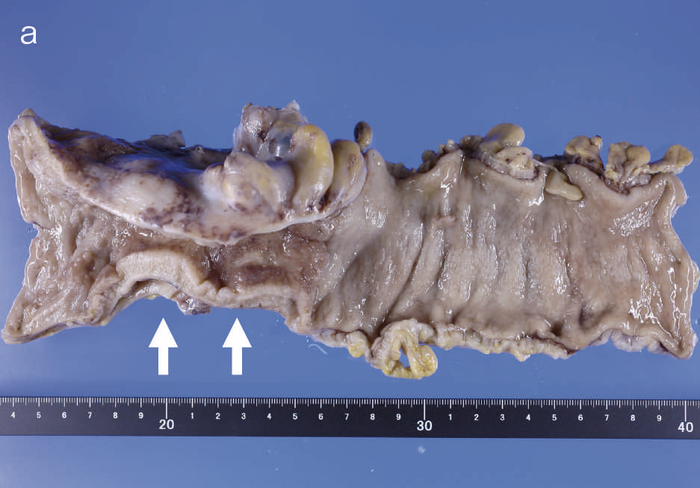
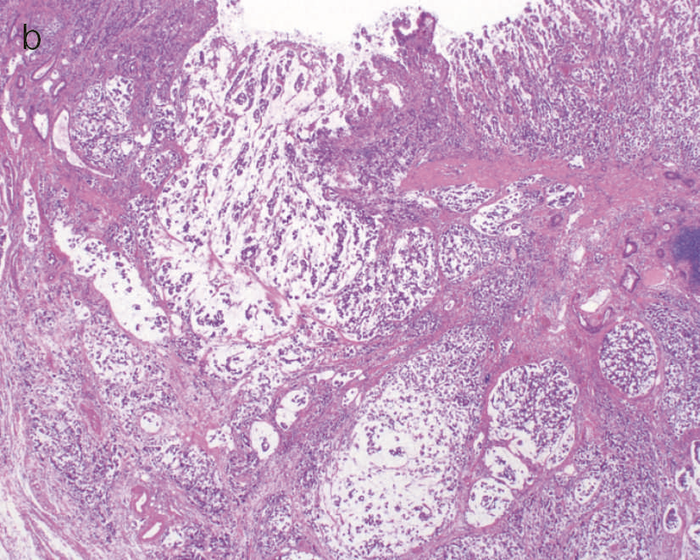
図7 UC関連進行大腸癌の代表的な肉眼像
- 内腔狭窄を伴った5型の腫瘍(矢印)を認める。
- 組織学的には,粘液癌あるいは低分化腺癌が壁内に浸潤している像を認める。
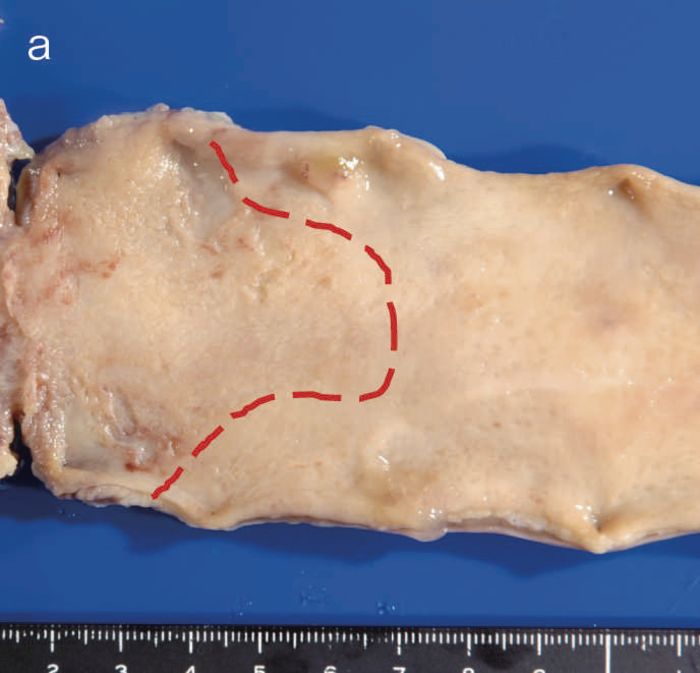
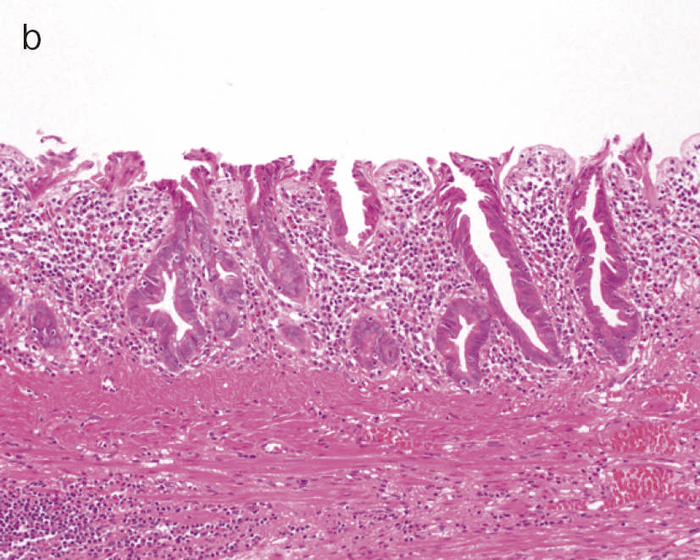
図8 Dysplasiaの代表的な肉眼像(平坦型)
- 直腸部の赤色点線部より肛門側(左側)に拡がるdysplasia(平坦型)を認める。
- 同平坦部では組織学的に高分化管状腺癌(粘膜内癌)を認めた。
- 組織学的特徴
dysplasiaはその異型度によりLGDとHGDに二分される(図9)。LGDは基本的に核の極性が比較的保たれており,表層への分化傾向がみられることを特徴とし,しばしば反応性異型との鑑別を要する。多彩な形態像を示すこともdysplasiaの特徴である。味岡らは,UC関連大腸腫瘍を5つの特殊なパターン(表層分化を示す分化型腺癌,分化細胞を豊富にもつ分化型腺癌,分化細胞に乏しい分化型腺癌,未分化型腺癌または分化型腺癌の脱分化,癌の判定が困難な分化型腫瘍)に分類し報告している3)。2019年に出版されたWHO分類には,IBDを背景に発生する粘膜内腫瘍をInflammatory bowel disease-associated dysplasia of the colorectumと呼称し,組織形態に基づき,intestinal(adenomatous)subtype,serrated subtype,mucinous type,a subtype with eosinophilic cytoplasm and marked goblet cell depletion,crypt cell subtypeやこれらの組織像が混在したmixed subtypeなどが存在すると記載されている4)(図10)。
このように多彩な像を呈するdysplasiaでは,特に異型度が低い場合に反応性異型との鑑別にしばしば難渋するが,dystrophic goblet cell,endocrine cell hyperplasia,Paneth細胞化生などの特徴的な上皮細胞分化異常を示す特殊な異型上皮の存在が形態学的な鑑別として有用である。また,dysplasiaでは,腫瘍発生早期の段階よりTP53遺伝子異常が起こることが知られている。したがって,上記の形態学的な異常とともに,免疫染色におけるp53蛋白異常発現の有無が反応性異型や散発性腺腫との鑑別において重要となる(TP53遺伝子変異が見られる際には,免疫染色においてp53蛋白過剰発現あるいは完全欠失を示すことが知られている)。これまでに,一般大腸腺腫・癌ではp53蛋白過剰発現はその異型度に相関するのに対し(腺腫で0.8~3.4%,低異型度癌で35.3%,高異型度癌で71.7%),dysplasiaでは低異型度の段階から高頻度(75%)にp53蛋白過剰発現を呈することが報告されている5)。したがって,特に低異型度腫瘍でp53蛋白異常発現パターンを示す場合はdysplasiaの可能性が高く,反応性異型との鑑別において診断的意義が高い。また,表層分化傾向を示すLGDではp53蛋白の過剰発現がある場合でも表層部ではp53蛋白の発現減弱がしばしば観察されるのに対し(unique basal patternと呼ばれる),HGDでは全層性にp53蛋白過剰発現を示すことが多い。Ki-67(増殖マーカー)染色では,dysplasiaでは細胞増殖帯が粘膜深層~中層に位置するが(bottom-up pattern),散発性腺腫では細胞増殖帯が腺管表層~中層に分布することが知られている(top-down pattern)。これらの免疫染色パターンは,dysplasiaと反応性異型や散発性腺腫との鑑別の際に重要な手がかりとなる(図9,図11)(CQ 12,CQ 13)。
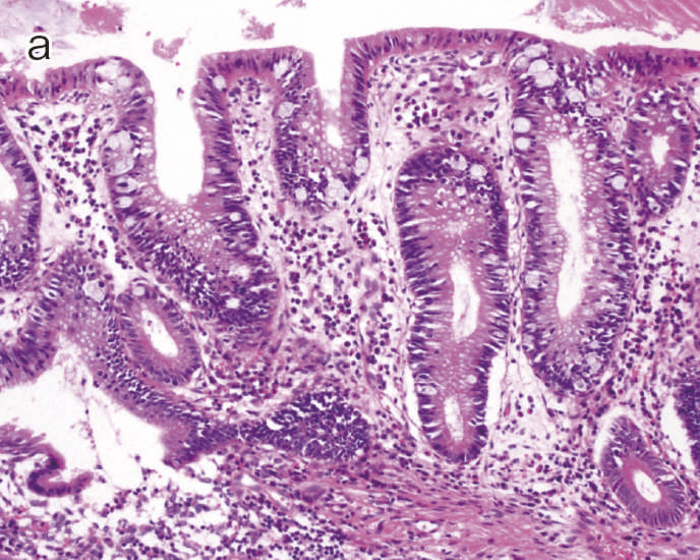
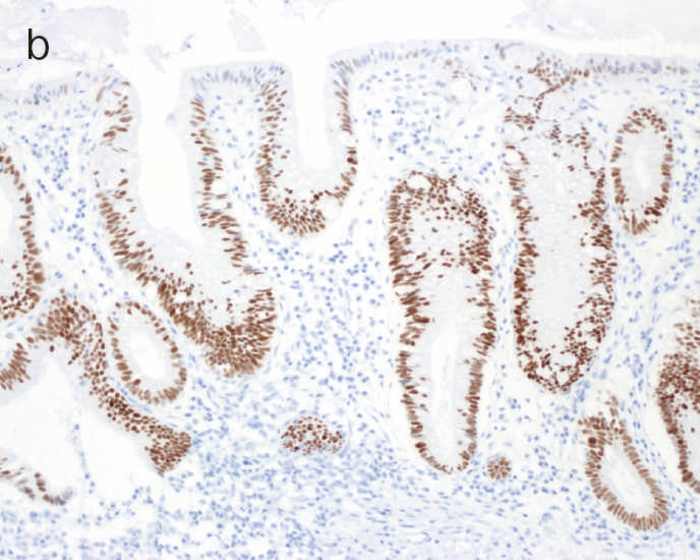
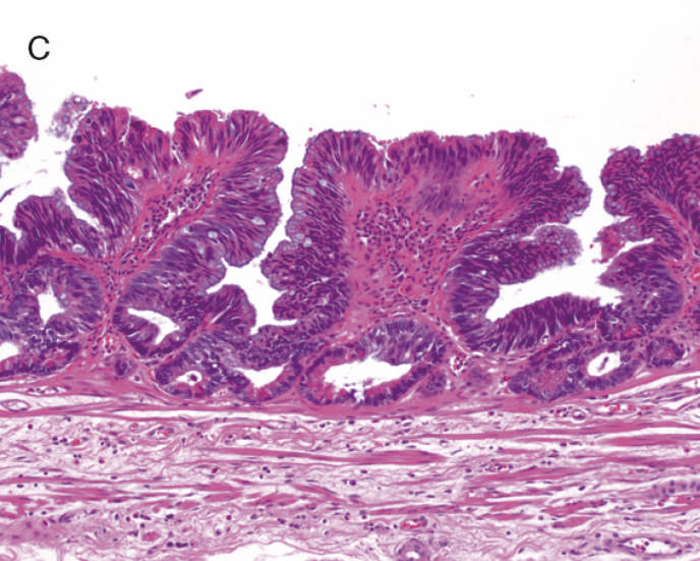
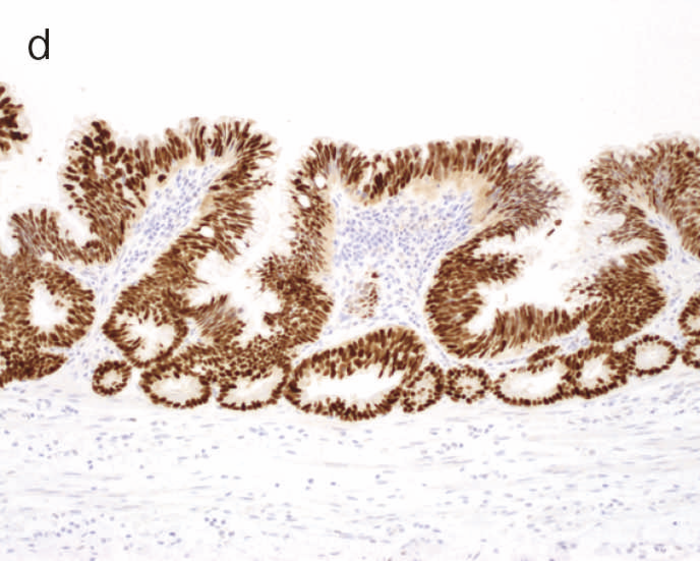
図9 Dysplasiaの代表的な組織像
- LGDの組織像(HE染色):異型腺管では表層への分化傾向が見られる。
- aのp53免疫染色:異型腺管深部側優位にp53蛋白過剰発現が見られる。
- HGDの組織像(HE染色):異型腺管では表層まで核腫大と重積が認められる。
- cのp53免疫染色:異型腺管表層部までp53蛋白の過剰発現が見られる。
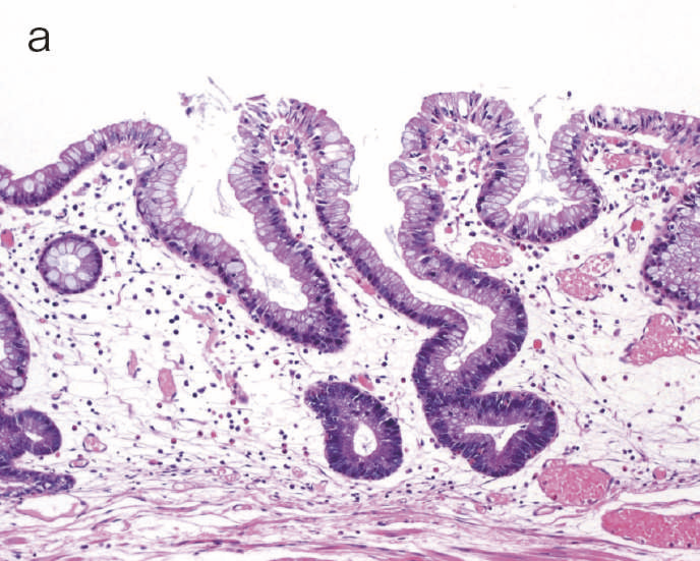
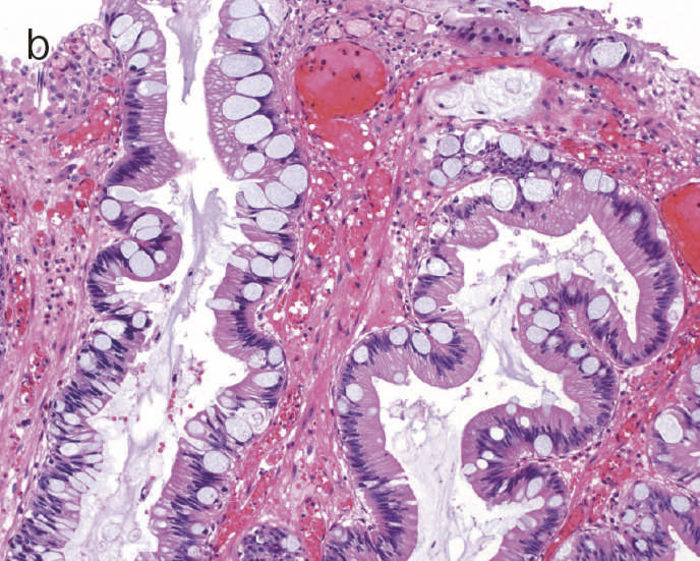
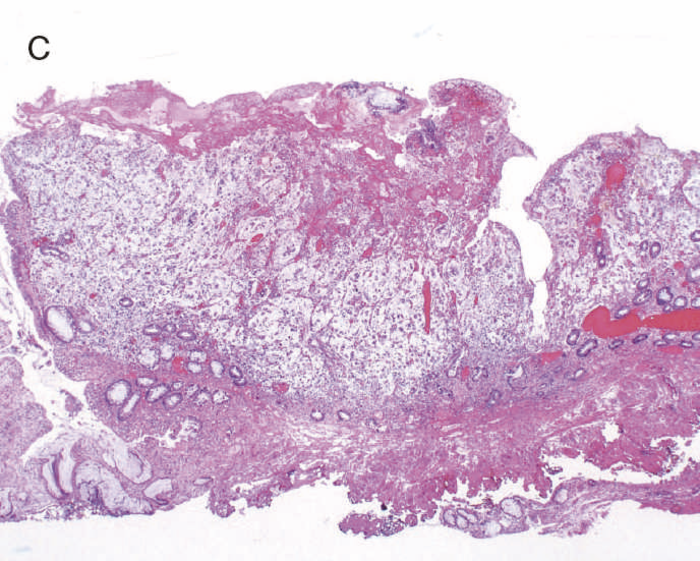
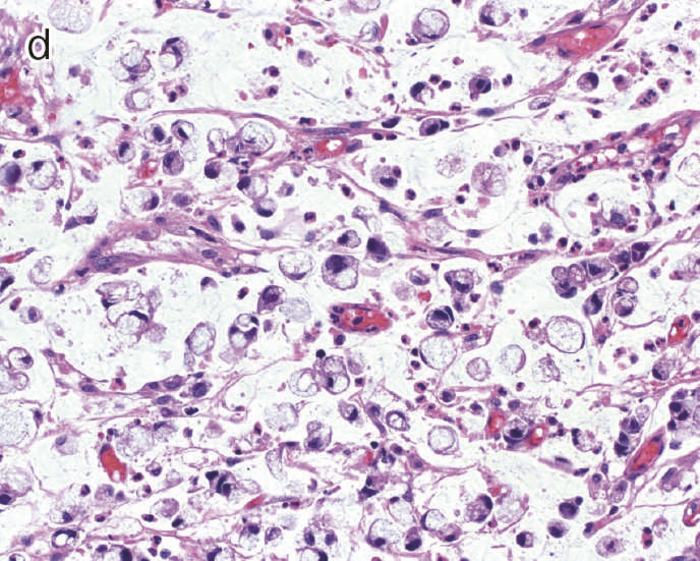
図10 Dysplasiaの多様な組織像
- 表層分化を示すdysplasia。
- 分泌顆粒の局在が核上,核下,表層と不規則な分布を示すdystrophic goblet cellを含むdysplasia。
- UC関連粘膜内低分化腺癌:粘膜内において粘液癌あるいは印環細胞癌が認められる。
- cの拡大像。
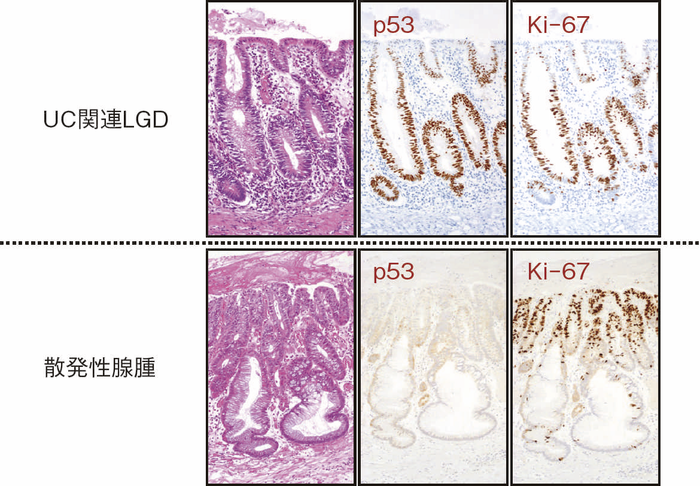
図11 LGDと散発性腺腫の代表的な病理組織像と特徴的免疫染色像
表層への分化傾向を示すLGDでは異型腺管深部側優位にp53蛋白過剰発現が見られるのに対し,散発性腺腫ではp53蛋白異常発現は認められない。また,Ki-67(増殖マーカー)染色においては,LGDでは細胞増殖帯が粘膜深層~中層に位置するが(bottom-up pattern),散発性腺腫では細胞増殖帯が腺管表層~中層に分布する(top-down pattern)(CQ 12,CQ 13)。
- 生検診断
dysplasiaの生検診断には,Riddell systemが国際的に広く用いられている6)。しかしながら,欧米と日本の間には,粘膜内癌をHGDに含めるか否かなど組織診断基準や用語に対する基本的な考え方の違いがあることから,1994年にはわが国においても,厚生省(現厚生労働省)難治性炎症性腸管障害調査研究班による基準が作成されている7)(CQ 11)。本ガイドラインでは,Riddell systemで定義されたdysplasia(LGDとHGD)の概念を採用するとともに,本邦で広く受け入れられている非浸潤癌(上皮内癌)の概念も取り入れ,dysplasiaのうち,組織学的異型度を指標とする日本の病理診断基準で癌と診断されるものは,非浸潤性であってもUC関連粘膜内癌とすることで,Riddell systemと本邦の病理診断とを対応させられるようにした。UCでは異型を有する非腫瘍性の炎症性・再生性上皮が少なからず存在し,これらの病変はdysplasiaとの鑑別を要することがしばしばある。Dysplasiaと散発性腫瘍との鑑別も治療方針決定において重要な要素となりうる(CQ 12,CQ 13)。
文献
- 岩男 泰,下田将之,杉野吉則,他:【colitic cancerの初期病変―遡及例の検討を含めて】内視鏡検査からみたcolitic cancerの初期病変 拡大内視鏡所見を中心に.胃と腸2014;49:1464-1478
- Sugimoto S, Naganuma M, Iwao Y, et al.:Endoscopic morphologic features of ulcerative colitis-associated dysplasia classified according to the SCENIC consensus statement. Gastrointest Endosc 2017;85:639-646.e2
- 味岡洋一,佐野知江:【炎症性腸疾患と大腸癌】潰瘍性大腸炎における大腸癌の病理組織学的特徴と生検診断.日消誌2013;110:379-384
- WHO Classification of Tumours Editorial Board:Digestive System Tumours, WHO Classification of Tumours, 5th Edition, Volume 1. Lyon:International Agency For Research on Cancer, 2019.
- 味岡洋一,渡辺英伸,西倉 健,他:【胃と大腸の腺腫と腺癌 より正確な診断をめざして】形態計測とp53蛋白,Ki-67免疫染色からみた大腸腺腫と腺癌.病理と臨1998;16:37-43
- Riddell RH, Goldman H, Ransohoff DF, et al.:Dysplasia in inflammatory bowel disease:standardized classification with provisional clinical applications. Hum Pathol 1983;14:931-68
- 武藤徹一郎,若狭治毅,喜納 勇,他:潰瘍性大腸炎に出現する異型上皮の病理組織学的判定基準surveillance colonoscopyへの応用を目的とした新判定基準の提案.日本大腸肛門病会誌1994;47:547-551
4 治 療
1)内視鏡治療
● ポイント
- UC関連大腸腫瘍に対する内視鏡切除の適応は病変の境界が明瞭であり範囲診断が正確に行えること,範囲診断に影響するような中等度~重度の炎症が病変部周辺に存在しないこと,および内視鏡的に,深部断端,側方断端いずれも陰性で一括切除できると予想できるLGDまでの病変である。
- UC関連大腸腫瘍に対する内視鏡切除の適応外病変は,同時性に認識困難なdysplasiaがランダム生検で認められた場合,またはHGDあるいは粘膜下層浸潤が疑われる場合である。
- UC関連大腸腫瘍において内視鏡切除の適応を検討する際,色素拡大内視鏡やimage-enhanced endoscopy(IEE)拡大内視鏡による十分な観察が必要である。
- Polypoid lesionに対する内視鏡切除としてendoscopic mucosal resection(EMR)による一括切除が必要である。
- Non-polypoid lesionに対する内視鏡切除としてとくに腫瘍径2 cmを超える場合,endoscopic submucosal dissection(ESD)が必要となる場合が多い。
- UC関連大腸腫瘍に対するESDは,線維化などによる治療困難性に十分注意し,経験豊富な内視鏡医が施行する必要がある。
- UC関連大腸腫瘍に対する内視鏡的治癒切除後には,継続的なサーベイランスを行うことが重要である。
● 解説
- UC関連大腸腫瘍に対する内視鏡切除の適応と診断
UC関連大腸腫瘍に対する治療では,病理診断において,HGD以上の診断がついた場合には,大腸全摘術の適応であることが世界的にもコンセンサスが得られている1)。一方,LGDの治療法に関しては議論が分かれるところである。炎症によるdysplasiaと,sporadicな腫瘍(腺腫)の鑑別が困難な場合があることも一因である。
日本消化器病学会「大腸ポリープ診療ガイドライン2020(改訂第2版)」では,
- 平坦粘膜からLGDが検出された場合は,複数の病理医にコンサルトすることを提案する
- 隆起性病変からLGDが検出された場合には,通常腺腫の可能性が高い場合は内視鏡切除を行って,詳細な病理学的検索を行うことを推奨する
- 癌およびHGDが認められ,慢性炎症を背景に発生したと判断された場合には大腸全摘術の適応であり,行うことを推奨する
としている2)。
これらから,現時点での内視鏡切除はLGDのみ適応と考えることが妥当と思われる。なお,内視鏡切除を施行する場合には,病変は完全切除(R0切除)可能であることが前提である3)。そのうえで大腸の他の部位に別病変を認めない場合,その後のサーベイランスが前提となるが,内視鏡切除で治癒切除が得られるとして良い4)。
UC関連大腸腫瘍においてどのような病変が内視鏡にて完全治癒切除可能かについてエビデンスは乏しい。さらに一般的にUC関連大腸腫瘍は,endoscopic submucosal dissection(ESD)による切除であっても,線維化や境界診断の困難性から技術的な難易度は高いと考えられる。少なくとも,周囲生検で明らかなdysplasiaがなく,いわゆるinvisible lesion(後述)でないこと,内視鏡的に範囲診断が高い確信度で診断可能であること,UCが寛解期であることが必要条件と考えられる3,5)。
なお病理CQ 1で述べられたように,UC関連消化管腫瘍では炎症性発癌はdysplasiaと呼ばれる上皮内腫瘍を形態学的初期病変とすると考えられる。日本と欧米では粘膜内腫瘍に関する病理診断基準が異なるため,欧米の研究,文献では粘膜下層以深に浸潤した病変のみ癌と記載され粘膜内腫瘍はすべて腺腫もしくはdysplasiaと記載されることが多い点に注意が必要である。
内視鏡切除の適応を判断するためには,narrow band imaging(NBI)やblue light imaging(BLI)拡大観察でJapan NBI Expert Team(JNET)分類Type 2AまたはType 2Bであることを確認し,さらにJNET Type 2Bの場合は可能な限りクリスタルバイオレット(CV)染色等の色素拡大内視鏡を施行することが望ましい3)。
UC関連大腸腫瘍においては,前述のごとく内視鏡的に,深部断端,側方断端いずれも陰性で一括切除できると予想できるLGDまでの病変あるいはsporadicな腫瘍(腺腫)が適応である。
その肉眼型から,(1)polypoid lesion,(2)non-polypoid lesion,(3)invisible lesionという3つに分類されることが一般的である4,6)。それぞれの肉眼型によって内視鏡切除の適応が異なる。
(1)Polypoid lesion
Polypoid lesionは規約に基づいた肉眼型ではParis 0-Ⅰp/0-Ⅰsに相当する。一般に,内視鏡的に切除可能とされており,内視鏡切除の良い適応と考える。(2)Non-polypoid lesion
Non-polypoid lesionは規約における肉眼型ではParis 0-Ⅱa,0-Ⅱb,Ⅱcに相当する病変である。発育進展分類である顆粒型側方発育型腫瘍(LST-G)や非顆粒型LST(LST-NG)病変も含まれる(図12)。
一般的にはこのようなnon-polypoid病変は腫瘍径2 cmを超えると,通常endoscopic mucosal resection(EMR)では一括切除が困難である7-9)ため,適切な症例に対して内視鏡切除を適応とすべきであり,またESDが必要となる場合が多い。
これまでの報告ではとくにnon-polypoid lesionにおいては,同時性多発のLGDが多いと報告されている。そのためnon-polypoid lesionに対する内視鏡切除に際しては注意が必要と考えられる10,11)。(3)Invisible lesion
Invisible lesionは,大腸内視鏡検査で病変を認識できないが,組織学的検査で発見されたdysplasiaと定義される。ランダム生検にて発見された病変であることがほとんどであると思われる。これまでの報告では,内視鏡の解像度や条件が異なることから一概に認識不可能といってもさまざまな病変が含まれている可能性が高い。
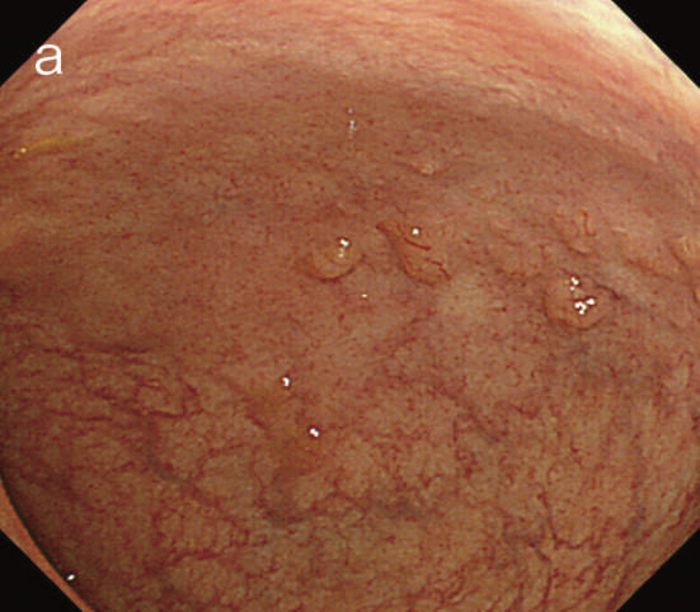
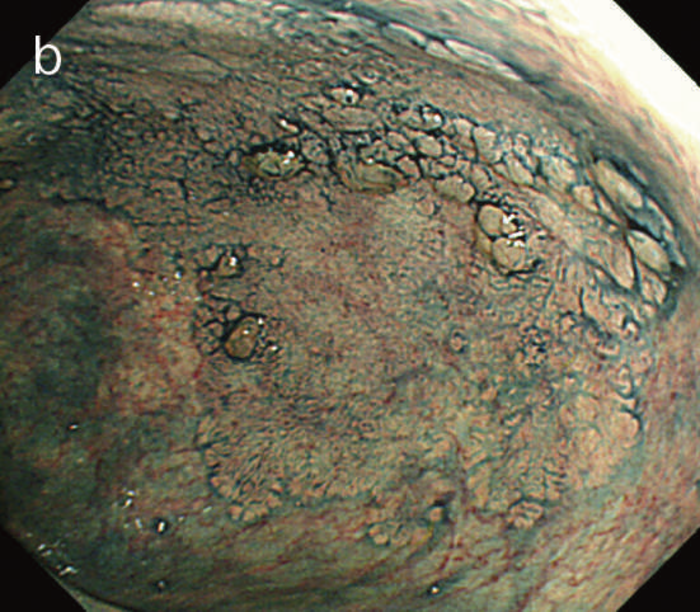
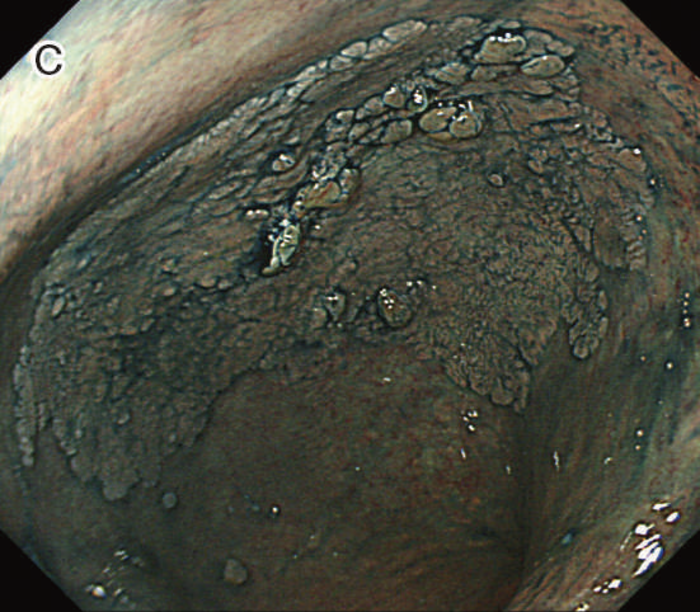
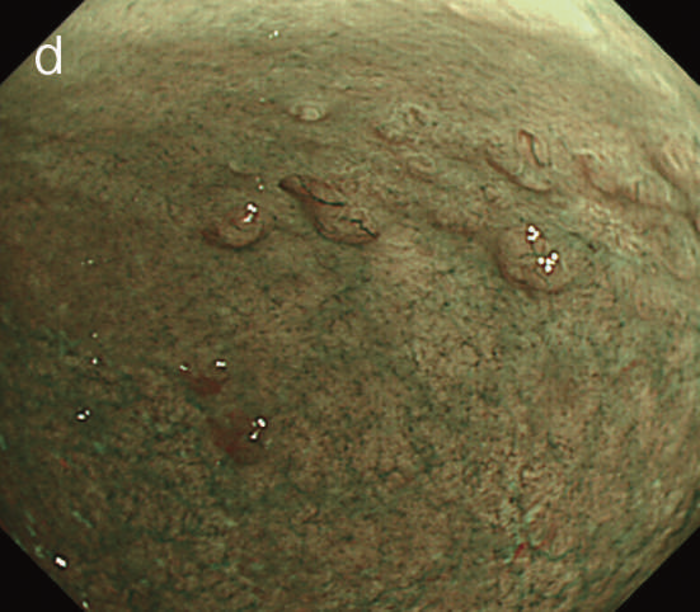
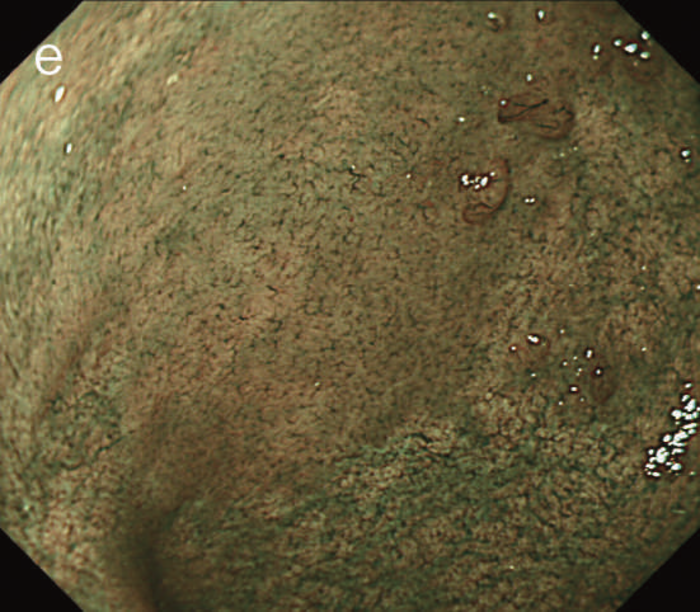
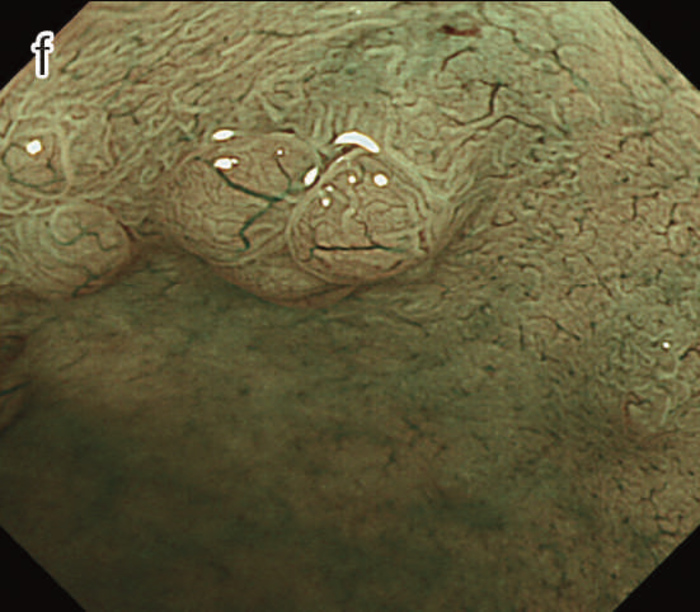
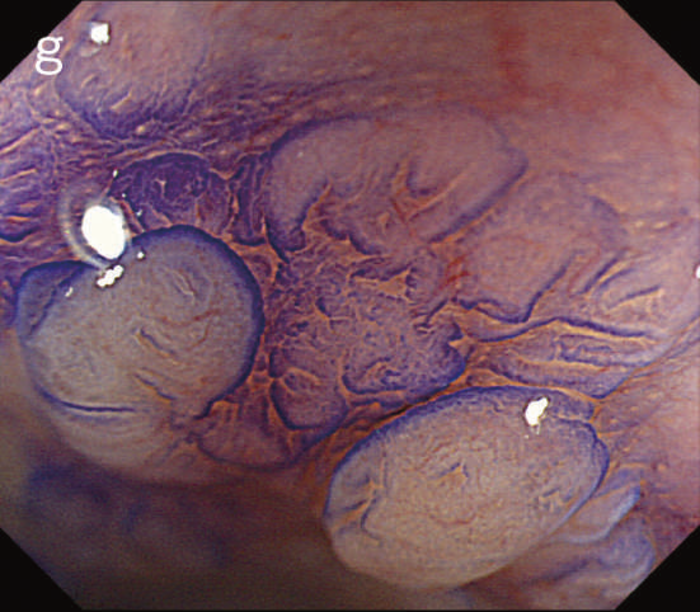
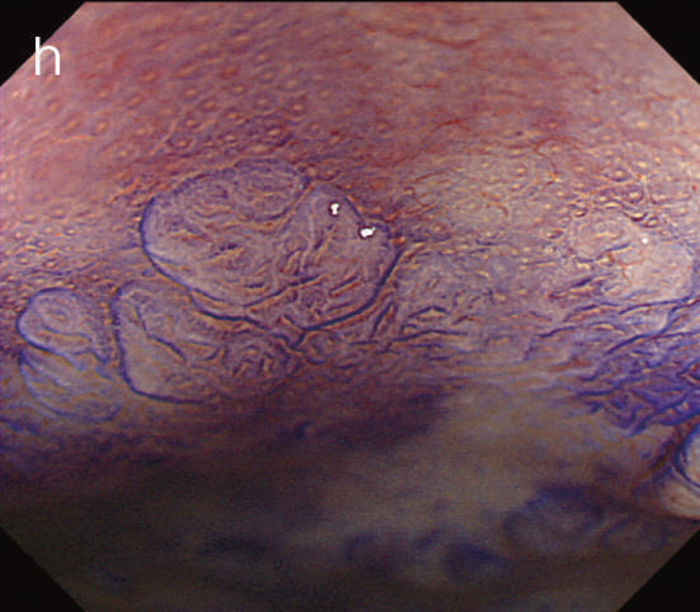
図12 Non-polypoid lesionの内視鏡所見
- 白色光観察
- インジゴカルミン散布像:境界がより明瞭に認識できる。
- 酢酸インジゴカルミン混合液(AIM)散布像:病変全体と周辺粘膜とのコントラストが明瞭となる。
- NBI非拡大観察像:非拡大においても境界の認識は比較的容易となる。
- NIBI拡大観察像:病変中心部では拡張した血管を認める。
- クリスタルバイオレット染色拡大観察像:病変中央では大腸不動の拡張したpitを認める。gの病変辺縁ではpit構造の違いにより周辺粘膜と病変の境界が認識できる。
診断時の内視鏡精度に応じてIEEや色素観察等の画像強調を含めた高画素内視鏡による再検査も考慮する。一方で高解像度・画像強調観察によっても範囲診断が困難である場合には,内視鏡切除の適応とは考えにくく外科的大腸切除術を検討する必要がある。
内視鏡切除の適応を考えるうえで留意すべきもう一つの点は,異時性多発のリスクをどの程度と考えるかである。生検でのみ発見されたinvisible dysplasiaが明らかな病変(LGDまたはadvanced neoplasia)に進展するリスクは報告によって異なり,10年間で3%とする報告12)や,5年間で53%とする報告や,初発病変がpolypoid lesionの場合5年後にHGD以上の異時性病変を認めるリスクは6%である一方,初発病変がnon-polypoid lesionの場合は65.2%とする報告もある。
これらのことから,non-polypoid lesionやinvisible dysplasiaの異時性多発のリスクに関して十分なデータがあるとはいいがたく,外科的大腸切除術におけるリスクベネフィットバランスが十分評価できるとはいえないのが現状と考えられる。
- 内視鏡切除の方法
内視鏡切除を行う際注意すべきUC関連腫瘍の特徴として,背景粘膜の炎症等のため範囲診断が困難である場合が多いこと,および,粘膜下層の線維化の頻度が多い点がある。内視鏡切除を行う時にはこれらの点に注意する必要がある。
European Crohn’s and colitis organization(ECCO)のガイドラインでは,内視鏡的に「完全切除」できる病変に関しては第一選択として内視鏡切除が推奨されている。SCENICでは内視鏡的な完全切除(endoscopically resectable)を「内視鏡的に境界が明瞭であり,内視鏡的にも組織学的にも病変が完全切除され,周囲の粘膜からdysplasiaが検出されないこと」と定義している6)。
(1)Polypoid lesion
polypoid lesionは,病変が完全にR0切除可能と診断され,他の部位にnon-polypoid lesionやinvisible dysplasiaがない場合には,確実な一括EMRを施行し,組織学的に治癒切除が得られた場合はその後の継続的なサーベイランスを行うことが可能であると考えられる。
これまでの報告でも,UC患者の大腸腫瘍病変が内視鏡的に切除・フォローアップされた場合,UC患者におけるdysplasiaと散発性腺腫(50%)間での新規病変の有病率に有意差はなく,UC患者におけるdysplasiaまたは散発性腺腫のいずれかと非UC患者における散発性腺腫の間でも新規病変の有病率に差は認めないことが報告されている13-16)。最近の文献でも同様の報告があり,UC関連のLGD 172人でpolypoid lesionを発見してから5年後にHGDまたは大腸癌が生じる累積発生率は6%であった10)。
また,これまでのメタアナリシス(10の研究,合計376人)では,polypoid lesionに対する内視鏡切除後の大腸癌プール発生率は,5.3/1,000人年(95%信頼区間2.6-10.1)と報告されている17)。(2)Non-polypoid lesion
ECCOガイドラインにおいてnon-polypoid lesionに対しては,内視鏡的完全切除が得られれば内視鏡的サーベイランスを許容するとしている4)。
そのため,内視鏡切除を行う際にはpolypoid lesionと同様一括R0切除が重要と考えられる。10 mm前後の病変に対してはEMRも選択枝として考えられるが,UC関連大腸腫瘍では線維化を伴う頻度が高いとされ5,7-9,18),20 mmを超える病変や線維化を疑う症例に対しては一括R0切除のためにはESDで対応すべきである。
一方でUC関連大腸腫瘍に対するESDのエビデンスは未だ十分とはいえず,単施設後方視的研究による報告がほとんどである7-9,19-24)。いずれの報告においても,UC関連大腸腫瘍に対するESDの安全性と有効性の可能性を示唆している。同時に,線維化が多く手技的に困難を伴うこと7-9,20),異時性多発病変が多く慎重かつ密な内視鏡的サーベイランスが必要なこと7,9,21,22)が強調されている。
これらのことを考慮すると,UC関連大腸腫瘍に対するESDは,色素拡大内視鏡やIEE拡大内視鏡による十分な診断のもと行うべきであり9),線維化やlifting不良等に対する困難性に十分注意したうえで,経験豊富な内視鏡医によって施行する必要がある3,24)と考えられる。
また,色素拡大内視鏡やIEE拡大内視鏡を使用しても範囲診断困難な病変が存在し,さらには術前の内視鏡で必ずしもすべての病変が認識できているとは限らないという視点での慎重なフォローアップも重要である8)。クリスタルバイオレットの使用については日本消化器内視鏡学会の声明を参照。
文献
- Itzkowitz SH, Harpaz N:Diagnosis and management of dysplasia in patients with inflammatory bowel diseases. Gastroenterology 2004;126:1634-1648
- 日本消化器病学会編:大腸ポリープ診療ガイドライン2020(改訂第2版).東京,南江堂,2020.
- Bak MTJ, Albéniz E, East JE, et al.:Endoscopic management of patients with high-risk colorectal colitis-associated neoplasia:a Delphi study. Gastrointest Endosc 2022;97:767-779
- Magro F, Gionchetti P, Eliakim R, et al.:Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1:Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders. J Crohns Colitis 2017;11:649-670
- 田中秀典,岡 志郎,田中信治:【手技の解説】潰瘍性大腸炎関連腫瘍に対するESDの実際.Gastroenterol Endosc 2021;63:1382-1388
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology 2015;148:639-651.e28
- Suzuki N, Toyonaga T, East JE:Endoscopic submucosal dissection of colitis-related dysplasia. Endoscopy 2017;49:1237-1242
- Kasuga K, Yamada M, Shida D, et al.:Treatment outcomes of endoscopic submucosal dissection and surgery for colorectal neoplasms in patients with ulcerative colitis. United European Gastroenterol J 2021;9:964-972
- Iacopini F, Saito Y, Yamada M, et al.:Curative endoscopic submucosal dissection of large nonpolypoid superficial neoplasms in ulcerative colitis(with videos). Gastrointest Endosc 2015;82:734-738
- Choi CH, Ignjatovic-Wilson A, Askari A, et al.:Low-grade dysplasia in ulcerative colitis:risk factors for developing high-grade dysplasia or colorectal cancer. Am J Gastroenterol 2015;110:1461-1471;quiz 1472
- Odze RD:Adenomas and adenoma-like DALMs in chronic ulcerative colitis:a clinical, pathological, and molecular review. Am J Gastroenterol 1999;94:1746-1750
- Befrits R, Ljung T, Jaramillo E, Rubio C:Low-grade dysplasia in extensive, long-standing inflammatory bowel disease:a follow-up study. Dis Colon Rectum 2002;45:615-620
- Rutter MD, Saunders BP, Wilkinson KH, et al.:Cancer surveillance in longstanding ulcerative colitis:endoscopic appearances help predict cancer risk. Gut 2004;53:1813-1816
- Vieth M, Behrens H, Stolte M:Sporadic adenoma in ulcerative colitis:endoscopic resection is an adequate treatment. Gut 2006;55:1151-1155
- Odze RD, Farraye FA, Hecht JL, et al.:Long-term follow-up after polypectomy treatment for adenoma-like dysplastic lesions in ulcerative colitis. Clin Gastroenterol Hepatol 2004;2:534-541
- Rubin PH, Friedman S, Harpaz N, et al.:Colonoscopic polypectomy in chronic colitis:conservative management after endoscopic resection of dysplastic polyps. Gastroenterology 1999;117:1295-1300
- Wanders LK, Dekker E, Pullens B, et al.:Cancer risk after resection of polypoid dysplasia in patients with longstanding ulcerative colitis:a meta-analysis. Clin Gastroenterol Hepatol 2014;12:756-764
- 斎藤 豊,春日健吾,山田真善,他.潰瘍性大腸炎関連腫瘍に対する内視鏡治療―私はこう考える.胃と腸2020;55:172-176
- Manta R, Zullo A, Telesca DA, et al.:Endoscopic Submucosal Dissection for Visible Dysplasia Treatment in Ulcerative Colitis Patients:Cases Series and Systematic Review of Literature. J Crohns Colitis 2021;15:165-168
- Zeng QS, Zhao ZJ, Nie J, et al.:Efficacy and Safety of Endoscopic Submucosal Dissection for Dysplasia in Ulcerative Colitis Patients:A Systematic Review and Meta-Analysis. Gastroenterol Res Pract 2022;2022:9556161
- Yang DH, Kim J, Song EM, et al.:Outcomes of ulcerative colitis-associated dysplasia patients referred for potential endoscopic submucosal dissection. J Gastroenterol Hepatol 2019;34:1581-1589
- Matsumoto K, Oka S, Tanaka S, et al.:Long-Term Outcomes after Endoscopic Submucosal Dissection for Ulcerative Colitis-Associated Dysplasia. Digestion 2021;102:205-215
- Lightner AL, Vaidya P, Allende D, et al.:Endoscopic submucosal dissection is safe and feasible, allowing for ongoing surveillance and organ preservation in patients with inflammatory bowel disease. Colorectal Dis 2021;23:2100-2107
- Kinoshita S, Uraoka T, Nishizawa T, et al.:The role of colorectal endoscopic submucosal dissection in patients with ulcerative colitis. Gastrointest Endosc 2018;87:1079-1084
2)手術治療
● ポイント
- UC関連大腸癌およびHGDは絶対的手術適応,LGDのうち癌合併の可能性が高い症例は相対的手術適応とされている。
- UC関連大腸癌症例に対する推奨される術式は大腸全摘,回腸囊肛門吻合術ではあるが,癌の局在,進行度,年齢,括約筋機能も考慮し,十分なインフォームドコンセントを得たうえ術式を決定すべきである。
- UC関連大腸癌症例に対する低侵襲手術は推奨されるが,難易度は高く各施設のチームの習熟度と症例の全身状態を考慮して適応を決定すべきである。本術式はhigh volume centerで行うことが望ましい。
- 術後に生じる難治性の回腸囊炎合併症例ではpouchのサーベイランスも考慮すべきである。
● 解説
- 手術適応
厚生労働省の「難治性炎症性腸管障害に関する調査研究」(久松班)令和3年度改訂版のUC外科治療指針には手術適応として上記の記載がある。ただ,癌,HGD,LGDの鑑別診断は容易ではない。正確な病理診断を目的に内視鏡検査によるtotal biopsyを行い,その結果を参考にし,手術適応を決定するのも一つの方法である1)。
- 術式の選択
UCに対する代表的な術式を図13に示した。UC関連大腸癌の場合,散発性大腸癌に比べて,腫瘍組織と非腫瘍組織の区別が難しい症例も多く,病変の周囲にdysplasiaを合併している症例も多いため,特に下部直腸に病変を有している症例では,術式の選択は慎重に行うべきである。
(1)大腸全摘,回腸囊肛門吻合術(Ileoanal anastomosis:IAA)
直腸粘膜をすべて切除し,回腸囊と肛門を手縫い吻合する。UCに対しても根治性が高い術式である。図14のように,肛門管粘膜の切除開始ラインは歯状線の肛門側で,肛門陰窩をすべて切除する。切除開始ラインが歯状線よりも口側になり,一部肛門管粘膜(移行帯上皮)を温存させた結果,この残存した粘膜からの発癌を強く示唆する症例報告も存在する2)。また,IAAを行ったにもかかわらず,術後に発癌したという症例報告も存在するが,多くは術後3年以内に発症している症例が多く,術前の直腸癌の局所再発が原因ではないかとの意見が一般的である3)。下部直腸から肛門管にかけて早期癌を合併するような症例では,術後の病理検査で,DM0,RM0であっても図15のように局所再発を生じる可能性もあるので,定期的な画像診断とともに,直腸診を行い,局所再発がないことを確認すべきである4)。
CQ 16で述べたように,UC関連大腸腫瘍を合併した症例に対してはIAAが推奨されるが,技術的にIAAが実施可能な体型かという問題も考慮しなければならない。図16のように回腸間膜を開窓してpouch topの位置確認を行うが,恥骨結節の下縁よりも少なくとも2 cm程度肛門側まで進展しない場合は,肛門吻合は難しい。術中判断で回腸囊が肛門まで到達することが困難な症例では回腸囊肛門管吻合術(ileoanal canal anastomosis:IACA)+術後のATZ(anal transitional zone)の内視鏡的サーベイランスという選択肢も考慮する必要がある。ただ,下部直腸に腫瘍が存在する場合はこの選択はできない症例もあり,大腸全摘,永久回腸人工肛門造設術が必要になることもあるので,術前に十分にインフォームドコンセントを得ておく必要がある。(2)大腸全摘,回腸囊肛門管吻合術(ileoanal canal anastomosis:IACA)
回腸囊と肛門管を器械吻合して肛門管粘膜を温存する術式である。IAAと比べて括約筋機能は良好であるという報告が多い反面,残存肛門管粘膜からの発癌症例もみられ,術後は残存肛門管粘膜に対する内視鏡的サーベイランスが必要である。図17にIACA後に残存肛門管から発癌した症例の切除標本を示す5)。できるだけ残存肛門管粘膜を少なくするために,後壁は歯状線近傍で吻合を行う,double stapling technique(DST)も報告されているが,この術式も体型による影響を受け,肥満体型の男性には低位での吻合は困難である6)。
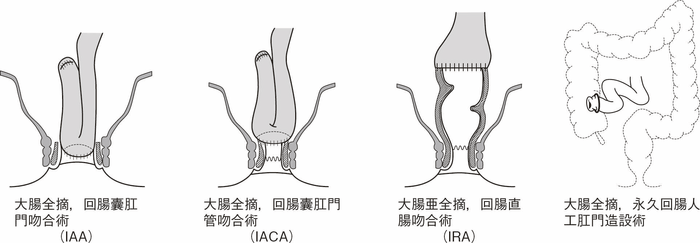
図13 潰瘍性大腸炎に対する主な術式
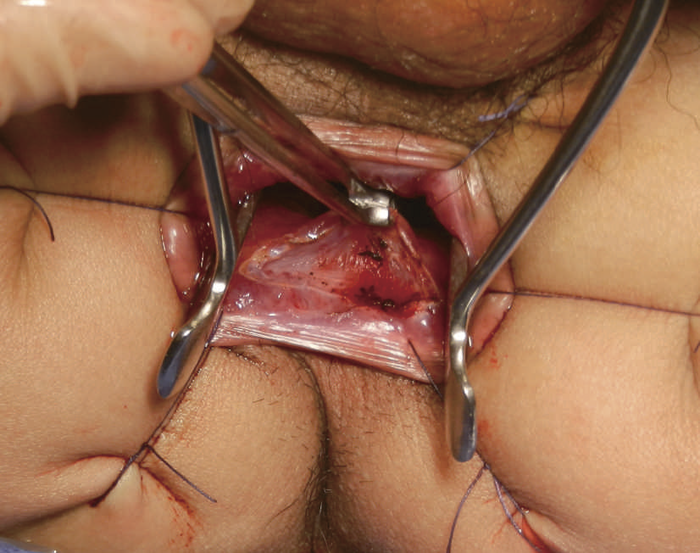
図14 IAA時の粘膜切除の開始ライン
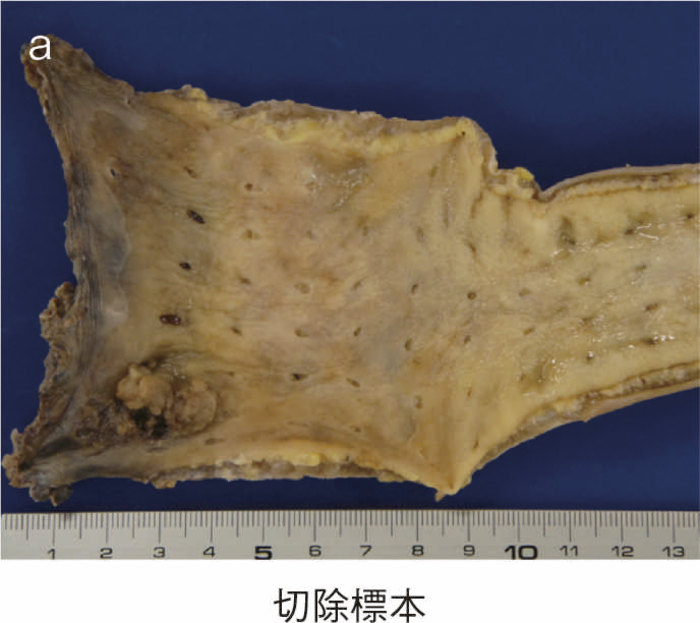
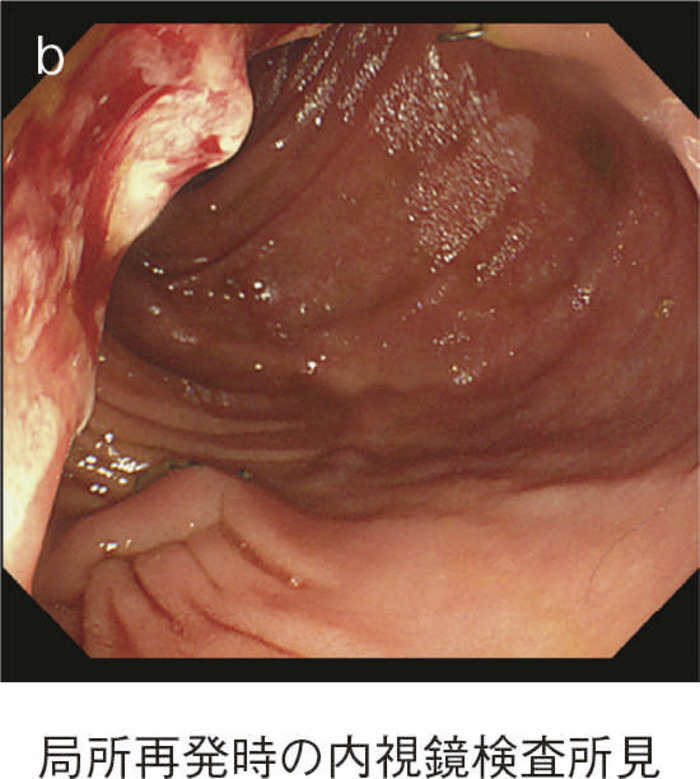
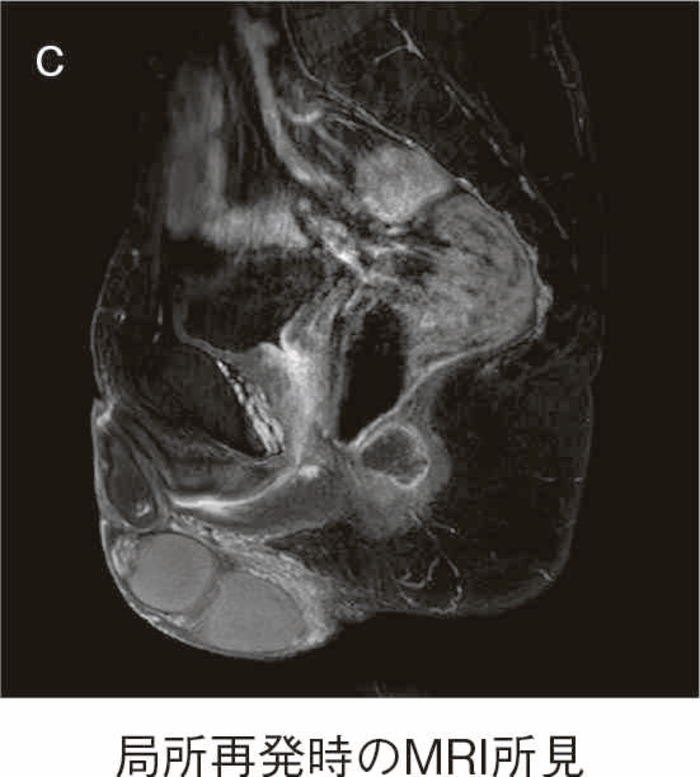
図15 IAA後に局所再発を生じた症例
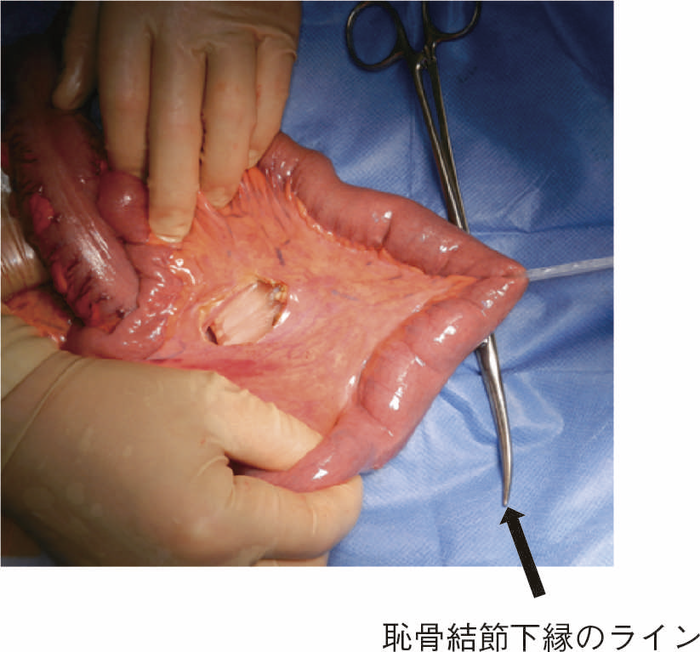
図16 回腸間膜の開窓とPouch topの位置確認
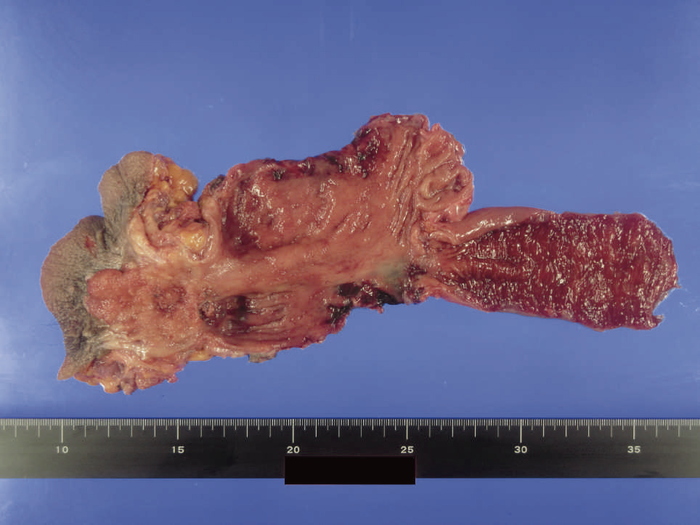
図17 IACA後の残存肛門管からの発癌症例
(3)大腸全摘,永久回腸人工肛門造設術
CQ 17でも示したように肛門温存が不可能な下部直腸の進行癌症例や最近増加が著しい,ADLの低下している高齢者に対して選択される術式である。術後のQOLを考えると,高齢者に対しては括約筋温存手術よりも良好である症例も多い。
(4)大腸亜全摘,回腸直腸吻合術(ileorectal anastomosis:IRA)
この術式は最も罹患歴の長い直腸を温存させる術式であるため,残存直腸の炎症のコントロールの問題だけでなく,直腸からの発癌症例の報告例も増加し,現在では直腸の炎症が軽微な高齢者など,条件を満たす症例以外には行われていない。残存直腸の炎症のコントロールや,残存直腸に対するサーベイランスが必要である。図18にIRA後に残存直腸から発癌した症例の切除標本を示した。
(5)大腸部分切除術
UCに合併する発癌症例がすべて炎症性発癌症例とは限らず,通常の大腸癌症例も存在する。p53染色の結果や病変周囲のdysplasiaの有無を参考にしながら診断されるが,両者の鑑別は必ずしも容易ではない。通常の大腸癌と診断された上行結腸癌に対する結腸右半切除術は,横行結腸に炎症がなければ,ほぼ問題なく行うことができる。一方,左側の病変では,吻合する口側,肛門側の大腸の炎症の有無にも影響を受けるため,一概に大腸部分切除術で良いとは言えない。寛解期であっても鉛管状になった硬化した腸管では,吻合に不安が残る。このような現状を考えると大腸部分切除は難しい。
- 癌合併症例に対する低侵襲手術
UCに対する手術は,通常開腹症例は減少し,小開腹手術,腹腔鏡下手術,ロボット併用手術へと進歩している。ただCQ 20に示したように,ロボット併用手術は大腸全摘術の直腸切除術のみに使われ,結腸の手術は腹腔鏡下手術で行われたとの報告が多く,UC関連大腸癌に対するロボット併用手術の有用性は今後の検討課題である7)。
UCに対するこれらの低侵襲手術は通常の開腹手術に比べて整容性の点で優れていることは言うまでもない。UCに合併する発癌症例に対する大腸全摘術も,部分切除を組み合わせた術式であることを考えると,根治性には問題がないと思われる。ただ,難易度は高い手術であり,これらの手術は専門施設で行うことが望ましい。 - 術後の経過観察
UC術後の回腸囊には回腸囊炎を合併する症例があることは広く知られており,本邦においても増加傾向である。UC術後のpouchからの腫瘍の発症率は術後10年で1.3%,20年で4.2%との報告がある8)。また,術前に癌を合併していた症例は,回腸囊の発癌のrisk factorであると報告されている8)。そのため癌/dysplasiaで手術となった症例や難治性の回腸囊炎を合併した症例では回腸囊のサーベイランスも必要となる。図19に回腸囊炎を繰り返し,術後30年目に回腸囊内にHGDを合併し回腸囊切除を行った症例の内視鏡検査所見を示す9)。
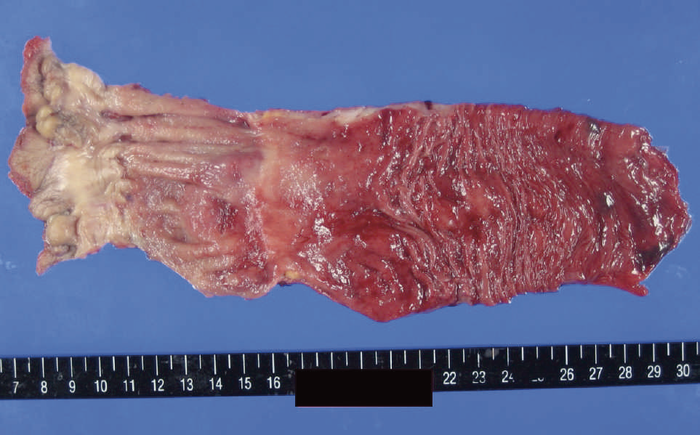
図18 IRA後の残存直腸からの発癌症例
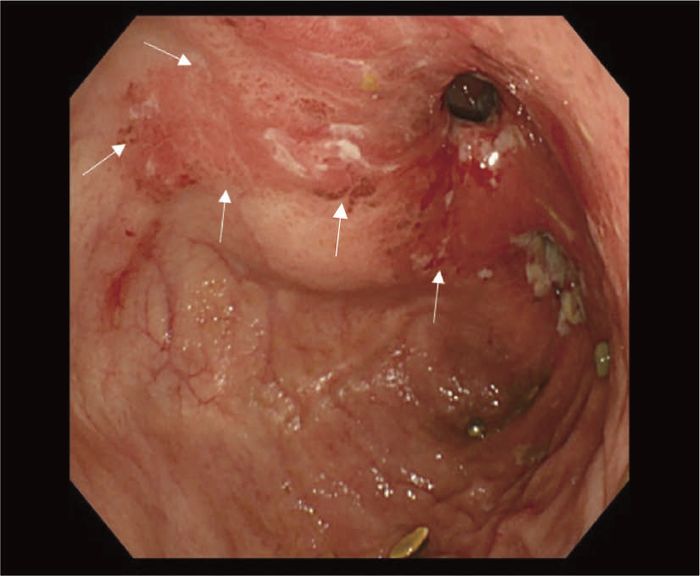
図19 回腸囊内にHGDを合併した症例
文献
- 「難治性炎症性腸管障害に関する調査研究」(久松班)令和3年度分担研究報告書別冊厚生労働科学研究費補助金難治性疾患政策研究事業.2022
- Rodriguez-Sanjuan JC, Polavieja MG, Naranjo A, et al.:Adenocarcinoma in an ileal pouch for ulcerative colitis. Dis Colon Rectum 1995;38:779-780
- Lee SW, Sonoda T, Milsom JW:Three cases of adenocarcinoma following restorative proctocolectomy with hand-sewn anastomosis for ulcerative colitis:a review of reported cases in the literature. Colorectal Dis 2005;7:591-597
- 桑原隆一,池内浩基,楠 蔵人,他:直腸肛門管早期癌に対する大腸全摘回腸囊肛門吻合術後に吻合部再発を来した潰瘍性大腸炎の1例.日消外会誌2022;5:464-472
- 平田晃弘,池内浩基,坂東俊宏,他:潰瘍性大腸炎に対する大腸全摘・J型回腸囊肛門管吻合術後に発生した残存肛門管癌の1例.日消外会誌2017;50:499-505
- 杉田 昭,小金井一隆,木村英明,他:【消化管再建術の現状と将来―最良の再建術は何か―】6.大腸全摘術後再建術.日外会誌2008;109:269-273
- Flynn J, Larach JT, Kong JCH, et al.:Robotic versus laparoscopic ileal pouch-anal anastomosis(IPAA):a systematic review and meta-analysis. Int J Colorectal Dis 2021;36:1345-1356
- Kariv R, Remzi FH, Lian L, et al.:Preoperative colorectal neoplasia increase risk for pouch neoplasia in patients with restorative proctocolectomy. Gastroenterology 2010;139:806-812
- 佐々木寛文,池内浩基,皆川知洋,他:潰瘍性大腸炎術後30年目にJ型回腸囊内にhigh grade dysplasiaを認めた1例.日消外会誌2018;51:784-790
3)薬物療法
● ポイント
- UC関連大腸癌における根治術後の補助化学療法や進行・再発大腸癌に対する化学療法の有効性はエビデンスが不十分なため明らかでない。
- UC関連大腸癌に対しては本邦では大腸癌研究会の大腸癌治療ガイドラインに準じ,全身状態,主要臓器機能を評価し薬物療法の適応やレジメン選択が行われているのが現状である。
● 解説
- 術後補助化学療法(CQ 24)
術後補助化学療法は治癒切除例に対して再発抑制を目的に術後に行われる薬物療法である。UC関連大腸癌に対する大腸全摘術後は慢性抗菌薬抵抗性回腸囊炎などの特殊な病態を除いて生物学的製剤などの免疫調節治療を用いることはないため,UCの病態を考慮することなく大腸癌に特化した治療を開始できる。
これまでUC関連大腸癌少数例に対する補助化学療法についての報告があるが1),術後補助化学療法の有効性を前向きに比較検討した報告はない。CDおよびUCに合併するIBD関連癌に対する補助化学療法に関する本邦からの後ろ向きの検討では,S-1が最も多く用いられ,5年無再発生存率は78%と報告されている2)。ただし,UC関連大腸癌に対する補助化学療法の有効性を検討したエビデンスはなく,大腸癌治療ガイドラインに準じて,全身状態,主要臓器機能に基づきオキサリプラチン併用療法,あるいはフッ化ピリミジン単独療法が行われているのが現状である。 - 切除不能進行・再発癌に対する薬物療法(CQ 25)
散発性大腸癌における切除不能進行・再発癌では薬物療法を実施しない場合,生存期間中央値(MST)は約8カ月とされているが3),最近の化学療法の進歩によりMSTは30カ月を超えるまでに延長している4-6)。
本邦から切除不能進行・再発IBD関連消化管癌に対する化学療法後の経過が報告されている2)。FOLFOXまたはFOLFOX+BEVまたはFOLFOX+CET療法が一次治療として多く用いられ,用量強度(dose intensity)は散発性消化管癌の報告と比べ低く7),無増悪生存期間の中央値,MSTはそれぞれ182日,315日であった2)。また切除不能進行・再発IBD関連大腸癌では散発性大腸癌に比べ5年生存率が低下していたとする報告がある8)。さらに切除不能進行・再発IBD関連消化管癌(大腸癌15例および小腸癌3例)に対し,FOLFOXまたはFOLFOX+BEV療法,FOLFIRIまたはFOLFIRI+BEV療法,5FU+l-LV療法,FOLFOX+肝動注療法が行われ,散発性消化管癌と比べて奏効率には差はなかったものの,MSTは短かった(13.5 vs 27.6カ月)と報告されている9)。
しかしIBD関連進行・再発消化管癌症例において,化学療法の有効性を前向きに比較検討した報告はなく,UC関連進行・再発大腸癌症例に限っても同様である。そのためUC関連進行・再発癌に対する化学療法は術後補助化学療法と同様に大腸癌研究会の大腸癌治療ガイドラインに準じ,薬物療法の適応やレジメン選択が行われているのが現状である。 - 化学療法の忍容性
IBD関連大腸癌に補助化学療法(FOLFOX療法,CAPOX療法,S-1,capecitabine,UFT+LV療法等)が行われた症例についての検討では,補助化学療法が完遂されたものは44%と散発性大腸癌に比較して完遂率が低い可能性が示された2)。化学療法に伴う有害事象とIBD疾患活動性の関連について,活動期ではGrade 3/4の胃腸障害発現率が増加したという報告2)がある一方,開始遅延や中断,薬剤減量に影響しなかったという報告8)もあるが,UC関連大腸癌に対する大腸全摘術後の化学療法の胃腸障害への影響について検討した報告はない。下痢などの胃腸障害が発生しやすい可能性があり注意を要する。
サイドメモ
- FOLFOX
- フルオロウラシル(5-FU)+レボホリナート(LV/l-LV)+オキサリプラチン(OX)
- FOLFIRI
- フルオロウラシル+レボホリナート+イリノテカン(IRI)
- CAPOX
- カペシタビン(Cape)+オキサリプラチン
- S-1
- テガフール・ギメラシル・オテラシルカリウム
- 5-FU+l-LV
- フルオロウラシル+レボホリナート
- UFT+LV
- テガフール・ウラシル(UFT)+レボホリナート
文献
- Gorfine SR, Harris MT, Bub DS, et al.:Restorative proctocolectomy for ulcerative colitis complicated by colorectal cancer. Dis Colon Rectum 2004;47:1377-1385
- Nio K, Higashi D, Kumagai H, et al.:Efficacy and safety analysis of chemotherapy for advanced colitis-associated colorectal cancer in Japan. Anticancer Drugs 2016;27:457-463
- Simmonds PC:Palliative chemotherapy for advanced colorectal cancer:systematic review and meta-analysis. Colorectal Cancer Collaborative Group. BMJ 2000;321:531-535
- Yamada Y, Takahari D, Matsumoto H, et al.:Leucovorin, fluorouracil, and oxaliplatin plus bevacizumab versus S-1 and oxaliplatin plus bevacizumab in patients with metastatic colorectal cancer(SOFT):an open-label, non-inferiority, randomised phase 3 trial. Lancet Oncol 2013;14:1278-1286
- Loupakis F, Cremolini C, Masi G, et al.:Initial therapy with FOLFOXIRI and bevacizumab for metastatic colorectal cancer. N Engl J Med 2014;371:1609-1618
- Yamazaki K, Nagase H, Tamagawa H, et al.:Randomized phase Ⅲ study of bevacizumab plus FOLFIRI and bevacizumab plus mFOLFOX6 as first-line treatment for patients with metastatic colorectal cancer(WJOG4407G). Ann Oncol 2016;27:1539-1546
- Cassidy J, Clarke S, Díaz-Rubio E, et al.:Randomized phase Ⅲ study of capecitabine plus oxaliplatin compared with fluorouracil/folinic acid plus oxaliplatin as first-line therapy for metastatic colorectal cancer. J Clin Oncol 2008;26:2006-2012
- Axelrad J, Kriplani A, Ozbek U, et al.:Chemotherapy Tolerance and Oncologic Outcomes in Patients With Colorectal Cancer With and Without Inflammatory Bowel Disease. Clin Colorectal Cancer 2017;16:e205-e210
- Yaeger R, Paroder V, Bates DDB, et al.:Systemic Chemotherapy for Metastatic Colitis-Associated Cancer Has a Worse Outcome Than Sporadic Colorectal Cancer:Matched Case Cohort Analysis. Clin Colorectal Cancer 2020;19:e151-e156
5 予 後
● ポイント
- UC関連大腸癌の全生存は散発性大腸癌よりも不良である。
- 切除術後の再発は腹膜播種が最も多く,予後不良の一因と考えられる。
● 解説
- 全生存
大腸癌研究会で行われたプロジェクト研究「炎症性腸疾患合併消化管癌のデータベース作成と臨床病理学的研究」(以下「プロジェクト研究」)で集積された,UC関連大腸癌症例(1983~2020年)の全生存率を図20に示す。進行度がStage 0, 1, 2のいわゆる「localized」の状態である症例の5年全生存率は90%以上と良好だが,Stage 3の「regional」の症例の5年全生存率は67%と低下してStage 0, 1, 2と比べて有意に不良である1)。遠隔転移を伴うStage 4症例の5年全生存率は18%と非常に不良である。過去に大腸癌研究会の全国登録症例を用いた散発性大腸癌との比較では,Stage 3においてUC関連大腸癌の方が散発性大腸癌よりも予後が悪いことが報告されている(Stage 3の5年生存率はUC関連大腸癌43.3%に対して散発性大腸癌57.4%)2)。両者を直接比較した国内外の報告に関するシステマティックレビューにおける10論文のメタアナリシスは,散発性大腸癌に比べてUC関連大腸癌の全生存率は有意に不良であることが示されている(ハザード比(HR)1.35)3)(CQ 27)。
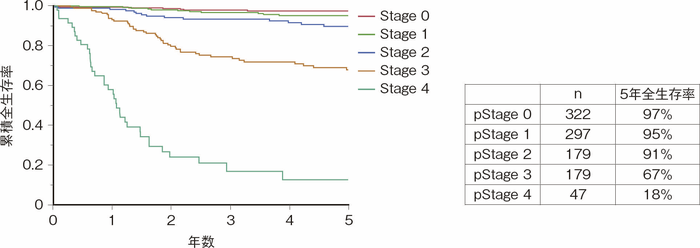
図20 UC関連大腸癌(全生存率)
- CD関連大腸癌との比較
プロジェクト研究におけるCD関連大腸癌との比較では,Stage 0, 1症例の全生存は同等であったが,Stage 2, 3, 4症例においてはUC関連大腸癌の全生存はCD関連大腸癌に比べて有意に良好であった1)(各論Ⅱ,CD関連消化管腫瘍,5.予後を参照)。UC関連大腸癌とCD関連大腸癌の予後を直接比較した論文は少ないが,3論文のメタアナリシスの結果でも同様にUC関連大腸癌の全生存はCD関連大腸癌よりも有意に良好である結果が示されている3)。 - 術後再発形式
プロジェクト研究で集積された症例の切除後における部位別再発症例数(観察期間中央値46カ月)を図21に示す。腹膜播種再発が最も多く,2番目に多いのは局所再発であった1)。大腸癌研究会による全大腸癌の全国登録の成績では肝再発が最も多く,次いで肺再発であり,いずれも腹膜再発や局所再発の約3倍の頻度であるが,プロジェクト研究のUC関連大腸癌においては腹膜播種や局所再発よりも少なかった。腹膜播種の治療成績は肝転移や肺転移に比べて不良であることが示されており4),UC関連大腸癌の予後が散発性大腸癌よりも不良である一因となっていることが推測される。
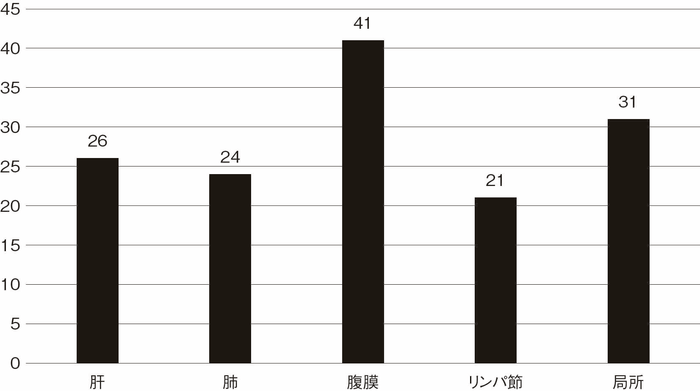
図21 UC関連大腸癌再発部位
文献
- Noguchi T, Ishihara S, Uchino M, et al.:Clinical features and oncological outcomes of intestinal cancers associated with ulcerative colitis and Crohn’s disease. J Gastroenterol 2023;58:14-24
- Watanabe T, Konishi T, Kishimoto J, et al.:Ulcerative colitis-associated colorectal cancer shows a poorer survival than sporadic colorectal cancer:a nationwide Japanese study. Inflamm Bowel Dis 2011;17:802-808
- Lu C, Schardey J, Zhang T, et al. Survival Outcomes and Clinicopathological Features in Inflammatory Bowel Disease-Associated Colorectal Cancer:A Systematic Review and Meta-Analysis. Ann Surg 2021;276:e319-e330
- Franko J, Shi Q, Meyers JP, et al.:Prognosis of patients with peritoneal metastatic colorectal cancer given systemic therapy:an analysis of individual patient data from prospective randomised trials from the Analysis and Research in Cancers of the Digestive System(ARCAD)database. Lancet Oncol 2016;17:1709-1719









