患者さんのための大腸癌治療ガイドライン 2022年版
Q&A
-
大腸癌の予防法
Q1 大腸癌にならない予防法はありますか? -
大腸癌のステージ
Q2 ステージⅢの大腸癌といわれました。ステージとは何ですか? -
大腸癌の内視鏡治療
Q3‒1 早期大腸癌だから内視鏡で切り取ることができるといわれました。お腹を切らなくてもよいのでしょうか?
Q3‒2 良性のポリープは癌になることはありますか?切除した方が良いのでしょうか? -
リンパ節郭清
Q4‒1 大腸癌の手術の時,リンパ節も取るといわれました。なぜリンパ節を取るのでしょうか?
Q4‒2 リンパ節を取っても大丈夫ですか? -
大腸癌の手術治療
Q5‒1 手術が必要といわれ,大腸を20~30cm切り取るといわれました。後遺症は大丈夫でしょうか?
Q5‒2 手術を受けるにあたり,排尿機能と性機能に障害が残る可能性があると説明されました。なぜでしょうか?
Q5‒3 腹腔鏡下手術とは何ですか?
Q5‒4 ロボット支援下手術について教えてください。 -
入院から退院までの経過
Q6 大腸癌手術の入院から退院までの経過はどのようになりますか? -
大腸癌手術の合併症について
Q7 大腸癌の手術後にはいろいろな合併症が起こり得るとの説明を受けました。詳しく教えてください。 -
肛門括約筋温存の可否
Q8 直腸癌で永久人工肛門になるといわれました。人工肛門になるかどうかは,どのように決められるのでしょうか? -
人工肛門について
Q9‒1 人工肛門とはどういうものでしょうか?
Q9‒2 人工肛門はどのような管理をするのでしょうか?
Q9‒3 お風呂に入っても大丈夫なのでしょうか?旅行に行って,温泉に入れるのでしょうか?
Q9‒4 日常生活で困ることがあれば教えてください。 -
大腸癌の治療成績
Q10 大腸癌はどの程度まで治るようになりましたか?また,「5年生存率」とは何ですか? -
大腸癌の再発
Q11‒1 癌を全部切り取ったのに,どうして再発が起こるのでしょうか?
Q11‒2 再発は早期に見つければ治るのでしょうか?
Q11‒3 再発した時の治療法はあるのでしょうか? -
大腸癌の薬物療法
Q12‒1 大腸癌の薬物療法ではどんな薬がありますか?また,どんな副作用が起こりますか?
Q12‒2 大腸癌の遺伝子検査とは何ですか?分子標的薬が使える患者さんと使えない患者さんがいると聞きますが,どうしてですか?
Q12‒3 分子標的薬を単独で使った場合,効果は減少しますか?
Q12‒4 薬物療法で重い副作用を起こしてしまった場合,その後,薬物治療はできないのでしょうか? -
大腸癌の補助化学療法
Q13 手術で癌を取り除いたら,もう治療はしなくて良いでしょうか?手術で取ったリンパ節に転移が見つかり,抗がん剤治療を奨められました。 -
切除不能進行・再発大腸癌の薬物療法
Q14‒1 肝臓と肺に転移して,抗がん剤治療を奨められました。抗がん剤治療は効くのでしょうか?
Q14‒2 ステージⅣの大腸癌といわれました。抗がん剤が効かなくなった場合はどうなるのでしょうか?
Q14‒3 抗がん剤を休むと,症状が進んでしまいますか? -
放射線治療
Q15 大腸癌の放射線治療について教えてください。 -
大腸癌手術後の生活について
Q16‒1 大腸癌手術後の食事のとり方について教えてください。
Q16‒2 大腸癌手術後の生活で気をつけることは何ですか?仕事に復帰することはできますか? -
大腸癌手術後のサーベイランス
Q17 大腸癌手術後に,定期的に通院して検査が必要といわれました。どのような検査をするのでしょうか?また,いつまで通院する必要があるのでしょうか? -
大腸癌の腫瘍マーカー
Q18 大腸癌手術後の検査で,CEAが高いので検査をするといわれました。どのような意味なのでしょうか? -
「説明と同意」
Q19 大腸癌の治療を始めるにあたって「説明と同意」に署名を求められました。これは必要なことでしょうか? -
セカンドオピニオン
Q20‒1 大腸癌と診断されましたが,お医者さんによって奨められた治療法が異なります。どうしたらよいでしょうか?
Q20‒2 ガイドライン以外の治療法を奨められましたが,決心がつきません。 -
代替療法
Q21‒1 友人に代替療法を奨められました。効果はあるのでしょうか?
Q21‒2 光免疫療法は大腸癌に奨められるでしょうか? -
臨床試験
Q22 担当医から臨床試験の説明がありましたが,参加しようかどうか迷っています。臨床試験とはどのようなものですか? -
高額療養費
Q23‒1 高額療養費とは何のことですか?
Q23‒2 ロボット支援下手術を受けると治療費が高額になりますか? -
がんゲノム医療
Q24 がんゲノム医療とはどのようなものですか?
大腸癌の予防法
A がんの予防に関しては国立がん研究センターをはじめとする研究グループで多くの調査がなされています。その中で日本人のがん予防には,禁煙,節酒,食生活,身体活動,適正体重の維持,感染の6 項目が重要であると考えられています。このうち“感染”以外の5項目は生活習慣に関わるもので,これらに気をつけた生活をおくるとがんのリスクはほぼ半減するということが示されています。
大腸癌に関しては,確実にそのリスクを上げるものとしては,喫煙,アルコール,ほぼ上げることが分かっているものとして肥満があげられています。また女性においては加工肉/赤肉の摂取がリスクを上げる可能性があるとされています。一方で,運動は大腸癌のリスクを下げることがほぼ確実といわれ,他にリスクを下げる可能性があるものとしては,食物繊維,カルシウム,魚由来の不飽和脂肪酸などが報告されています。また女性においてはコーヒーがリスクを下げる可能性があるとされています。
ただし,大腸癌の発生を確実に抑える有効な予防法は,現在のところ確立していません。大腸癌に限らず生活習慣病を予防するためには,バランスの良い食事,適度な運動,規則正しい生活を心がけることが大切だといえます。
大腸癌のステージ
A 「ステージ」は「病期」ともいい,大腸癌の広がりの程度を表したものです(図10参照)。ステージ分類には日本の大腸癌取扱い規約分類と国際的なTNM分類があります。どちらの分類でも,癌が大腸の壁のどの位の深さまで進んでいるか(壁深達度),リンパ節にどの程度転移しているか(リンパ節転移),肝臓や肺などのほかの臓器に転移しているか(遠隔転移)によりステージ0からステージⅣに分けられています。治療前にCTなどの画像診断でステージ(臨床分類ステージ)を予測し,切除された大腸などの組織を顕微鏡で調べた結果をあわせて最終的なステージ(病理分類ステージ)を決定します。大腸癌の治る可能性や,逆に再発する可能性をステージから予測できるため,治療方針の決定に役立ちます。
ステージⅢは,遠隔転移がなく,癌の周囲にあるリンパ節に転移があることを示しています。この場合,手術後に抗がん剤による補助療法を行うことが奨められています(「ステージ0~ステージⅢの大腸癌の治療」参照)。
大腸癌の内視鏡治療
A 大腸癌は大腸の粘膜(図5参照)から発生し,大腸壁の深い方へと浸潤していきます(図9参照)。早期大腸癌とは,癌の浸潤が粘膜下層までにとどまっている癌で,粘膜内癌(Tis癌)と粘膜下層癌(T1癌)に分けられます(図10参照)。Tis癌は転移しないので,内視鏡により癌が完全に取り切れれば,治療は完了です。一方,T1癌の場合は,遠くの臓器に転移する頻度は少ないものの,リンパ節に転移している可能性が10%前後あります。
癌の存在する部位,大きさ,浸潤の深さなどを総合的に評価して,癌病巣を安全かつ完全に切除することができると判断される早期大腸癌が内視鏡治療の対象となります。内視鏡で切除された癌は,顕微鏡を用いた詳細な検査(病理検査)に提出されます。この検査により癌がすべて取り切れたかどうかを調べるとともに,Tis癌かT1癌かが判定され,T1癌の場合は,リンパ節転移の危険性が評価されます。Tis癌や転移の危険性が低いT1癌と判断された場合は,内視鏡治療で治療は完了し,転移の危険性が高いT1癌と判断された場合は追加の治療としてリンパ節郭清(図21参照)を伴う腸切除が考慮されます。
A 良性のポリープでも放置すると癌になるものがあります。そのひとつに「腺腫」とよばれるポリープがあります。腺腫は大きくなるほど癌が発生するリスクが高くなるため,径6mm以上の腺腫は内視鏡的摘除の適応と考えられています。また,「過形成性ポリープ」とよばれるポリープは,「腺腫」に比して癌発生のリスクが低く,切除せずに放置する場合がほとんどです。一方,「鋸歯状病変」とよばれるポリープは一部に癌発生のリスクを有するものがあり,径10mm以上の病変を治療の適応とする施設が多いようです。すなわち,良性のポリープは「腺腫」なのか「過形成性ポリープ」なのか「鋸歯状病変」なのか,大きさはどの程度なのか,といったことを確認して切除するかどうかを判断しています。
リンパ節郭清
A リンパ節は,からだの中にたくさんある小さな(普通は径0.4~1.0cm)組織で,細菌などのからだにとって不都合な侵入物が体中に広がるのを止める“関所”の役割をしています。首すじやわきの下,足の付け根など,表面に近いリンパ節が腫れると,さわることができます。
大腸癌が広がるおもな道筋はリンパ管と静脈です(図9参照)。リンパ管に入り込んだ癌細胞は,リンパ管を通って大腸の周りのリンパ節に流れ込みます。多くの癌細胞はからだの攻撃により死滅しますが,生き残った癌細胞が増えるとリンパ節転移が形成され,時間の経過に伴って,より遠くのリンパ節に順次転移が進みます。
大腸癌がある程度進行すると,近くのリンパ節には癌細胞が潜んでいる可能性が高くなります。CTやPETで転移が疑われていなくても,細胞レベルでの転移が成立している可能性もあることから,手術では転移の可能性があるリンパ節を大腸癌と一緒に切除します。これをリンパ節郭清といいます。リンパ節郭清の範囲は,大腸癌のステージに応じて決められます(図21参照)。
A リンパ節はからだ全体に多数分布しています。大腸癌の手術で切除されるリンパ節は,切り取られる大腸の領域から集まってくるリンパ液の関所の役割をしています。手術では大腸癌に関連した領域のリンパ節を取るだけですので,その領域のリンパ節を取ってもからだに悪影響はありません(「手術治療」参照)。
大腸癌の手術治療
A 大腸の手術後の後遺症は,結腸癌と直腸癌で異なります。大腸の長さは1.5~2mほどあり,結腸を20~30cm切除しても,大腸のおもな機能である水分の吸収は残った大腸で十分に果たせますので後遺症はほとんどありません(「大腸とは」参照)。これに対し,直腸を切除した場合には,本来直腸に備わっている便をためる能力と便を押し出す能力が損なわれるため,排便の回数が増加したり,残便感が持続するなどの排便機能障害をきたす可能性がでてきます。また,肛門近くの直腸癌の場合は肛門を温存できたとしても,便失禁やがまんができないなどの症状を認める場合もあります。一般的にはこのような後遺症は手術直後に強く,半年から2年ほどの年月をかけて徐々に改善しますが,回復の程度には個人差があります。
A 直腸の周囲には神経のネットワーク(骨盤内自律神経)が存在します。この神経は膀胱や尿道などの泌尿器や,前立腺や膣などの生殖器に分布しています。直腸癌が神経ネットワークに浸潤したり,神経の近くに転移リンパ節がある場合,根治手術を行うためには,自律神経のネットワークの一部,または全部を切除する必要性が生じます(「直腸癌の手術」参照)。神経の切除範囲に応じて,程度は異なりますが,尿意が鈍くなり,排尿しても膀胱に残っている尿量(残尿)が多くなります。これを排尿障害といいます。また,男性の場合は射精障害や勃起障害が生じ,女性の場合は膣の湿潤度などに影響し,性交渉に障害がでる場合があります。
A 開腹手術はお腹を大きく切って,直接見ながら手を使って手術を行います。一方,腹腔鏡下手術はお腹を大きく切らずに穴をあけて「腹腔鏡」というカメラを挿入し,テレビ画面で内部を見ます。また,手術操作は穴から細長い器具を入れて行います。手術の創が小さいため外見上目立たないこと,痛みが少ないこと,腸の運動低下が少ないため手術後の回復が早く入院期間や休職期間が短いことが長所です。
開腹手術と異なる技術を要するため,大腸癌の部位や進行度などにより医師とよく相談の上で手術方法を決める必要があります。
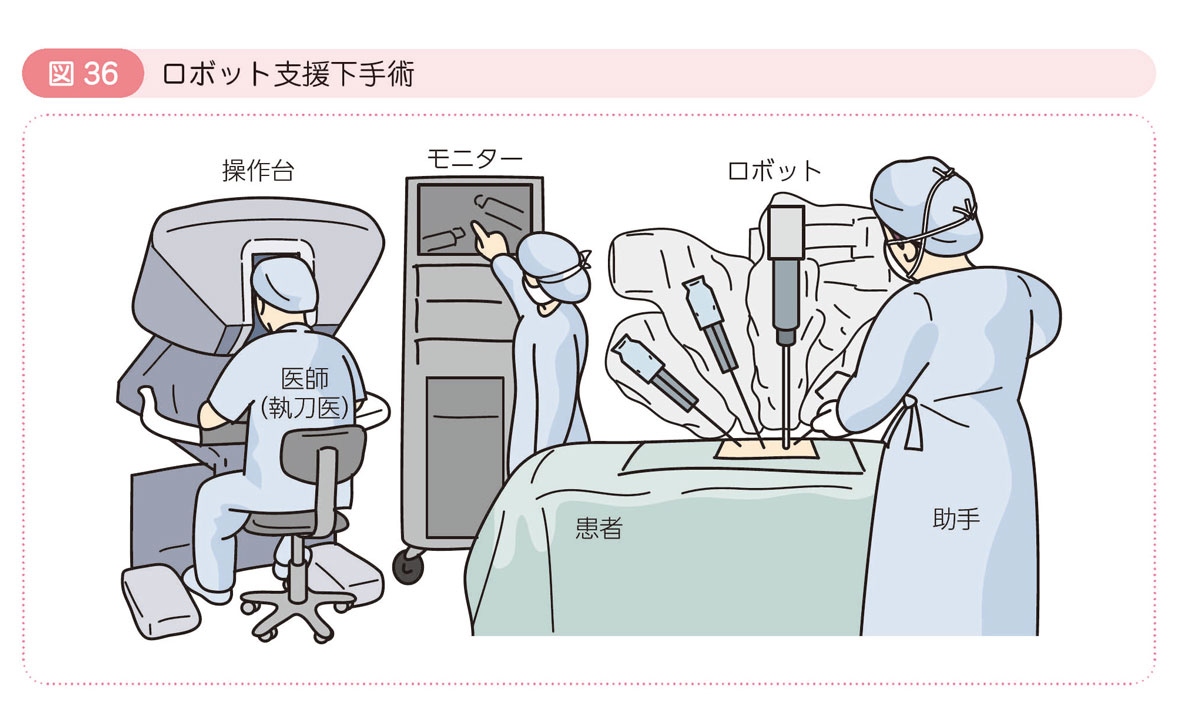
A 大腸癌に対する手術には,開腹手術,腹腔鏡下手術,ロボット支援下手術があります(「腹腔鏡下手術」参照)。大腸癌に対するロボット支援下手術は,2018年4月に直腸癌に対する術式として保険適用となりました。ロボット支援下手術とは,腹腔鏡下直腸切除術をロボット支援下に行うものです。術者は操作部に座り,患者さんの体の近くにおいたロボット本体を遠隔で操作します。腹腔鏡下手術と異なる点として,より高性能な3Dカメラを使用していること,鉗子に関節があり自由に曲がること,カメラも鉗子も手振れがしないことなどから,より繊細で精密な手術を行うことができます(図36)。結果として,癌をしっかり取り切ること(癌の根治性)とともに直腸の周囲に存在する神経を確実に温存することで,排尿・性機能障害を回避することが期待されています。ただし,現時点では,ロボット支援下手術の治療成績や合併症の頻度についてはまだ十分に検証されておらず,今後の課題といえます。
入院から退院までの経過
A 手術を行う医療機関や病状により多少異なりますが,一般的な手術の流れについて説明します。
- 1)
- 入院前または入院後:手術前に必要な一般的な検査として心電図や呼吸機能検査,血液検査を行い,手術に十分耐えられるか,検討します。
- 2)
- 手術前日は食事を中止し,下剤を飲んでいただき,腸の中をきれいにします。
- 3)
- 手術後の当日は,ベッド上で安静となります。
- 4)
- 手術翌日:起き上がり,可能なら歩行を行います。状態により水分摂取を開始します。
- 5)
- 手術後2~4日:腸の動きに合わせて食事を開始します。
- 6)
- 手術後3~7日:おならが出て,排便もあります。
- 7)
- 手術後7日以降:食事摂取が可能で,排便も順調であれば,体調により退院が可能となります。手術後10日~2週間で退院するのが一般的です。
大腸癌手術の合併症について
A 手術が原因となって生じる別の病気や症状を術後合併症といいます。薬の副作用に相当するもので,最大限の注意を払って治療を行っても一定の頻度で発生します。
大腸癌のおもな外科的合併症には,出血,縫合不全,吻合部狭窄,腸閉塞,創感染,腹腔内膿瘍,腹壁瘢痕ヘルニアがあり(「手術治療の合併症」参照),他にリンパ漏(リンパ液が漏れでておなかの中にたまること)などがあります。多くの合併症は退院までに起こることが多いですが,吻合部狭窄や腸閉塞は退院してからでも起こります。腸閉塞は手術後何年も経ってから起こることもあり,何度も繰り返す場合もあります。
一方,生命にかかわる重篤な合併症には,肺炎,肺塞栓症,心筋梗塞,脳梗塞などがあります。これらの合併症を予防するためには,手術後なるべく早くから体を動かすことが大切です。手術後なるべく早期に歩いていただくことで,腸の動きの回復が早くなり,また,腸が癒着して腸閉塞になることも予防できます。また,痰も出しやすくなるため肺炎の予防にもなります。足を動かすことで血流がよくなり肺塞栓の予防にもなります。手術の傷は痛いですが,痛み止めを使用しても手術後なるべく早くから体を動かしていただくことが大切です。
これらの合併症は,過誤や過失によるものではなく,患者さんの年齢,全身状態,併存する持病(糖尿病,高血圧,心臓疾患,呼吸器疾患,肝臓疾患など)の影響を大きく受け,同じ医師が同じように注意深く手術をしても一定の割合で不可抗力的に発生します。特にご高齢の方は持病が多く,体を動かすのも遅れることがあり,肺炎や心筋梗塞・脳梗塞などの合併症のリスクは高くなります。合併症に対する治療法は年齢によって大きく変わりませんが,認知症の有無や全身状態により治療方法がかわる可能性があります。手術に伴う合併症により不幸にして命を落とされる方(手術関連死亡率)は,大腸癌の手術を受ける患者さんの1~2%程度と報告されています。
肛門括約筋温存の可否
A 直腸癌の手術は,前方切除術と直腸切断術に大別されます(図24参照,図25参照)。腫瘍が肛門から比較的遠い口側に位置する場合,病変が存在する直腸を腹膜反転部より口側で切除してS状結腸と残った直腸を吻合します。これが前方切除術です。腹膜反転部より肛門側で直腸を切除して残った直腸と吻合する場合を低位前方切除術と言います。最近では,かなり肛門に近い直腸癌であっても肛門の機能を残す手術が行われるようになりました(「特殊な肛門温存手術ISR(括約筋間直腸切除術)」参照)。
一方,肛門の近くには3~4cmの長さにわたって肛門括約筋という構造があり,肛門から便が漏れる(便失禁といいます)のを防いでいますが,肛門の非常に近くに存在する直腸癌を完全切除するためには,肛門括約筋を一緒に切除しなければならないことがあります。肛門括約筋を広く切除すると,たとえ結腸と残った肛門をつなぎあわせても,手術後には高度の便失禁の状態となり,日常生活が非常に不便となります。このような場合には,吻合を行わず,直腸とともに肛門を一括して切除し,S状結腸で人工肛門を造ります。これが直腸切断術です。
解剖学的には前方切除術や低位前方切除術を行うことが可能な患者さんでも,縫合不全の発症が危惧される場合には,S状結腸と直腸の吻合を行わないことがあります。また,後遺症である排便機能障害により日常生活が著しく損なわれることが想定される患者さんにも,前方切除は選択されないことがあります。このような場合,体内に残った直腸の端は閉鎖し,S状結腸で人工肛門を造ります。この手術はハルトマン手術と呼ばれ,重度の併存疾患をお持ちの患者さんや高齢者に選択されます。
すなわち,直腸癌手術で永久人工肛門になるかどうかは,肛門括約筋を切除する必要があるかどうかによって決まります。それは直腸癌と肛門括約筋との距離と浸潤度によって決まります。また,前方切除術や低位前方切除術を行った場合の合併症や後遺症による生命や術後の生活の質への影響も,術式を決定する上で考慮すべき重要な要因となります。手術前に,なぜ人工肛門が必要なのかを担当医から説明してもらうことが大切です。
人工肛門について
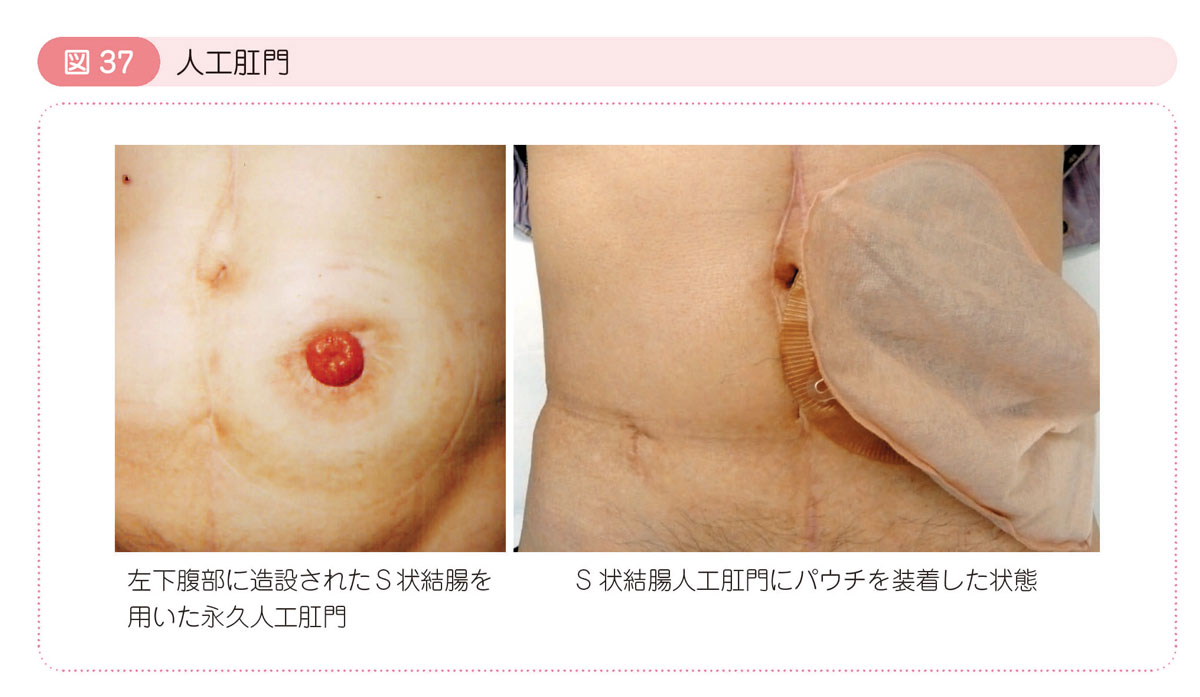
A 人工肛門とは人工的に造られた肛門(便の出口)のことで,ストーマともいいます。人工肛門という器具があるわけでなく,ご自身の腸の一部をお腹の壁に出して,そこから便が出るようにしたものです。結腸で造る場合と小腸(回腸)で造る場合があります。
人工肛門には,一時的人工肛門と,永久人工肛門とがあります。一時的人工肛門は,腸を吻合した後に縫合不全を引き起こす危険性が高いと考えられる場合に,予防的に吻合部の上流の腸管に造設されます。また実際に縫合不全が発生した際に,再手術時に造設される場合もあります(「縫合不全」参照)。多くは横行結腸か回腸に造られます。一時的人工肛門は,造設後3~4か月以降に,縫合不全がないことを確認した後に閉鎖され,本来の肛門から排便できるようになります。
一方,永久人工肛門のほとんどは直腸癌の手術の際に造設され,おもにS状結腸を用いて左中腹部に造られます。手術後に患者さん自身による人工肛門の管理がしやすいように,場所や形(1~2cmほど皮膚から突出した形)が工夫されます。永久人工肛門を保有される方は,身体障害者手帳を申請できます。住民票のある市区町村の福祉事務所に「身体障害者診断書・意見書(ぼうこう・直腸機能障害用)」を請求し,医療機関で診断書を作成してもらいます。
A 人工肛門を管理することをストーマケアといいます。ストーマケアは,人工肛門部に袋(パウチといいます)を貼って便を集める方法(自然排便法)が一般的です。パウチには粘着力のある面板という部分があり,中央に円形に穴が開いています。ここを人工肛門にあわせた上で,人工肛門の周りの皮膚に接着させます。自然排便法は,ストーマケアの基本的な方法で,体力のない方にも無理なく行える方法ですが,排便のタイミングを調整することはできません。
一方,人工肛門から微温湯(ぬるま湯)を入れることにより腸を刺激し,浣腸のように強制的に排便させる,洗腸排便法という方法があります。1日~2日に1度の洗腸で,一定の間は便が出なくなります。排便のタイミングを調整できる点で便利な方法ですが,人工肛門をお持ちのすべての患者さんに適しているわけではありません。洗腸のために1時間程度時間がかかりますので体力を要しますし,多量のお湯を腸の中に注入するため,不適切な方法で行うと腸穿孔などの危険性もありますので,開始にあたっては医療機関で十分に指導を受ける必要があります。
A 人工肛門の表面は粘膜でおおわれています。粘膜は皮膚よりもやわらかく出血しやすいので,やさしく取り扱う必要がありますが,お風呂や温泉に入ることに支障はありません。人工肛門の中にお湯が入りこんでも,人工肛門に石鹸がついても問題はありません。パウチをはずして湯ぶねにつかることもできます。入浴中に人工肛門から便が出ることが心配な方は,タオルを折りたたんで人工肛門にあてるか,パウチをつけて入浴します。肌色をして目立たない入浴用の小さなパウチもあります。温泉や銭湯など不特定多数の人が集まる場所では,このような装具を利用するとよいでしょう。洗腸排便法を行っていれば便が出ることがないので,そのままお風呂に入っても問題はありません。
A 人工肛門をつけても,食事に特別な制限はありませんし,適度なスポーツや旅行も可能です。ほとんどの患者さんが手術前の職場や学校に復帰されています。
人工肛門が自然肛門と違うのは,便の出る場所が腹部になることと,人工肛門には肛門括約筋がなく,排便や排ガスを自分でコントロールすることができないことです。
パウチと人工肛門周囲の皮膚との接着が十分でないと便が周囲に漏れますし,パウチの接着剤や皮膚についた便で皮膚炎を起こすことがあります。人工肛門の形や皮膚の性状に適したパウチを選択することが大切です。日常生活をする上で問題があると感じた場合は病院で相談してください。「ストーマ外来」を設けて,医師や専門の看護師が人工肛門に関する管理・教育を行っている病院もあります。
大腸癌の治療成績
A どの程度の期間に再発がなければ「治った」とみなしてよいかは,癌の種類によって異なります。大腸癌では,根治術から5年後に再発を認めない場合に「癌が治った」と考えるのが一般的です。大腸癌は手術後5年以上経って再発する確率は1%以下だからです。ただし,現代では,たとえ治癒切除不能大腸癌であっても,治療法の進歩により,長期延命が可能となっており,生存期間だけで「治った」と判断できない場合もあります。
癌治療の現場では「5年生存率」という言葉がよく使われます。「5年生存率」とは,癌の治療開始から5年後に生存している人の割合を示し,治療成績を評価するための大切な指標となります。5年生存率に強く関連するのがステージです(Q2参照)。
大腸癌研究会の集計(全国大腸癌登録2008年)によれば,ステージ別の5年生存率は,ステージⅠでは92%,ステージⅡでは84%,ステージⅢaでは81%,ステージⅢbでは65%,ステージⅣでは21%でした。
大腸癌の再発
A 手術前にはCT,MRIやPET-CTなどの精密検査を行うのですが,それらの検査でもある程度の大きさがないと映らないため,細胞レベルの微小な癌は診断できません。手術で癌を全部取り切ったと判断しても,肉眼的には把握できない細胞レベルの癌が体内に残っていることがあります。再発とは,手術後に体内に潜んでいた微小な癌が少しずつ大きくなって目に見えるようになることです。
再発する割合は大腸癌のステージによって異なります(「再発する割合」参照)。それは,ステージが悪くなるにしたがって目に見えない細胞レベルのがん細胞が遺残している可能性が高くなるからです。大腸癌研究会・全国登録 2007年の集計によれば,ステージ別の再発率はステージⅠでは5.7%,ステージⅡでは15.0%,ステージⅢでは31.8%でした。
A 再発を早く見つけたから治るとは限りません。再発が見つかった時点で多数の病巣が存在したり,切除できない場所に再発することがあるからです。一方,発見が遅れたために切除ができなくなることも少なくありません。そこで,手術で癌が完全に取り切れたとしても,再発の発見のために手術後5年までの間,再発のリスクに応じたスケジュールで検査を行います。また,再発した場合の治療方針は施設によって異なることがあります。セカンドオピニオンなどを利用していろいろな施設での治療方針を確認することも重要です。
A 大腸癌が再発する臓器のなかで割合が高いのは,肝臓と肺です。いずれの場合でも,患者さんの体力や術後の機能を勘案し,再発した癌をすべて切除することが可能と判断されれば手術が奨められます(「再発した大腸癌の治療」参照)。
肝臓に転移した癌の30~40%に手術が行われています。手術ができない場合は,薬物療法を行います(「薬物療法」参照)。薬物療法には,経口抗がん剤のほか,静脈から抗がん剤を注入する方法(全身薬物療法)があります。
肺に転移した場合でも手術の可否が検討され,手術ができないと判断された場合は,全身薬物療法を行います。最近は,最初に手術ができないと判断されていても薬物療法が効いて手術ができるようになることも増えてきました。
大腸癌の薬物療法
A 大腸癌に対する薬物療法の基本となる薬は,殺細胞性抗がん剤という従来からある癌細胞のDNAを標的とした治療薬です。最も重要な薬は,5フルオロウラシル(5-FU:ファイブ・エフ・ユー)であり,注射薬以外に,飲み薬としてUFT(ユー・エフ・ティー),TS-1(ティー・エス・ワン),カペシタビンなどがあります。注射薬の5-FUはロイコボリンというお薬と一緒に使い,別の殺細胞性抗がん剤であるイリノテカン(CPT-11:シー・ピー・ティー・イレブン)やオキサリプラチンと組み合わせる,FOLFOX(フォルフォックス)やFOLFIRI(フォルフィリ)という治療もあります。この治療を外来で行う場合には5-FUは約46時間の持続投与を中心静脈ポートから携帯型持続注入器(インフューザー)を用いて行います。飲み薬との組み合わせでは,カペシタビンとオキサリプラチンを組み合わせたCAPOXや,TS-1とイリノテカンを組み合わせたIRIS(アイリス)などがあります。
分子標的薬は,癌細胞や栄養血管の増殖因子を標的とした治療薬であり,血管新生阻害薬としてベバシズマブ(アバスチン®),アフリベルセプト(ザルトラップ®),ラムシルマブ(サイラムザ®)が,抗EGFR抗体薬としてセツキシマブ(アービタックス®),パニツムマブ(ベクティビックス®)が,単独もしくは他の抗がん剤と組みあわせて使用されます。
他にはレゴラフェニブ(スチバーガ®),トリフルリジン・チピラシル(ロンサーフ®)なども使用されます。
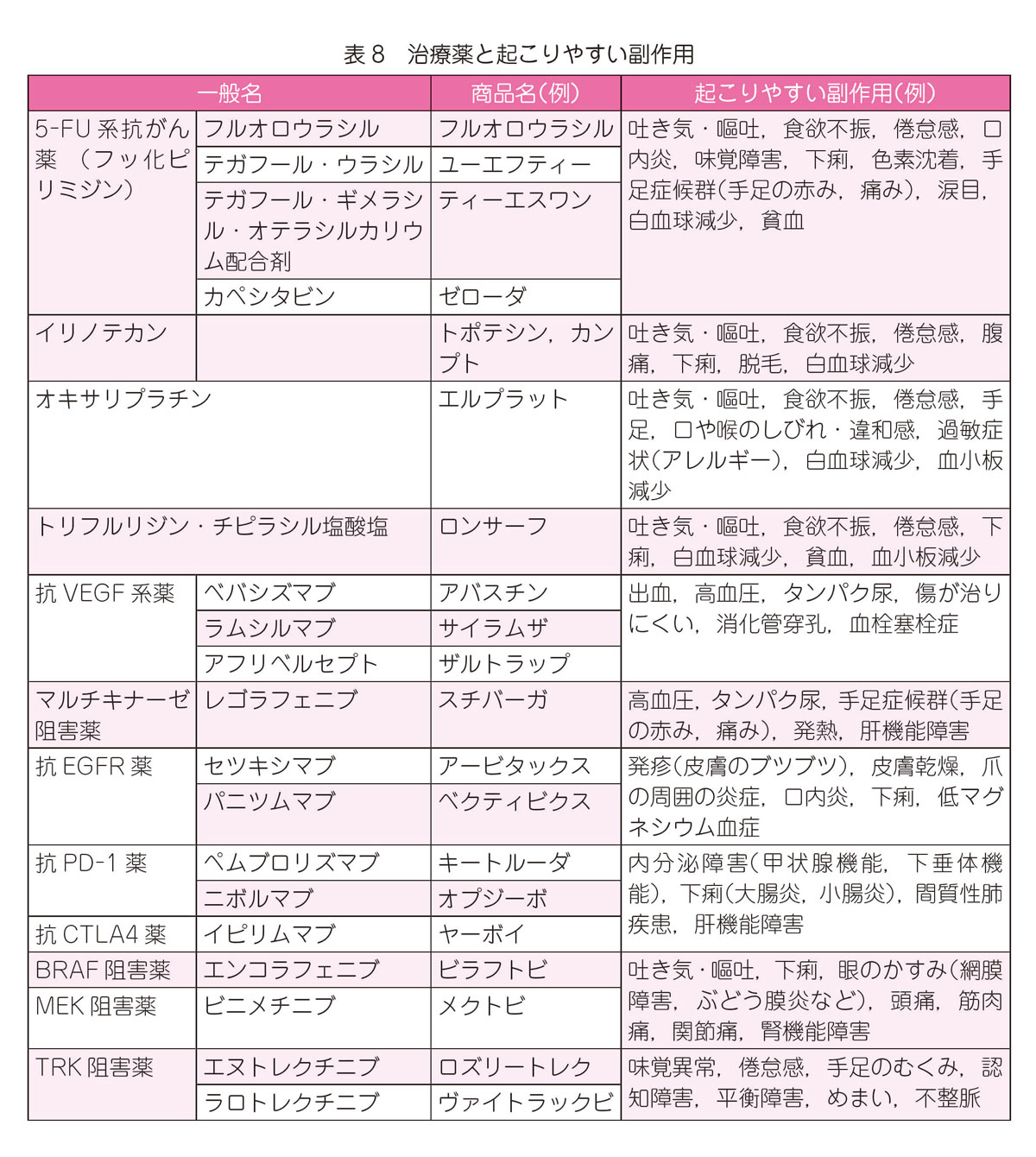
これらの薬物療法は治療効果が高いのですが,副作用への十分な対応も必要です。例えばイリノテカンには,食欲不振,重症の下痢,脱毛や骨髄抑制(白血球の減少),オキサリプラチンには,骨髄抑制に加え神経症状(手足のしびれ,のどのしめつけ感など)など,治療薬によって様々な副作用があります(表8)。また,これら分子標的薬も含めて,抗がん剤だけで大腸癌を完全に治すことはできません。重い副作用の危険性もあるので,慎重に治療法を選ぶ必要があります。
A 遺伝子検査には,患者さんの体質,遺伝を調べる遺伝学的検査と,癌のどのような遺伝子に傷がついているかを調べるがん遺伝子関連検査があります。前者の例には,UGT1A1遺伝子多型検査があり,これは大腸癌の薬物療法に使用するイリノテカンの副作用の出方を予想するために行う検査です。
後者の遺伝子関連検査として,大腸癌では癌細胞を用いたRAS遺伝子検査,BRAF遺伝子検査,MSI検査があります。これらの遺伝子異常により,特定の薬物療法の治療効果に差があります。大腸癌の約50%にRAS(KRASまたはNRAS)遺伝子変異があり,変異がある場合には抗EGFR抗体薬の効果が期待できないことが知られています。また,BRAF遺伝子変異は,大腸癌の約5%に認められ,変異陽性の場合には,BRAF阻害剤であるエンコラフェニブ(ビラフトビ®),MEK阻害剤であるビニメチニブ(メクトビ®)が効果を示すことが知られています。また,MSI(マイクロサテライト不安定性)とは,DNAの複製の際に生じる配列間違いを修復する機能の状態を表しており,大腸癌の約3%に認められるMSI—Highの場合には,免疫チェックポイント阻害剤であるペムブロリズマブ(キイトルーダ®),ニボルマブ(オプジーボ®)やイピリムマブ(ヤーボイ®)の治療が効く可能性があります。そのため,進行・再発大腸癌に対する薬物療法を行う前には,癌の組織を用いてこれらの遺伝子関連検査を行って,それぞれの患者さんの大腸癌の遺伝子の特徴(どの遺伝子に異常があるか)を把握しておくことが重要です。
A 分子標的薬の中で血管新生阻害薬であるベバシズマブ(アバスチン®),アフリベルセプト(ザルトラップ®),ラムシルマブ(サイラムザ®)は殺細胞性抗がん剤と併用することによって,治療効果を発揮します。抗EGFR抗体薬であるセツキシマブ(アービタックス®)やパニツムマブ(ベクティビックス®)は,単独で使った場合にも治療効果があることが分かっていますが,より効果を高めるため他の抗がん剤と併用することが多いです。分子標的薬を単独で使用するか,他の抗がん剤と併用するかについては期待される治療効果と副作用などから判断されます。
A 抗がん剤による重い副作用の例としては,アナフィラキシーショック,間質性肺障害,消化管穿孔などが報告されています。これらの薬剤に起因したと考えられる重い副作用が生じた場合には,その後これらの薬剤の使用については,再投与によって同様の副作用が生じるリスクと期待される治療効果のバランスを考慮して判断します。期待される効果よりもリスクが高いと判断した場合には,再投与はお奨めされません。
大腸癌の補助化学療法
A 手術後の再発を抑える目的で行う薬物療法を補助化学療法といいます。ただし,補助化学療法がすべての大腸癌の再発の予防に効果があると確認されたわけではありません。ステージⅢの結腸癌に対しては,再発を予防し,生存率を高める効果があるとされています。リンパ節に転移があった場合はステージⅢですから,補助化学療法をお奨めします。補助化学療法は,あくまでも予防を目的とし,6か月間注射する方法か,抗がん剤を飲んでもらう方法が一般的です(「術後補助化学療法」参照)。また,ステージⅡやステージⅣの患者さんで,再発リスクが高いと考えられた患者さんにも補助化学療法が奨められることがあります。
切除不能進行・再発大腸癌の薬物療法
A 肝臓や肺へ転移した癌もすべてを切除することにより治ることがあります。
しかしながら,肝臓や肺にいくつもの転移があったり,肝臓や肺以外の臓器にも転移があり手術で癌を完全に取り除くのが難しい場合は,手術をせずに薬物療法を行います。肝臓や肺の病巣も,もともとの大腸癌が転移したものですので,使用する抗がん剤は肝臓癌や肺癌に対する薬ではなく大腸癌に対する治療薬を用います。
薬物療法で大腸癌を完治させることはできませんが,癌を小さくすることで,手術ですべての病巣が切除可能となった場合には,手術することで癌を治すことができる場合もあります。また切除できない場合も,癌の進行を遅らせることで,その患者さんの生存する期間を延長させる効果があることが示されています。
ただし抗がん剤は癌細胞だけでなく,正常の細胞にも障害を与えるために副作用がでてきます(「薬物療法の副作用」参照)。副作用の種類や程度は抗がん剤の種類や個人の体質により異なります。また,添付文書に記載されている副作用がすべてでるわけではありません。現在では,副作用を軽くしたり予防したりする薬の開発もすすみ,特に吐き気・嘔吐に対しては十分な対応ができるようになってきています。薬物療法を受ける場合は,担当医からどのような副作用(種類や時期,期間,対処方法など)がでるのかの説明をよく聞いて,治療を受けてください。
A 標準治療とは臨床試験により治療効果が証明されている治療であり,標準治療の抗がん剤が効かなくなった場合には,癌の進行をコントロールするのが困難です。癌による症状を緩和する緩和医療を継続しながら,どのように対応していくのが患者さんにとってベストなのか担当医や医療スタッフと相談しながら決めていきます。
A 副作用がひどい場合には抗がん剤を休むことが必要です。副作用が回復してから,抗がん剤を再開すれば治療効果に影響はありません。また,副作用のない場合でも,一定期間は抗がん剤を休んでも抗がん剤による延命効果は変わりません。ただし,長期間休むと多くの場合には癌はまた大きくなると考えられますが,そのスピードには個人差があります。治療を休みたい場合は担当医と相談しましょう。
放射線治療
A 大腸癌に対して現在行われている放射線治療としては大きく分けて2通りあります。1つは直腸癌に対して行われる手術前もしくは手術中・手術後に行われる治療で手術治療に放射線治療を加えることによって骨盤内の再発予防や人工肛門を避けることを目的としており,多くの場合は放射線の効果を高める抗がん剤を組み合わせ,外来通院で行われます。また肺や脳に転移があっても,小さく数が少ない場合に適応になる場合があります。
もう1つは再発した大腸癌の症状緩和を目的に骨盤内再発,骨転移,リンパ節転移などに行われる治療で約80%に痛みなどの症状の改善がみられます。最近では多方向から正確に照射できるような機器を用いるようになってきたため非常に有効性が増し,副作用も軽減しています。
大腸癌手術後の生活について
A 原則として,退院後の食事に制限はありません。しかしながら,手術後間もない間は腸の運動が十分に回復していないことがあるため,食べ過ぎに注意し,食物繊維の多い食べ物や消化しにくいものは避けるのがよいでしょう。術後1か月もすれば元どおりの食生活に戻してもらってかまいませんが,腹部膨満感や便秘などの症状があれば主治医に相談してください。
A 大腸を切り取ったことによる栄養吸収の低下や体重減少はほとんどありません。盲腸から横行結腸までの癌の手術後は,ほぼ元どおりの生活ができます。一方,S状結腸や直腸の手術後は,しばしば排便の様子が変わります。排便回数の増加,1回の排便量の減少,残便感(排便後に便が出きっていない感じがすること)などの排便障害が起こります。直腸切除後はさらに,便のもれやガスと便の識別困難が起こることもあります。これらの症状は数か月である程度改善しますが,完全には戻りません。生活習慣を考慮して順応していく必要があります。
社会復帰はほぼ全員が可能ですが,その時期は,年齢や体力,社会的状況,仕事内容,手術術式などにより異なりますので,個々の状況に応じて対応すべきです。目安としては術後1か月が,ある程度余裕をもって復職可能な時期です。気分も良く,体力を含めすべて回復したと感じる時期は2~3か月後,というアンケート調査結果がありますので,無理をせずに徐々に生活を戻していくことが肝要です。
大腸癌手術後のサーベイランス(「サーベイランスの方法」参照)
A 手術後の経過観察(サーベイランス)は,早い時期に再発を発見して,効果的に治療するために行います。再発の頻度は大腸癌のステージによって異なるので,サーベイランスのスケジュール(通院の間隔)もステージによって異なります。検査の内容は,通常の診察,腫瘍マーカー測定(血液検査の一部で,癌が再発した時に高くなるたんぱく質です),CT,大腸内視鏡検査などです。必要に応じてMRIやPETも行います。サーベイランスのための通院期間は手術をしてから5年が原則です。
大腸癌の腫瘍マーカー
A 正常細胞よりも癌細胞で多量に作られて血液中に放出される物質で,癌の補助的な診断に用いられるものを腫瘍マーカーといいます。CEA(癌胎児性抗原)もその1つで,大腸癌が再発すると8割以上の人で血液中のCEAの値が上昇します。CEAが高くなると,再発を疑ってCTなどの検査を行い,再発した場所を探して治療をします。ただし,煙草を吸う方や糖尿病,肝臓病の方は,癌の再発がなくてもCEAが上がることがあります。大腸癌ではCEAのほかにCA19-9,p53という腫瘍マーカーを測ることもあります。
「説明と同意」
A 現在はどのような病気でも,医師は患者さんに病気や病状,治療法を説明した上で,患者さんからの同意を得てから治療を行います。治療法によっては強い副作用や不可抗力な事故が発生する危険性を伴うため,治療を始めるにあたって医師は患者さんにとって不都合な事態について患者さんに理解を求めることが必要です。そのために,医師は病気や治療の内容を口頭と文書で患者さんに説明し,患者さんに治療方法を納得していただきます。その際,治療法について医師と患者さんの間で無用なトラブルが生じないよう覚書をかわす意味で署名をします。治療法に納得がいかなければ,その治療を受ける必要はありません。その場合は署名をする必要はありません。しかし最も重要なのは医師と患者さん相互の信頼関係です。
セカンドオピニオン
A 大腸癌の標準治療はある程度確立していますが,有効性が十分に確認されておらず,医師により意見が異なる治療法も少なくありません。そのような場合,一人の医師の考えだけではなく,他の医師の意見をきくこと(セカンドオピニオン)も,ご自分が納得して治療を受ける上で役に立ちます。セカンドオピニオンについてはどの医師も理解していますので,今までかかっていた医師に気楽に相談していただければと思います。
A ガイドラインとは標準治療の基本を記したものです。大腸癌の治療のなかには,標準治療がまだ決まっていないものもあります。また,標準治療よりもさらに効果の高い治療法を目指した臨床試験もあります。病院によっては独自の治療法を開発し,その方法を患者さんに奨めるところもあります。治療法の選択で迷った場合は,他の病院でのセカンドオピニオンを求めるとよいでしょう。肝心なことは自ら納得して治療法を選ぶことです。
代替療法
A 代替療法は,治療の基盤となる手術治療,薬物療法,放射線療法以外で,それらを補う治療法に位置づけられます。免疫細胞療法,鍼治療,精神療法,サプリメントなど幅広いものが含まれます。しかし,代替療法によって癌が小さくなったり,癌が治ったりする効果が科学的に証明されたものはありません。ただ,代替療法を行うことで,精神的な安心感が得られる場合があります。代替療法を受けるか否かについては,担当医と十分相談されることをお奨めします。
A がん細胞だけに吸着する薬剤を投与した後,正常なヒト組織にはほぼ害を与えない近赤外光を照射することでがん細胞を死滅する治療法です。手術などの治療法では治療できない難治性再発頭頸部がんが保険適用となっております。現在のところ,大腸癌に対して有効であったという報告はなく,保険適用となっていません。
臨床試験
A 新しい検査法や治療法が安全で有効であるかを科学的に証明するための研究的な診療を臨床試験といいます。臨床試験にはさまざまなタイプのものがありますが,代表的な臨床試験では,現在標準治療とされている治療法とそれと同等以上の効果が期待される治療法を,医師や患者さんの意思や好みでなく,一定の決まりにより振り分けて治療し,その効果を比較して調べることもあり,この方法を無作為化比較試験といいます。臨床試験は患者さんをはじめとして,多くの専門家が関わって長い年月をかけて行われます。患者さんの意思で治療法を選べないため,参加をためらわれる方もいらっしゃいます。しかし,信頼できる新しい効果的な治療法を開発するためには臨床試験が不可欠ですので,患者さんには臨床試験の内容をよく理解していただき,できるだけ参加していただきたいと思います。
高額療養費
A 手術による入院や化学療法の費用が高額となる可能性があります。そこで「同じ月内」に,受けた保険診療に係る一部負担金(自己負担額)が「自己負担限度額」を超えた場合,超えた額が「高額療養費」として支給されます。お住まいの地域の行政窓口サービス課(保険年金:保険)で申請してください。
なお,室料差額(差額ベッド代)や歯科の材料差額など,保険診療外のものは,「高額療養費」の対象になりません。詳しくは病院の医療ソーシャルワーカーや会計担当者にお聞きください。
(厚生労働省サイト:https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/iryouhoken/juuyou/kougakuiryou/index.html)
A 2020年7月より腹腔鏡下直腸切除・切断術がロボット支援下手術の保険適用になりました。診療報酬点数は,腹腔鏡下直腸切除術が75,460点,腹腔鏡下低位前方切除術は83,930点,腹腔鏡下直腸切断術が83,930点となっています。診療報酬点数は,1点あたり10円を乗じて医療費を算出します。診療報酬点数の合計は,上記の手術点数のほかに麻酔や検査・入院料等が加わりますので,患者さんの状態によって異なりますが,以下に1例を示します。
概算の医療費(3割負担として計算)
腹腔鏡下直腸低位前方切除術 40~50万円(入院日数7~10日)
また,年収によってかわりますが高額療養費制度を利用すれば患者さんが負担する費用は10万円前後となります。
がんゲノム医療
A がんゲノム医療とは,がん組織や血液を用いて,がん遺伝子パネル検査を行い癌関連遺伝子異常を網羅的に調べ,その遺伝子検査の結果を参考に,個人の癌に合った分子標的治療薬を投与する個別化医療です。プレシジョン・メディシン,精密医療とも呼ばれます。大腸癌でも標準治療終了が見込まれる患者さんに,がん組織や血液を用いたがん遺伝子パネル検査を実施することができます。全国にがんゲノム医療中核拠点・拠点・連携病院が指定されており,全国どこでもがんゲノム医療が受けられるようになることを目指して,体制づくりが進められています。詳細は担当医師におたずねください。









